Testes para Diagnóstico

TESTES PARA DIAGNÓSTICO DE COVID-19
21/08/2021 a 27/08/2021
Na atual pandemia de COVID-19, é necessário um melhor entendimento da relação entre a simples ligação e os anticorpos funcionalmente neutralizantes para caracterizar a imunidade antiviral protetora após a infecção ou vacinação. Um painel de 123 amostras de plasma de uma população de estudo de COVID-19, pré-selecionado por teste semiquantitativo anti-SARS-CoV-2 IgG, foi usado para avaliar a relação entre o novo ELISA quantitativo (IgG) e um ensaio de microneutralização. A ligação de IgG direcionada ao antígeno S1 foi detectada em 106 (86,2%) amostras usando o QuantiVac ELISA, enquanto 89 (72,4%) amostras apresentaram atividade de anticorpos neutralizantes. A análise de correlação de Spearman demonstrou uma forte relação positiva entre os níveis de IgG anti-S1 e os títulos de anticorpos neutralizantes (rs = 0,819, p <0,0001). Níveis altos e baixos de IgG anti-S1 foram associados a um valor preditivo positivo de 72,0% para anticorpos neutralizantes de alto título e um valor preditivo negativo de 90,8% para anticorpos neutralizantes de baixo título, respectivamente. Estes resultados fundamentam a implementação do QuantiVac ELISA para avaliar a imunidade protetora após a infecção ou vacinação (20/08/2021). Fonte: Journal of Medical Virology
14/08/2021 a 20/08/2021
Estudo busca verificar que a saliva pode ser uma fonte alternativa potencial de amostra para o diagnóstico de infecção por SARS-CoV-2 por PCR de transcriptase reversa (RT-PCR). Dos resultados a amostragem de saliva é uma alternativa aceitável frente ao esfregaço oro-nasofaríngeo (ONPS) para diagnosticar a infecção por SARS-CoV-2 em indivíduos sintomáticos que apresentam sintomas por ≤ 10 dias. Esses resultados reforçam a necessidade de ampliar o uso de amostras de saliva, que são auto-coletadas e não requerem swabs (09/08/2021). Fonte: Journal of Medical Microbiology
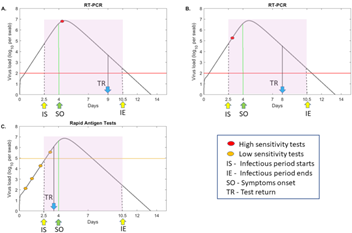
Recente estudo no campus universitário sugere que o teste rápido do antígeno SARS-CoV-2 pode ajudar a conter a disseminação na comunidade, detectando infecções assintomáticas. O estudo descobriu que o teste de antígeno - que é mais rápido e barato do que o teste de reação em cadeia da polimerase (PCR) padrão-ouro - é altamente sensível para detectar infecções por SARS-CoV-2 quando realizado pelo menos em intervalos de alguns dias. O teste de PCR nasal e saliva foi mais sensível do que o teste de antígeno com amostras nasais no início do curso da infecção. No entanto, a sensibilidade do teste de antígeno atingiu 98% quando realizado pelo menos a cada 3 dias, equiparando-se ao teste de PCR na mesma frequência. Os pesquisadores citam que o teste rápido de antígeno em casa, duas a três vezes por semana, é uma maneira vantajosa e conveniente para os indivíduos rastrearem a infecção por COVID-19 (10/08/2021). Fonte: Jama
07/08/2021 a 13/08/2021
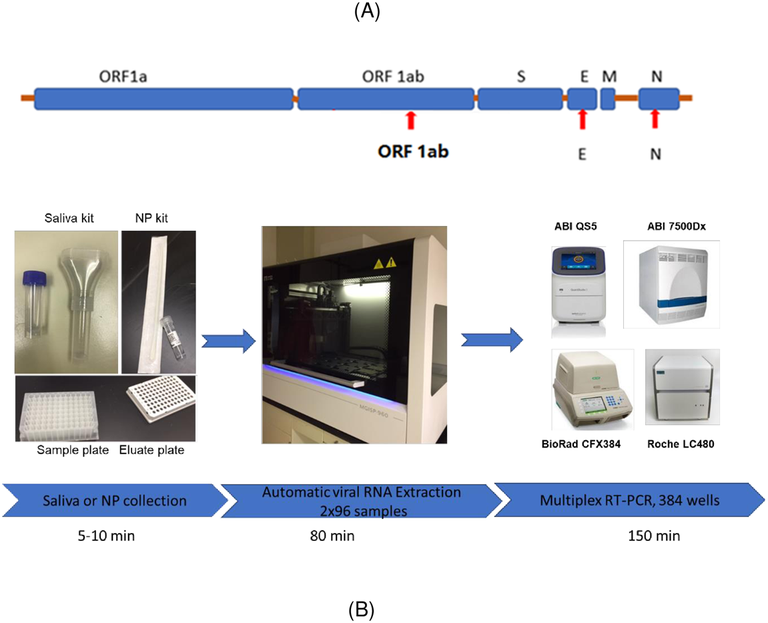
Estudo utilizou um total de 452 amostras duplas (saliva e NPS) de pacientes com suspeita de COVID-19 para comparar os resultados obtidos para as diferentes amostras ao usar RT-PCR de RNA extraído de NPS e saliva, bem como saliva diretamente sem extração de RNA. O SARS-CoV-2 não foi detectado em 13 amostras de saliva (direta) das 80 amostras positivas de NPS e em 16 amostras de saliva (RNA) de um total de 76 amostras positivas de NPS. A sensibilidade de detecção dos genes virais ORF1ab, E e N na saliva é afetada de forma diferente e a detecção desses genes em amostras de saliva apresenta grande variabilidade quando as amostras de NPS. Os pesquisadores citam que o uso de saliva como amostra deve ser cuidadosamente considerado devido à taxa de falsos negativos e o sistema usado para a detecção também pode ser muito relevante, uma vez que os diferentes genes virais são afetados de forma diferente em termos de sensibilidade de detecção usando saliva (17/07/2021). Fonte: Journal of Clinical Virology
31/07/2021 a 06/08/2021
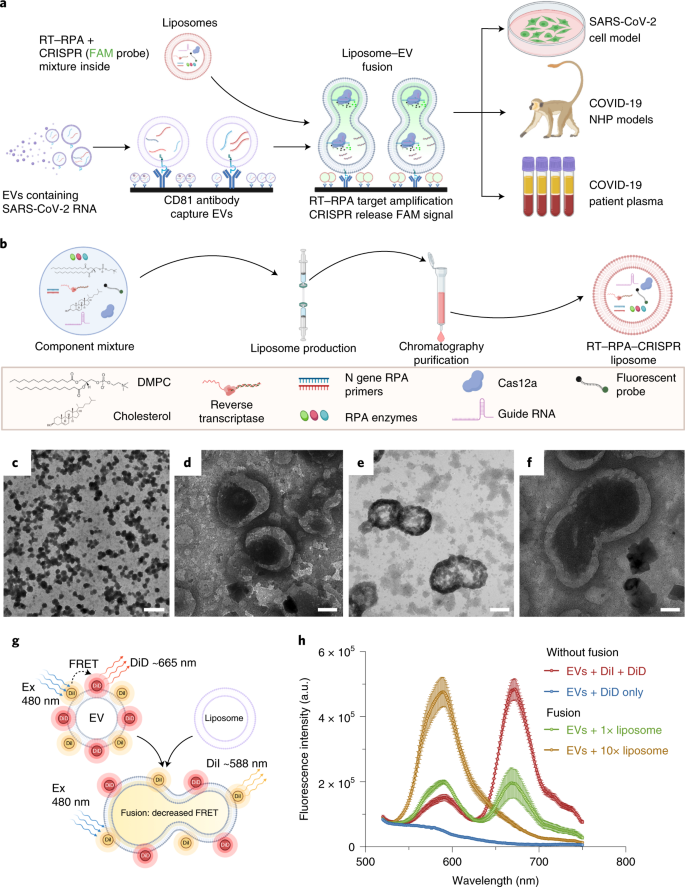
O RNA plasmático da SARS-CoV-2 pode representar uma alternativa diagnóstica viável aos níveis de RNA respiratório, que diminuem rapidamente após a infecção. Os ensaios de referência de PCR quantitativo com transcrição reversa (RT-qPCR) exibem baixo desempenho com plasma, provavelmente refletindo a diluição e degradação do RNA viral liberado na circulação, mas esses problemas podem ser resolvidos analisando o RNA viral empacotado em vesículas extracelulares. Aqui descreve-se uma abordagem de ensaio em que vesículas extracelulares capturadas diretamente do plasma são fundidas com lipossomas carregados com reagente para amplificar e detectar sensivelmente um alvo do gene SARS-CoV-2. Esta abordagem identificou com precisão os pacientes com COVID-19, incluindo casos desafiadores perdidos por RT-qPCR. Vesículas extracelulares positivas para SARS-CoV-2 foram detectadas no dia 1 após a infecção e estabilizaram do dia 6 ao dia 28 em um modelo de primata não humano, enquanto durações de sinal por 20-60 dias foram observadas em crianças pequenas. Esta abordagem nanotecnológica usa uma amostra não infecciosa e estende as janelas de detecção de vírus, oferecendo uma ferramenta para apoiar o diagnóstico COVID-19 em pacientes sem RNA do SARS-CoV-2 detectável no trato respiratório (22/07/2021) Fonte: Nature nanotechnology
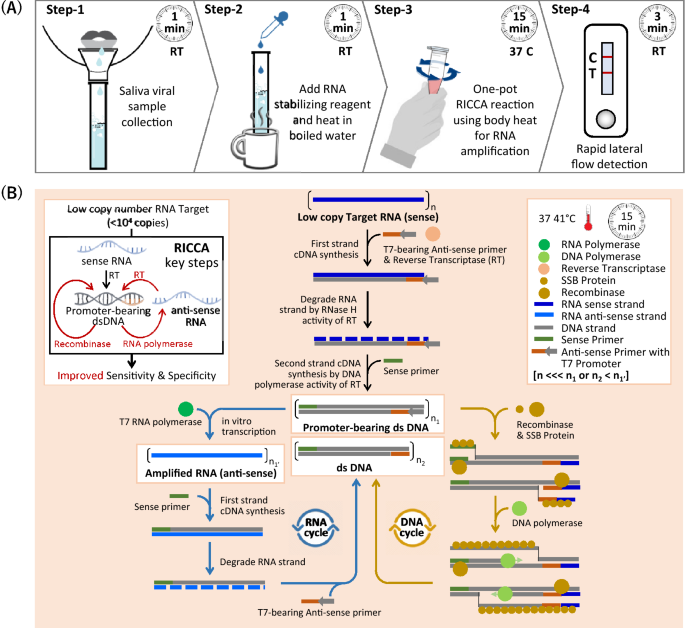
Pesquisadores citam que testes simples de infecciosidade que retornam resultados em minutos e diretamente de amostras, mesmo com baixas cargas virais, podem ser uma virada de jogo em potencial na luta contra o COVID-19. Estudo descreve um ensaio de amplificação de ácido nucleico isotérmico melhorado, denominado reação RICCA (RNA Isotérmico Co-assistido e Amplificação Acoplada), que consiste em um formato de um único recipiente simples de "amostra dentro e fora do resultado" com um foco principal na detecção de baixo número de cópias de vírus de RNA diretamente da saliva sem a necessidade de processamento laboratorial(06/08/2021). Fonte: Nature
24/07 a 30/07/2021
Pesquisadores investigaram a sensibilidade analítica de nove Ag-RDTs disponíveis comercialmente usando SARS-CoV-2 em cultura, comparando a linhagem B.1.610 (primeira onda pandêmica de COVID-19 na Europa) com VOCs B.1.1.7, B.1.351 e P. 1 e VOI P.2. Os pesquisadores concluem que, embora o teste de sensibilidade analítica com vírus em cultura não possa substituir totalmente os dados clínicos, os dados deste estudo fornecem resultados tranquilizadores para o uso de Ag-RDTs para diagnosticar VOCs (29/06/2021). Fonte: The Lancet Microbe
17/07 a 23/07/2021
A amplificação do ácido nucléico serve como método padrão ouro para a confirmação da infecção por COVID-19. No entanto, os desafios enfrentados pelos laboratórios de diagnóstico de países subdesenvolvidos incluem a falta de kits e suprimentos para purificar o RNA viral. Portanto, é urgente validar métodos alternativos de isolamento de ácido nucleico para SARS-CoV-2. Os resultados deste estudo demonstram que um tampão de amplificação de lise viral concentrado (vLAB) preparado com o detergente não iônico IGEPAL permite a detecção qualitativa de SARS-CoV-2 por dRT-PCR. Além disso, o vLAB foi eficaz na inativação do SARS-CoV-2. Uma vez que este método é barato e nenhum equipamento de purificação de RNA ou síntese adicional de cDNA é necessário, este dRT-PCR com vLAB deve ser considerado como um método alternativo para a detecção qualitativa de SARS-CoV-2 (09/07/2021). Fonte: Scientific Reports (Nature)
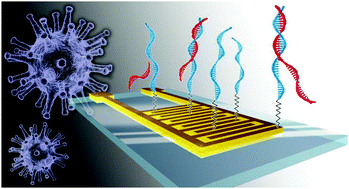
Pesquisadores brasileiros desenvolveram genessensores que permitem a detecção rápida e barata do SARS-CoV-2. Os genossensores desenvolvidos são capazes de detectar uma sequência de ssDNA do genoma SARS-CoV-2, que imita o gene GU280 gp10 (codificando a fosfoproteína do nucleocapsídeo viral), usando quatro princípios distintos de detecção e tratamento dos dados com visualização de informações e técnicas de aprendizado de máquina. Em condições apropriadas, a fita simples imobilizada liga-se a outra fita simples e complementar de DNA eventualmente contida na amostra líquida a ser analisada. Esse processo, chamado de hibridização, denuncia a presença do SARS-CoV-2 na amostra, que pode ser constituída por saliva ou outros fluidos corporais. A detecção foi realizada por espectroscopias de impedância elétrica e eletroquímica e ressonância de plasma de superfície localizada (LSPR). A maior sensibilidade foi alcançada com espectroscopia de impedância, incluindo o uso de um analisador de impedância caseiro de baixo custo (US$ 100). Os pesquisadores concluem que os genossensores propostos aqui são promissores para detectar material genético (RNA) de SARS-CoV-2 em fluidos biológicos em ambientes de ponto de atendimento (24/06/2021). Fonte: Materials Chemistry Frontiers
10/07 a 16/07/2021
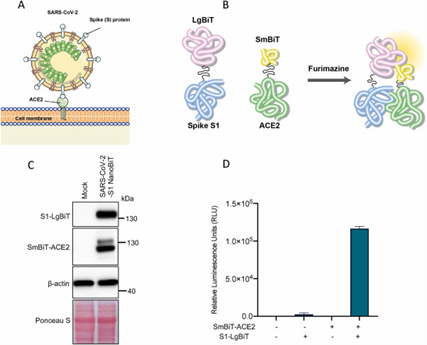
Pesquisadores da Universidade Federal de São Carlos (UFSCar) desenvolveram uma nova estratégia para detectar em amostras biológicas anticorpos contra o patógeno causador da COVID-19, ao combinar uma enzima encontrada em vagalumes com uma proteína capaz de se ligar ao novo coronavírus. A enzima usada na pesquisa pertence à classe das luciferases e o grupo utilizou aquela produzida pelo vagalume Amydetes vivianii, que gera a bioluminescência mais brilhante e estável. A luciferase foi acoplada, por engenharia genética, a uma proteína capaz de se ligar aos anticorpos. Desta forma, se os anticorpos contra SARS-CoV-2 estiverem presentes na amostra, a ligação ocorrerá e isso poderá ser detectado por meio da emissão de luz. O próximo passo, agora, é saber se a quantidade de anticorpos presentes na saliva ou esfregaço nasal é suficiente para desencadear a bioluminescência, de modo que o novo biossensor possa ser utilizado em testagem rápida e não invasiva para COVID-19. O grupo já depositou um pedido de patente para o novo sistema bioluminescente no Instituto Nacional da Propriedade Industrial (INPI). Segundo os pesquisadores, o estudo é tão recente que o artigo que o descreve ainda está em fase de redação (14/07/2021). Fonte: Agência FAPESP
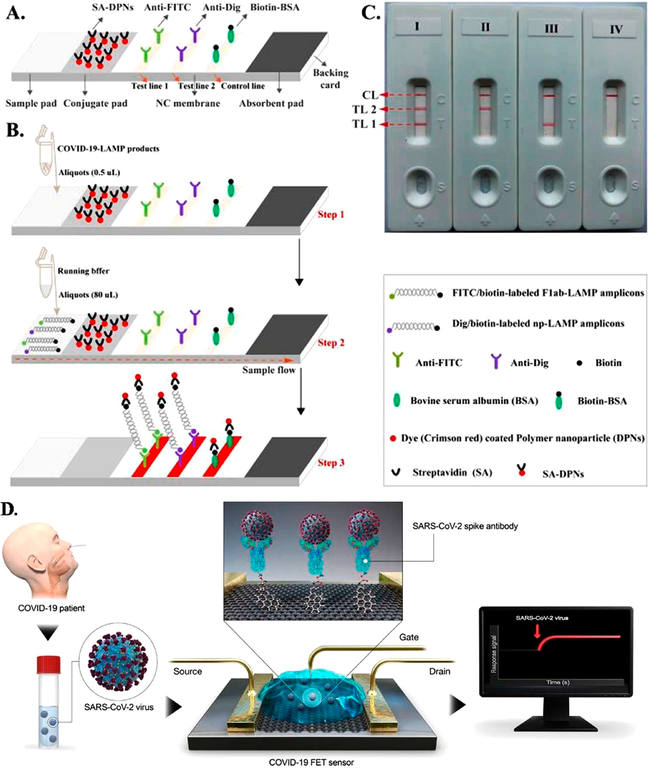
Cientistas do Instituto de Bioquímica Médica (IBqM/UFRJ) e do campus Duque de Caxias da UFRJ criaram um kit que diagnostica a presença de coronavírus a partir de amostras de saliva e de secreção nasal. O resultado é obtido em menos de uma hora e ao custo de apenas R$ 30,00 é possível concluir se o Sars-CoV-2 está no organismo. Exames realizados em 60 pacientes revelaram que a invenção é 100% eficaz quando comparada ao tradicional PCR. O Lamp-COVID-19, como o teste desenvolvido é chamado, amplifica o genoma viral em menos de meia hora e consegue encontrar até dez cópias do vírus considerando uma única amostra. O exame pode ser realizado em lugares com pouca infraestrutura e o resultado é conferido de forma colorimétrica (15/07/2021). Fonte: UFRJ
02/07 a 09/07/2021
Pesquisadores desensenvolveram um kit de diagnóstico para detecção do novo coronavírus, que pode ser aplicado diretamente em unidades básicas de saúde, fornecendo o resultado em até 45 minutos, com baixo custo e alta precisão. A inovação, que pode contribuir para o enfrentamento da COVID-19, teve a patente depositada, após mais de um ano de trabalho de pesquisadores do Instituto Oswaldo Cruz (IOC/Fiocruz), Universidade Federal de Santa Catarina (UFSC) e Instituto Federal de Santa Catarina (IFSC), em parceria com a empresa SPK Solutions(08/07/2021). Fonte: Fiocruz

O Laboratório de Genética Celular e Molecular do Instituto de Ciências Biológicas (ICB) da UFMG iniciou os testes do método de detecção da COVID-19 que utiliza amostras salivares. Os exames estão sendo feitos em vários estados do país por laboratórios que integram o Projeto institucional em rede: laboratórios de campanha para testes de diagnóstico da COVID-19. Menos invasivo e mais rápido (sai em dois minutos) que o RT-PCR, o teste salivar utiliza raios infravermelhos que incidem sobre as amostras. Posteriormente, elas são analisadas por inteligência artificial. Os resultados por saliva e por swab são equivalentes, o que prova que o método de testagem salivar é tão eficiente quanto o RT-PCR, recomendado pela Organização Mundial de Sapude (OMS) (06/07/2021). Fonte: UFMG

26/06 a 02/07//2021
O objetivo foi desenvolver um fluxo de trabalho direto RT-LAMP para detecção viral na saliva e fornecer mais informações sobre seu potencial no diagnóstico COVID-19. O fluxo de trabalho planejado atingiu 93,2% de sensibilidade, 97% de especificidade e 0,895 Kappa para salivas contendo> 102 cópias/μL. Análises posteriores na saliva mostraram pico de carga viral nos primeiros dias dos sintomas e cargas virais mais baixas em mulheres, particularmente entre indivíduos jovens. Este novo fluxo de trabalho de RT-LAMP de saliva pode ser aplicado a testes de ponto de atendimento. Este trabalho reforça que a saliva se correlaciona melhor com a dinâmica de transmissão do que os espécimes NOP, e revela diferenças de gênero que podem refletir uma transmissão mais elevada pelo sexo masculino. Para maximizar a detecção, o teste deve ser feito imediatamente após o início dos sintomas, especialmente em mulheres(09/06/2021). Fonte: MedRxiv
Máscara facial foi criada para detectar se o usuário está contaminado pelo SARS-CoV-2 em cerca de 90 minutos. A parte interna da máscara de papel é revestida por biossensores capazes de detectar partículas virais por meio do hálito e da respiração. Inicialmente, esses biossensores estão liofilizados, ou seja, desidratados por uma técnica que conserva o material estável por um longo período de tempo. Quando o usuário aciona o botão para realizar o teste, uma pequena quantidade de água é liberada, hidratando e reativando o material, que torna-se capaz de detectar a presença do Sars-Cov-2. O teste de alta precisão e baixo custo pode ser adaptado para indicar variantes ou outros patógenos, como bactérias e toxinas, conforme os pesquisadores (28/06/2021). Fonte: Nature biotechnology.
21 a 25/06/2021
Exame de saliva desenvolvido na USP é capaz de apontar uma diferença de carga viral não detectada nos testes feitos com amostras tiradas do nariz e faringe. Testes feitos em pacientes com COVID-19 sugerem que os homens têm uma maior carga de vírus na saliva do que mulheres, algo que não aparece nos swabs de nasofaringe. Segundo os pesquisadores, essa diferença precisa ser confirmada por novos estudos, envolvendo um maior número de casos e em outros contextos. O resultado foi obtido em um estudo preliminar coordenado pelo Centro de Pesquisa sobre Genoma Humano e Células-Tronco (CEGH-CEL), do Instituto de Biociências (IB) da USP. Os pesquisadores desenvolveram um teste rápido para detecção do coronavírus, que pode ser feito em locais com pouca infraestrutura, com menos custos (11/06/2021). Fonte: Jornal USP e medRxiv
Pesquisadores de uma empresa e da Universidade Estadual de Maringá (UEM), no norte do Paraná, criaram um programa capaz de fazer a leitura da língua de pacientes para verificar a presença do novo coronavírus. O exame é feito por meio de um aparelho portátil. O equipamento consegue fazer uma análise molecular da saliva humana e indicar a presença do novo coronavírus em três segundos. Segundo os desenvolvedores, a tecnologia aguarda aval da Agência Nacional de Vigilância Sanitária (Anvisa) para o uso em larga escala. O software foi testado com 970 pessoas. Segundo os estudos, o programa tem 84% de eficácia entre os casos positivos e de 91% entre casos negativos. Apesar de ser mais rápido e menos invasivo, o teste ainda é menos eficaz que o exame do tipo RT-PCR. Os estudos continuam, e a expectativa da empresa e da UEM é de que o software também possa ser usado para o diagnóstico de outras doenças, no futuro (18/06/2021). Fonte: G1
14 a 18/06/2021
Tecnologia desenvolvida por pesquisadores da Unicamp usa inteligência artificial na realização de diagnósticos em nível molecular. A técnica de análise de espectrometria de massa por inteligência artificial foi licenciada, com o apoio da Inova Unicamp, para o Lacen (Laboratório Central de Saúde Pública) em uso exclusivo para testes de COVID-19. A detecção é feita a partir de uma amostra de sangue do paciente, na qual é gerado uma assinatura numérica que mostra alterações causadas pelo coronavírus (11/06/2021). Fonte: Unicamp
O objetivo do estudo foi avaliar a verdadeira positividade em pessoas, cujos resultados do teste inicial de swabs nasofaríngeos (NPS) mostraram uma carga viral muito baixa de coronavírus SARS-CoV-2. Setenta e sete pessoas detectadas com baixas cargas virais de SARs-CoV-2 em amostras de nasofaringe (Ct ≥ 35) foram incluídas no estudo. Para tanto, um segundo NPS foi coletado para rRT-PCR (reação em cadeia da polimerase de transcrição reversa em tempo real) combinado com um par de amostras de soro para detecção de anticorpos anti-nucleocapsídeo (anti-N) e anti-spike (anti-S). Em 8 pessoas, os exames subsequentes indicaram um aumento das cargas virais, a partir daí, seguido por um aumento dos anticorpos anti-N e anti-S, achados compatíveis com um estágio inicial da infecção por COVID-19. Em 9 pessoas, que já tinham anticorpos anti-N aumentados, o exame subsequente mostrou uma diminuição ou ausência da carga viral e um aumento dos anticorpos, indicativo de um estágio tardio da infecção por COVID-19. Em 60 pessoas, o exame subsequente mostrou ausência de infecção (conforme indicado pela ausência de carga viral e anticorpos). Os pesquisadores propuseram uma combinação de um segundo NPS e uma amostra de soro, ambos colhidos três dias após o primeiro NPS, ajuda significativamente a evitar resultados falso-positivos (10/06/2021). Fonte: Microorganisms
02 a 09/06/2021
RT-PCR digital da gota (RT-ddPCR) oferece uma plataforma atraente para a quantificação do RNA do SARS-CoV-2. Os pesquisadores avaliaram oito conjuntos de primer/sonda originalmente desenvolvidos para testes de diagnóstico SARS-CoV-2 baseados em RT-PCR em tempo real para uso em RT-ddPCR e identificaram três (Charité-Berlin, E-Sarbeco e Pasteur Institute IP2 e IP4) como o mais eficiente, preciso e sensível para a quantificação de RNA SARS-CoV-2 baseada em RT-ddPCR (29/05/2021). Fonte: The Journal of Molecular Diagnostics
A avaliação da imunidade humoral ao SARS-CoV-2 e outros agentes infecciosos é normalmente restrita à detecção de anticorpos específicos para o antígeno no soro. Pesquisadores testaram a hipótese de que a eficiência do revestimento do antígeno pode ser universalmente melhorada em um conjunto diversificado de antígenos virais se a absorção do antígeno direto padrão (não específico, baixa afinidade) para a membrana fosse substituída pela captura de alta afinidade. Especificamente, relataram um aumento na sensibilidade do ensaio e uma redução nas concentrações de proteínas necessárias por meio da captura de proteínas recombinantes por meio de sua etiqueta de afinidade hexahistidina (6XHis) codificada. O revestimento de antígeno de etiqueta de afinidade permitiu a detecção de células secretoras de anticorpos individuais reativo ao domínio de ligação do receptor spike (RBD) de SARS-CoV-2 e também melhorou significativamente o desempenho do ensaio usando antígenos de controle adicionais. Coletivamente, o estabelecimento de uma abordagem de revestimento de antígeno universal agiliza a caracterização do compartimento de células B de memória após a infecção com SARS-CoV-2 ou vacinações com COVID-19 e facilita os esforços de monitoramento imunológico de alto rendimento de grandes coortes de doadores em geral (03/06/2021). Fonte: medRxiv
31/05/2021
Estudo avalia o perfil de proteína através da técnica de MALDI-ToF como plataforma de diagnóstico rápido potencial para COVID-19. Considerando as limitações e a alta demanda dos testes COVID-19, autores empregaram a espectrometria de massa MALDI-ToF para a análise de 60 amostras de gargarejo de doadores humanos e compararam os espectros com seus respectivos resultados de RT-PCR. Vários padrões, incluindo imunoglobulinas isoladas de soro humano e controles, como saliva pré-COVID-19 e vírus SARS-CoV-2 inativado por calor, foram analisados simultaneamente para fornecer uma visão relativa da saliva e do proteoma viral. Foram estabelecidos cinco picos de biomarcadores potenciais que demonstraram alta consistência com amostras positivas de PCR. No geral, a concordância desses resultados com o teste de RT-PCR não foi inferior a 90% para a coorte estudada, que consistia em estudantes atletas jovens e em grande parte assintomáticos (30/05/2021). Fonte: medRxiv
28/05/2021
Pesquisadores apresentam a expressão recombinante de um domínio de ligação ao receptor estendido (RBD) da proteína spike do SARS-CoV-2 usada como antígeno de captura em um imunoensaio rápido exclusivo para detectar a presença de anticorpos de ligação a RBD com alta sensibilidade e especificidade. Os pesquisadores também sugerem que como as vacinas disponíveis se concentram no RBD Spike, o teste desenvolvido também poderia ser usado para monitorar uma resposta imune bem-sucedida após a vacinação com uma vacina baseada em RBD (05/05/2021). Fonte: CHIMIA
26/05/2021
Nove especialistas de países latino-americanos, incluindo 1 brasileiro, desenvolveram um algoritmo simplificado para o diagnóstico de COVID-19, usando um método Delphi modificado. Vinte e quatro questões relacionadas às configurações de diagnóstico foram propostas, seguidas de uma discussão da literatura e da experiência de especialistas. O algoritmo considera três intervalos de tempo (≤7 dias, 8-13 dias e ≥ 14 dias) e discute as opções de diagnóstico para cada um. O rRT-PCR para SARS-CoV-2 é o teste de escolha do dia 1 ao dia 14 após o início dos sintomas ou contato próximo, embora o teste de antígeno possa ser usado em situações particulares, do 5º ao 7º dia. Ensaios de anticorpos podem ser usados para confirmação, principalmente após o dia 14. Se a suspeita clínica for muito alta, mas os outros testes forem negativos, esses ensaios podem ser usados como um complemento para a tomada de decisão do dia 8 ao dia 13 (07/05/2021). Fonte: IJID
21/05/2021
Pesquisadores examinaram o uso de amostras de DBS e plasma de sangue capilar (punção digital) coletados em tubos Microtainer para teste de SARS-CoV-2 com os ensaios automatizados Abbott ARCHITECT ™ SARS-CoV-2 IgG e IgM e uso de sangue total venoso com um protótipo PANBIO ™ ensaio rápido de fluxo lateral SARS-CoV-2 IgG. O ensaio ARCHITECT ™ SARS-CoV-2 IgG foi inicialmente otimizado para uso com DBS, plasma venoso, capilar e sangue total venoso coletado de pacientes com sintomas e COVID-19 confirmado por PCR e controles assintomáticos negativos. A linearidade e a reprodutibilidade foram confirmadas com 3 amostras de DBS planejadas, juntamente com a estabilidade da amostra e a recuperação do sinal após 14 dias. Os resultados do ensaio ARCHITECT ™ SARS-CoV-2 IgG e IgM mostraram alta concordância entre amostras de DBS de punção digital e DBS venosa e entre amostras de DBS de punção digital e sangue total venoso (n = 61). Plasma de ponta de dedo coletado em tubos Microtainer (n = 109) mostrou resultados 100% concordantes com plasma venoso de paciente compatível no ensaio ARCHITECT ™ SARS-CoV-2 IgG. Alta concordância dos resultados do ensaio (92,9% positivo, 100% negativo) também foi observada para o ensaio PANBIO ™ SARS-CoV-2 IgG em comparação com o ensaio ARCHITECT ™ SARS-CoV-2 IgG executado com plasma venoso correspondente (n = 61) . As amostras de DBS e plasma com punção digital são fáceis e baratas de coletar e, junto com o uso de plataformas de teste rápido de ponto de atendimento, irão expandir o acesso ao teste de sorologia SARS-CoV-2, particularmente em áreas com recursos limitados (11/05/2021). Fonte: Journal of Clinical Virology
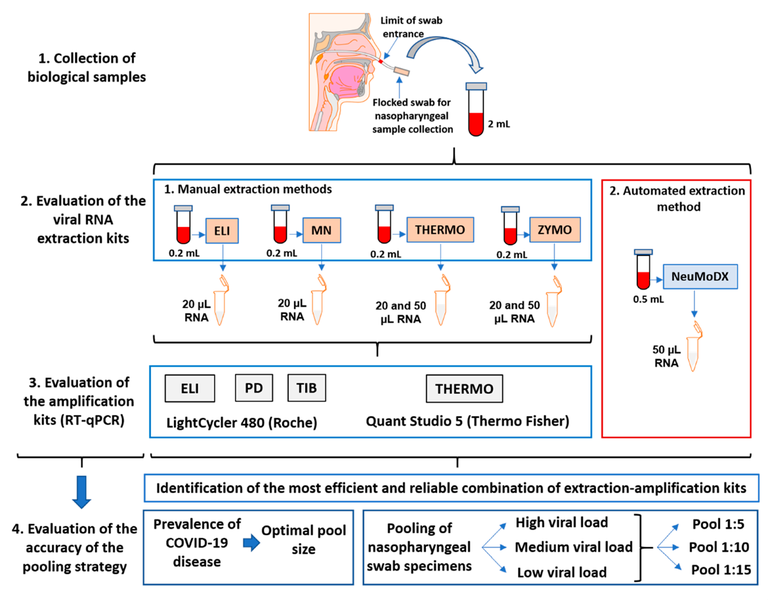
Pesquisadores investigaram a eficiência e a confiabilidade de uma abordagem de agrupamento hierárquico para testes de PCR em grande escala para o diagnóstico de SARS-CoV-2. Para identificar as melhores condições para a abordagem de pooling para diagnóstico de SARS-CoV-2 por RT-qPCR, foram investigados quatro métodos manuais para extração de RNA e avaliação de PCR visando um ou mais dos genes RdRp, N, S e ORF1a, usando dois dispositivos de PCR e um fluxo automatizado para detecção de SARS-CoV-2. O cálculo do tamanho ideal do pool incluiu a prevalência de SARS-CoV-2, a sensibilidade do ensaio de 95%, uma especificidade do ensaio de 100% e uma gama de tamanhos de pool de 5 a 15 amostras. Essa investigação revelou que o procedimento mais eficiente e preciso para detectar o SARS-CoV-2 tem um limite de detecção de 2,5 cópias/reação de PCR. Esta abordagem de agrupamento provou ser eficiente e precisa na detecção de SARS-CoV-2 para todas as amostras com valores de ciclo de quantificação individual (Cq) inferiores a 35, representando mais de 94% de todas as amostras positivas. Os dados podem servir como um guia prático abrangente para os centros de diagnóstico SARS-CoV-2 que planejam abordar essa estratégia de pooling (13/05/2021). Fonte: Viruses
19/05/2021
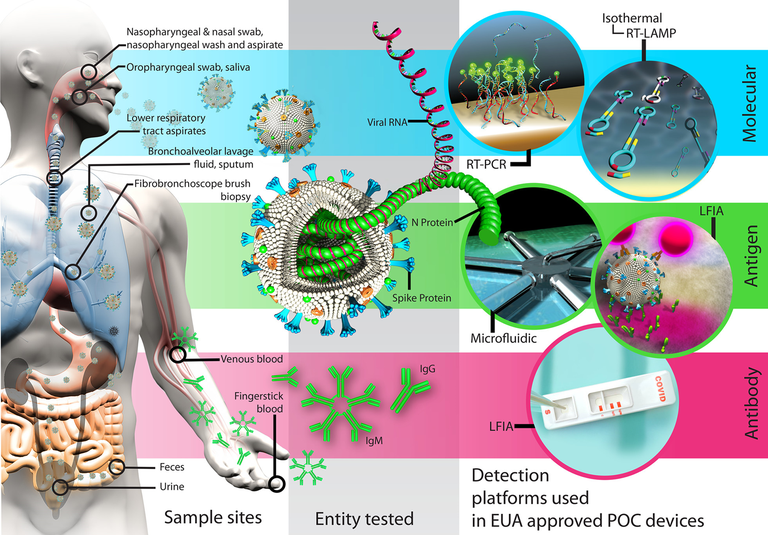
As tecnologias de “point-of-care” (POC) que permitem o diagnóstico descentralizado, rápido, sensível e de baixo custo da infecção por COVID-19 são urgentemente necessárias em todo o mundo. Com muitas tecnologias aprovadas para comercialização nos últimos 10 meses, o campo de diagnósticos POC para COVID-19 está evoluindo rapidamente. Nesta perspectiva, o estudo analizou o estado atual das tecnologias POC para o diagnóstico e monitoramento da infecção por COVID-19 e discute os desafios futuros no diagnóstico de COVID-19. À medida que a pandemia COVID-19 se torna endêmica, os avanços obtidos durante o ano passado provavelmente também serão utilizados para previsões futuras de surtos e pandemias emergentes(13/05/2021). Fonte: ACS Nano
Artigo apresenta um teste de diagnóstico baseado no sequenciamento de células T de memória específica para SARS-CoV-2 de longa duração, que pode fornecer um complemento ao teste de anticorpos para determinar a exposição anterior ao SARS-CoV-2. O teste T-Detect COVID-19 recebeu autorização de uso de emergência da Food and Drug Administration (FDA) no mês passado. O teste adaptativo envolve o sequenciamento de última geração para identificar as células T que reconhecem os antígenos SARS-CoV-2. O teste não se destina ao diagnóstico de infecção ativa, mas é um complemento aos testes de anticorpos usados para confirmar infecções recentes ou anteriores. O procedimento baseado em laboratório, que tem um tempo de resposta de sete a dez dias, agora está autorizado para uso em amostras coletadas de indivíduos pelo menos 15 dias após o início dos sintomas. Em um estudo de validação clínica, o ensaio T-Detect COVID atingiu 97,1% de sensibilidade (definida como concordância percentual positiva) e 100% de especificidade (definida como concordância percentual negativa) em comparação com o teste de PCR de 15 dias ou mais após o diagnóstico. (12/05/2021). Fonte: Nature Biotechnology
14/05/2021
Estudo observacional em um National Health de 185 leitos com duas estratégias de teste consecutivos: teste de casos sintomáticos apenas, seguido por testes semanais em toda a instalação de funcionários e residentes, independentemente dos sintomas. O teste nasofaríngeo e orofaríngeo com RT-PCR para SARS-CoV-2, incluindo sequenciamento de amostras positivas, foi realizado com avaliação de sintomas padronizados. No total 91,1% dos funcionários positivos para SARS-CoV-2 eram sintomáticos, sem diferença entre as duas estratégias de teste. A perda de olfato e paladar, dor de garganta, dor de cabeça ou mialgia dificilmente foram relatados em residentes em comparação com toda a equipe (07/05/2021). Fonte: Age and Ageing
Em função dos testes rápidos de antígeno geralmente apresentarem desempenhos mais baixos do que o esperado, seu uso para triagem na linha de frente a ainda é controverso. Apesar da falta de dados do uso clínico diário, os ensaios microfluídicos de terceira geração (como o teste LumiraDx SARS-CoV-2 Ag) foram recentemente sugeridos por terem desempenhos semelhantes aos do RT-qPCR e foram propostos como ferramentas alternativas de diagnóstico. Ao analisar 960 swabs nasofaríngeos de 960 indivíduos nas admissões do departamento de emergência de um hospital de COVID-19 terciário, o ensaio LumiraDx demonstrou uma especificidade de 97% e uma sensibilidade de 85% em comparação com RT-qPCR, que aumenta para 91% para amostras com um limite de ciclo ≤ 29. Cinquenta resultados LumiraDx falso-negativos foram confirmados por quantificação direta de RNA genômico SARS-CoV-2 por meio de PCR digital de gota, respectivamente, indicando a presença de replicação viral ativa. No geral, o teste LumiraDx cumpre os requisitos mínimos de desempenho da OMS. No entanto, o risco de um erro de reconhecimento de pacientes com COVID-19 ativo persiste e a necessidade de confirmação RT-qPCR não deve ser alterada (01/05/2021). Fonte: Viruses
10/05/2021
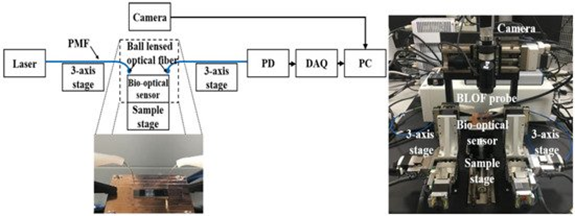
Estudo desenvolveu um sensor bio-óptico rápido que usa uma sonda de fibra óptica com lentes esféricas (BLOF) e uma plataforma de análise automática para diagnosticar com precisão patógenos infecciosos como o SARS-CoV-2. A sonda BLOF é fácil de alinhar e possui uma alta sensibilidade de detecção óptica (1,5 vezes) e uma grande faixa de detecção (1,2 vezes) para um sistema de detecção óptica automática. Os resultados do sistema revelaram a medição estável e automática do sinal óptico de DNA com 100% de precisão. Pesquisadores prevêem que este sensor baseado em sonda BLOF seria uma ferramenta prática para o diagnóstico rápido, simples e sensível de patógenos infecciosos emergentes (15/04/2021). Fonte: MDPI
Pesquisadores propõem um ensaio ELISA de alta sensibilidade para detecção de anticorpos IgG, A e M para a glicoproteína S de SARS-CoV-2 no soro e saliva, otimizando diferentes antígenos e etapas de amplificação, em indivíduos infectados por SARS‐CoV‐2 não hospitalizados. O uso de glicoproteína S trimérica, em vez de nucleocapsídeo, permitiu a detecção de respostas em indivíduos com baixas respostas de anticorpos. IgG1 e IgG3 predominam para ambos os antígenos, mas foi detectável mais IgG1 do que IgG3. Todos os antígenos foram eficazes para detectar respostas em pacientes hospitalizados. As respostas de anticorpos IgG, IgA e IgM anti-S foram prontamente detectáveis na saliva de uma minoria de indivíduos sintomáticos não hospitalizados e confirmados por RT‐PCR, e estes eram principalmente os indivíduos que tinham os níveis mais altos de anticorpos séricos anti-S. Portanto, a detecção de respostas de anticorpos na saliva e no soro pode contribuir para determinar a exposição ao vírus e compreender as respostas imunológicas após a infecção por SARS-CoV-2 (01/05/2021). Fonte: Immunology
07/05/2021
Estudo propôs elucidar as implicações das cópias de SARS-CoV2 em amostras simultâneas de swab nasofaríngeo (NPS), líquido bucal total (WMF) e gotículas respiratórias (RD) na patogênese / transmissão da doença. Dos resultados os pesquisadores concluiram que o WMF pode ser usado de forma confiável como um substituto para o diagnóstico e que o número elevado de cópias no NPS provavelmente implicam no início precoce da doença, enquanto no WMF e RD podem implicar doença mais grave e aumento da inflamação (30/04/2021). Fonte: Virus Research
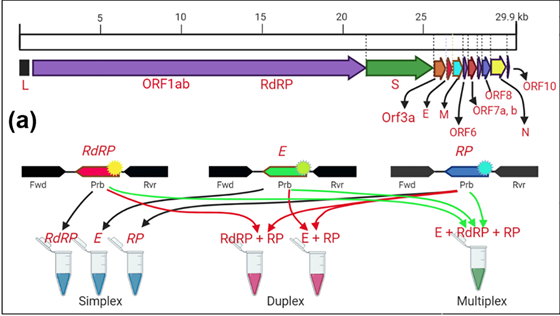
O RT-PCR é a técnica mais utilizada na detecção do SARS-CoV-2, no entanto, possíveis resultados falso-negativos e falso-positivos, tornam necessário o aprimoramento dos métodos existentes. Neste estudo, pesquisadores desenvolveram um método de diagnóstico multiplex rRT-PCR, que tem como alvo dois genes virais (RdRP e E) e um gene humano (RP) simultaneamente. A reação foi testada usando RNA pseudoviral e sequências de mRNA alvo humano como modelo. Além disso, o protocolo foi validado usando 14 amostras clínicas positivas para SARS-CoV-2. Os resultados estão de acordo com o sistema de diagnóstico Xpert® Xpress SARS-CoV-2 da Cepheid autorizado pelo CDC (100%). Ao contrário das estratégias de direcionamento de gene único, o método atual fornece a amplificação de duas regiões virais na mesma reação de PCR. Portanto, graças a essa estratégia, um método rRT-PCR rápido, confiável e fácil de usar é obtido para diagnosticar o SARS-CoV-2 (29/04/2021). Fonte: PLOS ONE
Artigo apresenta dados sobre o desempenho de dispositivos de fluxo lateral (LFDs) para testar cerca de 8.000 alunos na Universidade de Birmingham entre 2 de dezembro e 9 de dezembro de 2020. O desempenho foi validado contra quase 800 amostras usando PCR realizado no laboratório de testes da Universidade e teoricamente validado em milhares de resultados de testes de PCR realizados em amostras de testes domiciliares de baixa prevalência. Os dados mostram que os LFDs não detectam infecções que apresentam valores de PCR Ct acima de 29 a 30, conforme determinado usando o ensaio Thermo Fisher TaqPath. Isso pode ser de particular importância na detecção de indivíduos que estão nos estágios iniciais ou tardios da infecção e reforça a necessidade de testes recorrentes e frequentes (29/04/2021) Pre proof. Fonte: PLOS Biology
05/05/2021
O artigo apresenta um teste simples, de uma etapa e rápido para detectar anticorpos contra a proteína do nucleocapsídeo SARS-CoV2 N (scN) por meio da visualização direta da reação antígeno-anticorpo. Um total de 40 amostras de soro de pacientes com SARS-CoV2 foram adquiridas da RayBiotech. Um total de 50 amostras de soro humano pré-pandêmico do San Diego Blood Bank foram usadas como controles negativos. Os autores sugerem baseados nos resultados que seu teste é mais sensível do que o imunoensaio de fluxo lateral (LFIA), o teste rápido de anticorpos mais amplamente usado. Afirmam também que o teste de uma etapa tem uma excelente especificidade (27/04/2021). Fonte: Biochemistry, Biophysics and Molecular Biology
Pesquisadores demonstraram o uso do método de identificação rápida de par de afinidade via seleção dirigida (RAPIDS) para descobrir múltiplos pares de afinidade para a proteína do nucleocapsídeo SARS-CoV-2 (proteína N), um biomarcador de COVID-19, a partir de bibliotecas in vitro em 10 semanas. O par com a maior sensibilidade do biomarcador foi integrado em um teste de papel de celulose de fluxo vertical de 10 minutos. O teste atingiu os limites de detecção de 40 pM e 80 pM em 1 × PBS (esfregaço simulado) e matrizes de saliva enriquecidas com vírus SARS-CoV-2 gerados por cultura de células e também é capaz de detectar a proteína N a partir de amostras de esfregaço clínico caracterizadas. Assim, este trabalho abre caminho para a produção em massa de ensaios à base de papel de celulose que podem suprir a escassez enfrentada devido à dependência da nitrocelulose e das técnicas de fabricação atuais. Além disso, os resultados aqui relatados indicam a promessa de RAPIDS e proteínas ligantes projetadas para o desenvolvimento oportuno e flexível de testes de diagnóstico clinicamente relevantes em resposta a doenças infecciosas emergentes (19/04/2021). Fonte: ChemRxiv
03/05/2021
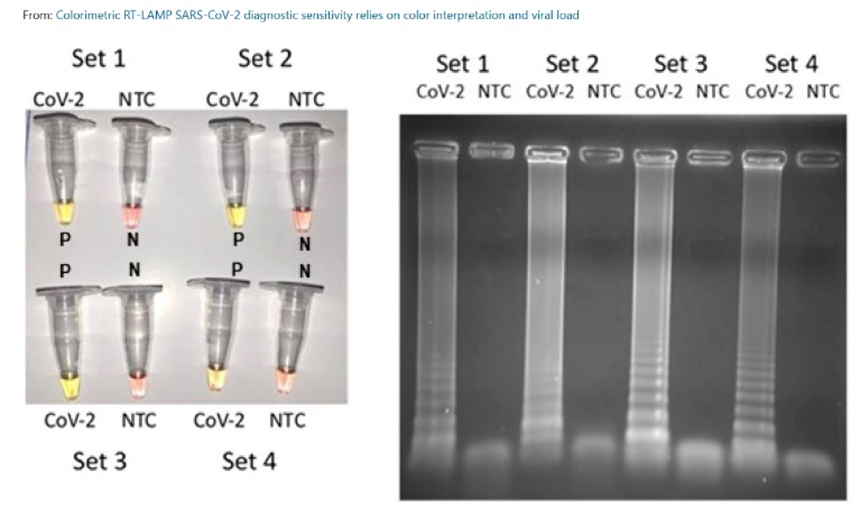
Pesquisadores demonstram que a reação RT-LAMP tem uma sensibilidade de apenas 200 cópias de vírus de RNA, com uma mudança de cor de rosa para amarelo ocorrendo em 100% das 62 amostras clínicas testadas positivas por RT-qPCR. Também demonstraram que esta reação é 100% específica para SARS-CoV-2 após testar 57 amostras clínicas infectadas com dezenas de vírus respiratórios diferentes e 74 indivíduos sem qualquer infecção viral. Esta técnica descreve apenas a presença de estados de duas cores (rosa = negativo e amarelo = positivo), porém esta pesquisa identificou que há um grupo de terceira cor evidente (laranja), em geral relacionada a amostras positivas com baixa carga viral, mas que não podem ser definidas como positivas ou negativas a olho nu. As cores laranja devem ser repetidas ou testadas pelo RT-qPCR para evitar um falso diagnóstico. RT-LAMP é, portanto, muito confiável, sendo tão sensível e específico quanto um teste RT-qPCR. Todas as reações foram realizadas em 30 min a 65° C. O uso de tempo de reação superior a 30 min também não é recomendado, uma vez que amplificações inespecíficas podem causar falsos positivos (27/04/2021). Fonte: Scientific Reports
30/04/2021
Artigo avaliou um ensaio CRISPR-Cas12 liofilizado para detecção de SARS-CoV-2 (kit Lyo-CRISPR SARS-CoV-2) com base na transcrição reversa, amplificação isotermal e reação CRISPR-Cas12. De um total de 210 amostras de RNA extraídas de cotonetes nasofaríngeos, o kit Lyo-CRISPR SARS-CoV-2 detectou 105/105 (100%) amostras positivas e 104/105 (99,05%) amostras negativas que foram testadas anteriormente utilizando RT-qPCR comercial. O índice kappa global estimado foi de 0,991, refletindo um nível de concordância quase perfeito entre os dois testes diagnósticos. Foi demonstrado, portanto, que o desempenho do kit Lyo-CRISPR SARS-CoV-2 foi semelhante ao do RT-qPCR comercial, sendo o primeiro altamente sensível e específico, além de proporcionar economia de tempo (1,5 h), ser mais barato, e não exigir equipamentos sofisticados (05/03/2021). Fonte: Viruses
28/04/2021
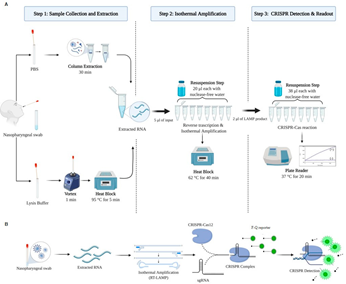
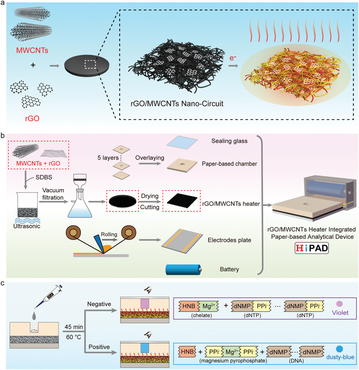
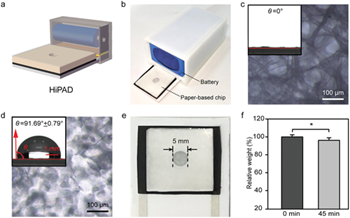
Pesquisadores desenvolveram o chamado HiPAD que é dispositivo analítico baseado em papel integrado com um aquecedor rGO/MWCNTs para detecção visual de SARS-CoV-2 por reação LAMP colorida. Para a detecção de SARS ‐ CoV ‐ 2 no HiPAD, a faixa de detecção foi de 25–2,5 × 1010 cópias mL− 1 com 25 cópias mL− 1 como limite de detecção em 45 min. O HiPAD compreende nanotubos de carbono de paredes múltiplas hibridizados com óxido de grafeno reduzido nano-circuito integrado em um aquecedor baseado em papel que é integrado em um dispositivo analítico baseado em papel (20/04/2021). Fonte: Advanced Funcyional Materials
Pesquisadores descrevem um ensaio nanofluídico quantitativo que supera algumas das deficiências do RT-qPCR, com base no instrumento BiomarkTM da Fluidigm. Este sistema oferece a possibilidade de analisar 192 amostras clínicas combinadas com 12 pares de primers, permitindo assim o monitoramento de SARS-CoV-2 incluindo a detecção de variantes específicas de SARS CoV-2, bem como a detecção de outros patógenos e / ou respostas celulares do hospedeiro (receptores de vírus, marcadores de resposta, micro RNAs). O volume da faixa de 10 nL das reações BiomarkTM é compatível com reações sensíveis e reproduzíveis que podem ser adaptadas de forma fácil e econômica a várias configurações RT-qPCR e conjuntos de primers / sonda. Os pesquisadores defendem que a utilização combinada de um buffer de processamento otimizado e um dispositivo de PCR em tempo real de alto rendimento contribuiria para melhorar o tempo de entrega dos resultados do teste aos pacientes e aumentar as capacidades de teste do SARS-CoV-2 (14/04/2021). Fonte: PLOS ONE
19/04/2021
Pesquisadores realizam uma validação prospectiva, em um único centro, de dois testes de diagnóstico rápido de detecção de antígeno (Ag-RDT), ambos atendendo aos critérios da OMS de ≥80% sensibilidade e ≥97% de especificidade, em comparação com RT-PCR em swab nasofaríngeo. Embora menos sensíveis do que RT-PCR, esses ensaios podem ser benéficos devido aos seus resultados rápidos, facilidade de uso e independência das estruturas laboratoriais existentes. Os critérios de teste com foco em pacientes com sintomas típicos no início do período sintomático precoce podem aumentar ainda mais o valor diagnóstico (31/03/2021). Fonte: PLOS ONE
16/04/2021
O estudo buscou avaliar o desempenho de 11 testes de anticorpos contra SARS-CoV-2 usando um conjunto de referência de amostras inativadas por calor de 278 pessoas não expostas e 258 pacientes com COVID-19, alguns dos quais contribuíram com amostras em série. O conjunto de referência incluiu amostras com uma variação nos títulos de anticorpos IgG contra SARS-CoV-2, conforme determinado por um ensaio de imunofluorescência interno (IFA). Os cinco testes de diagnóstico rápido avaliados tiveram uma especificidade de 99,0% e uma sensibilidade que variou de 56,3 a 81,6% e diminuiu com baixos títulos de IFA IgG. Dos resultados os testes de anticorpos avaliados mostraram uma heterogeneidade em seus desempenhos e apenas alguns testes tiveram bom desempenho com amostras com baixos títulos de IFA IgG, um aspecto importante para diagnósticos e investigações epidemiológicas (07/04/2021). Fonte: Scientific reports - Nature
07/04/2021
Estudo descreve o uso de uma solução desnaturante e inativadora de vírus (DS) para diminuir a infectividade do vírus em amostras clínicas sem afetar a integridade do RNA. Amostras de esfregaço foram coletadas de pacientes infectados e de pessoal de laboratório usando uma solução de transporte viral disponível comercialmente e o DS interno.As amostras foram testadas por RT-qPCR e a exposição a vírus infecciosos também foi acessada por ELISA. O DS usado não interferiu na detecção do genoma viral e foi capaz de manter a integridade do RNA por até 16 dias em temperatura ambiente. Os pesquisadores citaram que o DS fornece uma estratégia para manter a precisão do diagnóstico e proteger o pessoal do laboratório de diagnóstico de infecções acidentais (31/03/2021). Fonte: Brazilian Journal of Microbiology
05/04/2021
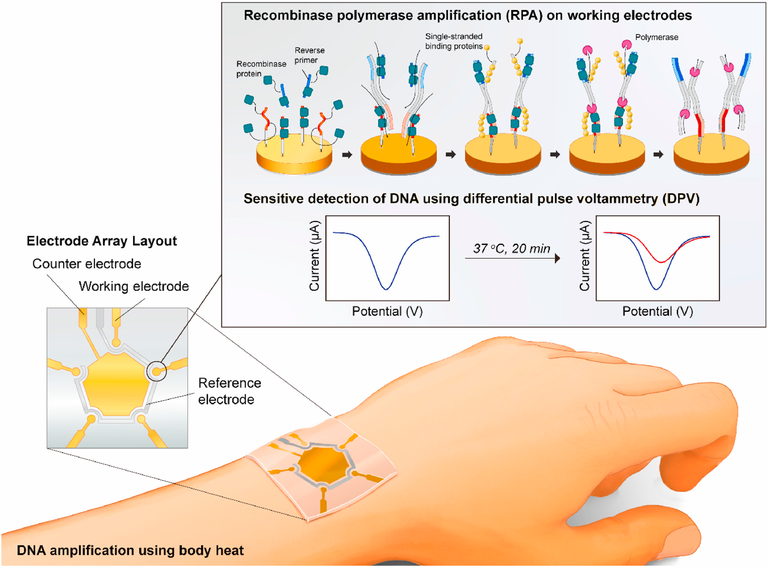
Estudo revela um biossensor eletroquímico combinado com amplificação da polimerase recombinase (RPA) para detecção rápida e sensível de SARS-CoV-2. O biossensor eletroquímico baseado em uma matriz de microeletrodos permite a detecção de múltiplos genes alvo por voltametria de pulso diferencial. O método de detecção eletroquímica acoplada a RPA proposto para a detecção do genoma SARS-CoV-2 permite a detecção de genes-alvo em menos de 20 minutos na temperatura do corpo humano. Para RPA on-chip, uma placa de PDMS com um orifício cilíndrico de 25 mm de diâmetro foi preparada para uma câmara de reação, e os eletrodos foram revestidos com primers modificados com tiol. O ensaio resulta em tempos de “amostra-resposta” mais curtos do que o PCR convencional e não necessita de um equipamento de ciclagem térmica (18/03/2021). Fonte: Biosensors and Bioeletronics
31/03/2021
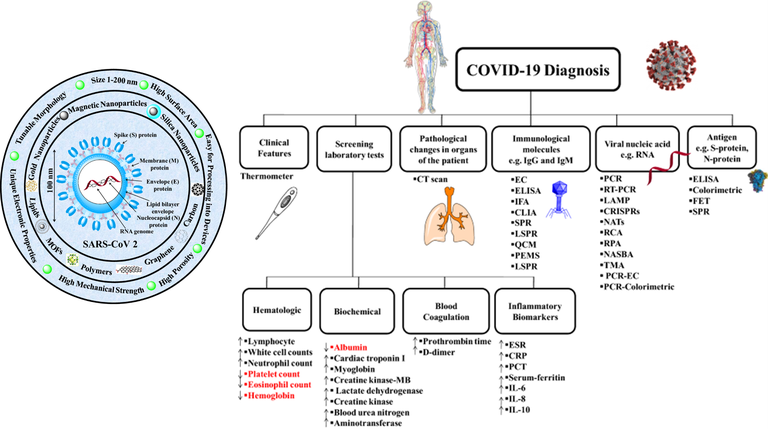
As nanopartículas apresentam desempenho promissor e grande potencial para servir de plataforma para o diagnóstico de infecções virais em curto espaço de tempo e com alta sensibilidade. Esta revisão destacou o potencial das nanopartículas como plataformas para o diagnóstico de COVID-19. Vários métodos analíticos podem ser usados para o diagnóstico de COVID-19. Existem três testes principais chamados testes moleculares (por exemplo, testes com base genética ou testes de ácido nucleico (NATs)), testes de antígeno e testes de anticorpos (por exemplo, testes sorológicos). Os pesquisadores alertam que as nanopartículas como nanopartículas de ouro, nanopartículas magnéticas e grafeno (G) foram aplicadas para detectar SARS-CoV-2 com sucesso (24/03/2021). Fonte: Nanotechnology for Environmental Engineering
29/03/2021
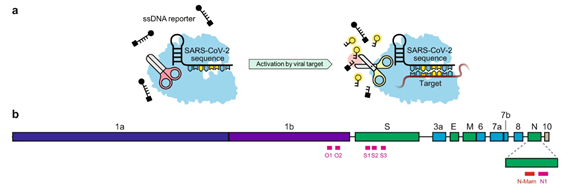
Os pesquisadores da universidade de Oxford desenvolveram um teste, que detecta a presença de anticorpos anti-vírus em vez de uma infecção por coronavírus, pode ser adaptado para trabalhar no sangue de uma picada no dedo - tornando-o rápido e fácil de usar. O teste baseia-se na ligação de uma parte da proteína viral da spike à superfície das células vermelhas do sangue. Quando os anticorpos contra o vírus estão presentes, eles criam um aglomerado de células vermelhas do sangue. Este aglomerado é grande o suficiente para ser visto a olho nu (29/03/2021). Fonte: University Oxford

Os autores propõem um sensor magnético (MRSw) baseado em pontos quânticos de grafeno magnético conjugado com anticorpo SARS-CoV-2 (GQDs) que reconhece especificamente o SARS-CoV-2. A sonda de MRSw pode ser misturada diretamente com a amostra de teste em um frasco totalmente selado sem pré-tratamento de amostra, o que reduz em grande parte o risco de infecção dos testadores durante a operação. A estratégia de tubo fechado de uma etapa para detectar SARS-CoV-2 é desenvolvida com ressonância magnética nuclear de campo ultrabaixo (ULF NMR) trabalhando a 118 μT. A sonda magnética baseada em GQDs mostra ultra-alta sensibilidade na detecção de SARS-CoV-2, e o limite de detecção é otimizado para 248 partículas mL‒1. Enquanto isso, o tempo de detecção no sistema ULF NMR é de apenas 2 min, o que pode melhorar significativamente a eficiência da detecção. Em suma, o MRSw magnético baseado em GQDs acoplado com ULF NMR pode realizar uma detecção rápida, segura e sensível de SARS-CoV-2 (15/06/2021). Fontes: Sensors and Actuators
Pesquisadores apresentam um ensaio de diagnóstico baseado em CRISPR que é robusto para mutações do genoma viral e temperatura, produz resultados rápidos, pode ser aplicado diretamente em amostras de nasofaringe (NP) sem purificação de RNA e incorpora um controle interno humano dentro da mesma reação. Especificamente, mostram que o uso da enzima AsCas12a projetada permite a detecção de SARS-CoV-2 de tipo selvagem e mutado e permite realizar a etapa de detecção com amplificação isotérmica mediada por loop (LAMP) em 60-65°C. Também revelaram que o uso de guias híbridos de DNA-RNA aumenta a taxa de reação, permitindo que o teste seja concluído em 30 minutos. Utilizando amostras clínicas de 72 pacientes com infecção por COVID-19 e 57 indivíduos saudáveis, demonstraram que o teste exibe uma especificidade e valor preditivo positivo de 100% com uma sensibilidade de 50 e 1000 cópias por reação (ou 2 e 40 cópias por microlitro) para amostras de RNA purificado e espécimes NP não purificados, respectivamente (19/03/2021). Fonte: Nature
26/03/2021
Pesquisadores desenvolvem um sensor FET (field-effect transistor) MXene-grafeno tanto para o vírus influenza quanto para o SARS-CoV-2. O sensor desenvolvido combina a alta sensibilidade química do MXene e a continuidade de alta qualidade do grafeno para formar um material de transdução ultrassensível para sensoriamento de vírus (VSTM). Através da ligação do polímero, os pesquisadores foram capazes de utilizar a ligação anticorpo-antígeno para alcançar a transdução de sinal eletroquímico quando os vírus são depositados na superfície do VSTM. O VSTM MXene-grafeno foi integrado em um canal microfluido que pode receber diretamente vírus na solução. O sensor desenvolvido foi testado com várias concentrações de antígenos de dois vírus: influenza inativada A (H1N1) variando de 125 a 250.000 cópias/mL e a proteína S recombinante do SARS-CoV-2 variando de 1 fg/mL a 10 pg/mL. O tempo médio de resposta foi de cerca de ∼50 ms, o que é significativamente mais rápido do que o método de PCR existente (>3 h). O baixo limite de detecção (125 cópias/mL para o vírus da gripe e 1 fg/mL para a proteína S recombinante do SARS-CoV-2) demonstrou a sensibilidade do MXene-grafeno VSTM à detecção de vírus na plataforma FET. Foi demonstrado também a ultrasensibilidade do sensor FET MXene-grafeno desenvolvido (02/03/2021). Fonte: ACS Omega
22/03/2021
A técnica chamada Surface Plasmon Resonance imaging (SPRi) foi utilizada para determinar a presença e a força de ligação de IgG, IgM e IgA contra o Domínio de Ligação ao receptor (RBD) do SARS-CoV-2 no soro de 119 pacientes com CoViD-19. O ensaio SPRi mede os níveis de isotipos de anticorpos e a força da ligação ao RBD de 384 amostras de pacientes em uma única corrida. Durante o curso da doença, os níveis de IgG e a força da ligação aumentaram enquanto geralmente os níveis de IgM e IgA decresceram. Todos os pacientes recuperados mostram alta resistência da ligação do tipo IgG à proteína RBD. O ensaio de imunoglobulinas anti-RBD por SPRi fornece insights adicionais sobre o estado imunológico dos pacientes em recuperação da CoViD-19 e este novo método pode, além disso, ser aplicado para a avaliação da qualidade da reação imune de indivíduos saudáveis ao SARS-CoV-2 em programas de vacinação (16/03/2021). Fonte: Biosensors and Bioelectronics

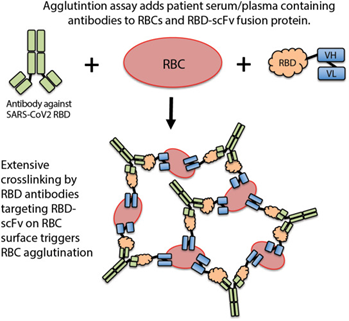
Estudo apresenta um método alternativo de teste de anticorpos que depende da adição de um reagente de proteína ao soro / plasma do paciente ou sangue total com leitura visual direta. Duas novas proteínas de fusão, RBD-2E8 e B6-CH1-RBD, foram projetadas para ligar glóbulos vermelhos (RBCs) por meio de um fragmento variável de cadeia única (scFv), exibindo assim o domínio de ligação ao receptor (RBD) da proteína spike de SARS-CoV -2 na superfície de RBCs. A mistura de RBD-2E8 e B6–CH1-RBD derivados de soro de paciente convalescente da COVID-19 e RBCs levou a hemaglutinação visível, indicando a presença de anticorpos contra SARS-CoV-2 RBD. Os pesquisadores demonstram que o teste de hemaglutinação usa métodos rotineiramente usados em laboratórios clínicos de hospitais em todo o mundo para tipagem sanguínea e assim, o teste pode ser implantado rapidamente em ambientes de poucos recursos a um custo mínimo (15/03/2021). Fonte: Biochemical and Biophysical Research Communications
17/03/2021
Pesquisadores do Instituto de Ciências Biológicas da Universidade Federal de Minas Gerais (UFMG) desenvolveram um teste rápido e de baixo custo capaz de monitorar as variantes mais perigosas do novo coronavírus em circulação atualmente no Brasil. O teste consegue identificar as variantes do Rio de Janeiro, de Manaus e a do Reino Unido, além da sul-africana, ainda não registrada no Brasil. A identificação do tipo da cepa foi possível graças a um aprofundamento no código genético das variantes feito pelos pesquisadores da UFMG. O custo bruto do teste para identificação das linhagens preocupantes é de R$ 60, 10% do valor cobrado para o sequenciamento total do novo coronavírus. A partir do teste capaz de apontar cada uma das variantes preocupantes em circulação no País será possível acompanhar a disseminação das mesmas (17/03/2021). Fonte: Estadão
Artigo apresenta um método para a detecção rápida de coronavírus diretamente em soluções aquosas com condutividade diferente. Para a pesquisa foi utilizado um sensor acústico baseado em uma slot wave em uma linha de atraso acústico. A adição de anticorpos diluídos em solução aquosa levou a uma mudança na profundidade e na frequência dos picos ressonantes na dependência da frequência da perda de inserção do sensor. A diferença nos parâmetros de saída do sensor antes e depois da interação biológica do vírus em soluções com os anticorpos específicos permite tirar uma conclusão sobre a presença/ausência dos vírus estudados na solução analisada. A possibilidade de detecção de vírus em soluções aquosas com a condutividade de 1,9–900 μs / cm, bem como na presença de partículas virais estranhas, foi demonstrada. O tempo de análise não excedeu 10 min (05/03/2021). Fonte: Sensors

Estratégias de controle que empregam testes RT-PCR para o diagnóstico e vigilância da epidemia de COVID-19 são ineficientes no combate à epidemia devido ao alto custo, demora na obtenção de resultados e necessidade de pessoal e equipamentos especializados para processamento laboratorial. Alternativas mais baratas e rápidas, como testes de antígeno e tira de papel, têm sido propostas. Eles retornam resultados rapidamente, mas têm limites de sensibilidade mais baixos para detecção de vírus. Para quantificar os efeitos das compensações entre sensibilidade, custo, frequência de teste e atraso no retorno do teste no curso geral de um surto, neste estudo, pesquisadores construíram um modelo imunoepidemiológico em várias escalas que conecta o perfil do vírus de indivíduos infectados com transmissão e teste ao nível da população. Observou-se que, quando a frequência de teste é aumentada para compensar o custo mais baixo de testes menos sensíveis, há uma grande redução na contagem de casos cumulativos, de 55,4% para 1,22% no semestre. Os resultados prevêem que o teste de vigilância que emprega testes de baixa sensibilidade em alta frequência é uma ferramenta eficaz para o controle da epidemia (11/03/2021). Fonte: Viruses
Neste estudo piloto, amostras de sebo foram coletadas de 67 pacientes hospitalizados (30 COVID-19 positivos e 37 COVID-19 negativos) por meio de gaze. A análise lipidômica foi realizada por cromatografia líquida e espectrometria de massas, identificando 998 características reproduzíveis. Análises estatísticas univariadas e multivariadas foram aplicadas ao conjunto de recursos resultante. Os níveis de lipídios estavam diminuídos em participantes positivos para COVID-19, indicativo de dislipidemia. Valores de p de 0,022 e 0,015 foram obtidos para triglicerídeos e ceramidas, respectivamente, com tamanhos de efeito de 0,044 e 0,57. A Análise Discriminante de Mínimos Quadrados Parciais mostrou separação de participantes COVID-19 positivos e negativos com sensibilidade de 79% e 83%, respectivamente, quando controlados para comorbidades. COVID-19 desregula muitas áreas do metabolismo; neste trabalho pesquisadores mostraram que o lipídio da pele pode ser adicionado à lista. Dado que as amostras podem ser fornecidas de forma rápida e indolor, concluíram que o sebo é digno de consideração futura para amostragem clínica (05/03/2021). Fonte: Lancet
12/03/2021
Os pesquisadores desenvolveram um novo biossensor baseado em bioluminescência para sondar uma interação vírus-hospedeiro-chave durante a entrada viral: a ligação da proteína spike (S) viral SARS-CoV-2 ao seu receptor, a enzima conversora de angiotensina 2 (ECA2). Derivado da tecnologia binária de Nanoluciferase (NanoBiT), o biossensor é composto de Nanoluciferase dividida em duas subunidades complementares, Large BiT e Small BiT, fundidas ao domínio Spike S1 da proteína SARS-CoV-2 S e ectodomínio ECA2, respectivamente. A interação ECA2-S1 resulta na remontagem da Nanoluciferase funcional, que catalisa uma reação bioluminescente que pode ser testada de maneira sensível e específica. Demonstraram a ampla faixa dinâmica do biossensor, termoestabilidade aprimorada e tolerância ao pH. Além disso, mostraram a versatilidade do biossensor para a triagem de alto rendimento de drogas que interrompem a interação ECA2-S1, bem como sua capacidade de atuar como um ensaio de neutralização de vírus substituto. Os resultados obtidos com biossensor se correlaciona com aqueles obtidos com um ensaio de lentivírus pseudotipado de Spike. Esta ferramenta rápida in vitro não requer vírus infeccioso e deve permitir o desenvolvimento de modalidades antivirais visando a entrada de SARS-CoV-2 (02/03/2021). Fonte: Biosensors and Bioelectronics
Estudo verifica o desempenho clínico, a sensibilidade e o fluxo de trabalho do Xpert Xpress e de dois kits rRT-PCR (BioGerm, Shanghai e Sansure, Hunan) de 86 pacientes sintomáticos foram avaliados. A concordância percentual positiva (PPA) do Xpert Xpress foi de 100%, seguido pelo Kit BioGerm (96,15%) e Kit Sansure (90%), respectivamente. O estudo ainda fornece algumas indicações para a seleção de métodos de diagnóstico (08/03/2021). Fonte: The Journal of Molecular Diagnostics
08/03/2021
Artigo descreve um protocolo livre de extração de RNA para detecção de SARS-CoV-2 por RT-qPCR a partir de amostras clínicas de swab nasofaríngeo em solução salina. O método inclui um tratamento com proteinase K seguido de inativação por calor (método PK + HID). Os pesquisadores demonstraram que PK + HID melhora o desempenho de RT-qPCR em comparação com o procedimento de inativação por calor. Além disso, mostraram que este protocolo livre de extração pode ser combinado com uma variedade de kits RT-qPCR de multiplexação (26/02/2021). Fonte: Plosone
03/03/2021
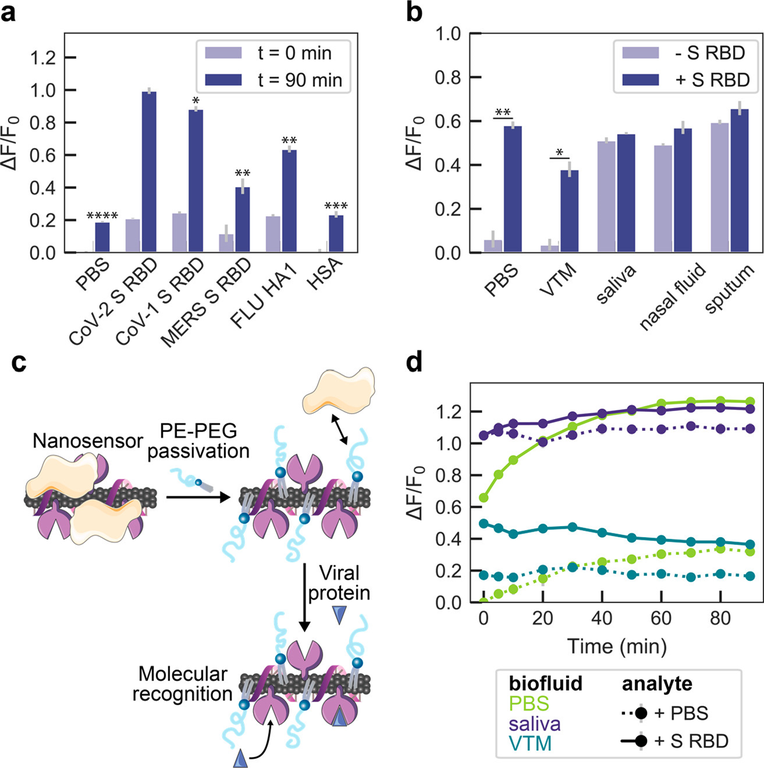
Estudo utiliza uma abordagem de sensoriamento óptico baseada em nanotubos de carbono de parede única (SWCNT) para este fim. Foi construído um nanosensor baseado em SWCNTs não covalentemente funcionalizado com ECA2, uma proteína hospedeira com alta afinidade de ligação para a proteína S de SARS-CoV-2. A presença da proteína S de SARS-CoV-2 provoca um aumento robusto de fluorescência no nanosensor de 2 vezes dentro de 90 minutos de exposição à proteína S. Foi caracterizado o mecanismo de estabilidade e sensoriamento do nanosensor e avaliação do nanosensor para a resposta sensoriante na saliva e no meio do transporte viral. Foi demonstrado ainda que esses nanosensores ECA2-SWCNT retêm a capacidade de detecção em um formato imobilizado na superfície, exibindo uma resposta de 73% de fluorescência dentro de 5 s de exposição a partículas semelhantes a SARS-CoV-2. Os dados demonstram que os nanosensores ECA2-SWCNT podem ser desenvolvidos como uma ferramenta óptica para detecção rápida de SARS-CoV-2 (26/02/2021). Fonte: Nano Letters
01/03/2021
Revisão discute os métodos de teste convencionais, rápidos e eficientes desenvolvidos para o diagnóstico do SARS-CoV-2. Os métodos de teste podem ser baseados na detecção de alvos, que incluem RNA, proteína S e anticorpos como IgG e IgM. Além do desenvolvimento do PCR direcionado ao RNA, foram desenvolvidos ensaios de neutralização de anticorpos e pseudovírus VSV, juntamente com várias outras técnicas de diagnóstico. Além disso, sensores baseados em nanotecnologia estão sendo desenvolvidos para o diagnóstico do vírus, e estes também são discutidos (03/02/2021). Fonte: ACS Applied Bio Materials
26/02/2021
Estudos demonstraram com o teste QuantiVirus™ SARS-CoV-2 tem um limite de detecção de 200 cópias/mL em amostras de saliva artificial. O desempenho clínico dos testes baseados na saliva é comparável ao dos testes baseados em swab nasifaríngeo. O estudo também demonstrou que o agrupamento de amostras de saliva para detecção de SARS-CoV-2 é viável (23/02/2021). Fonte: Plosone
Artigo mostra que o uso de PCR digital, um método de alta sensibilidade para detectar baixos números de amplicons, permitiu detectar corretamente a infecção em material de swab em um número significativo de falsos negativos. Os resultados mostraram um desempenho superior da amplificação dPCR para o diagnóstico de infecção por SARS-CoV-2 em indivíduos com títulos virais baixos em testes de swab convencionais. Além disso, dada a existência de múltiplos receptores e vias intracelulares envolvidas na entrada do vírus nas células, este método parece útil para investigar a base biológica da baixa replicação do SARS-CoV-2 nas vias aéreas superiores em uma proporção significativa de pacientes sintomáticos com COVID-19, com benefícios para a gestão geral do surto (22/02/2021). Fonte: Nature
Pesquisadores do Centro de Tecnologia em Nanomateriais e Grafeno da Universidade Federal de Minas Gerais (CTNano) desenvolvem tecnologia capaz de realizar, de forma mais rápida e barata, dois dos testes de diagnóstico para COVID-19: o sorológico, chamado de teste rápido, e o molecular, o RT-PCR. Os exames podem ser feitos na plataforma portátil de biodiagnóstico, equipamento criado pelos cientistas mineiros cuja tecnologia é inovadora em todo o mundo. Com o desenvolvimento iniciado em 2015, a plataforma é composta por duas partes: um leitor ótico, que pode ser portátil ou não, e os nanossensores. A tecnologia pode ser aplicada tanto para a realização de testes sorológicos, quanto molecular com alta sensibilidade e rapidez. A universidade tem a patente do leitor da plataforma e uma start up fez o licenciamento do equipamento para exploração comercial desse leitor. Os nanosensores são construídos de acordo com o diagnóstico que se pretende fazer. Portanto, não há uma transferência de patente. Eles são desenvolvidos em parceria com a universidade (25/02/2021). Fonte: Jornal Estado de Minas
24/02/2021
Fiocruz desenvolve teste rápido capaz de detectar variantes do coronavírus. Teste consegue identificar mutações das variantes do Brasil, Reino Unido e África do Sul. O RT-PCR foi aplicado em um grupo de 500 pessoas. Do total, 70% apresentaram resultado positivo para a variante brasileira P.1. O Laboratório Central de Saúde Pública do Amazonas será o primeiro a usar o produto. Os kits também estão sendo enviados para Rondônia, Roraima, Mato Grosso do Sul, Ceará e Rio de Janeiro (24/02/2021). Fonte: G1
Pesquisadores desenvolveram uma abordagem homogênea rápida para detecção de anticorpos denominada LFRET (imunoensaio de transferência de energia de ressonância de Förster resolvido com base em proteína L). No LFRET, a proteína L marcada com fluoróforo e o antígeno são colocados em estreita proximidade por imunoglobulinas específicas do antígeno, resultando no sinal de TR-FRET. Os pesquisadores realizaram ensaios LFRET para anticorpos contra proteínas S e N e avaliaram seu desempenho diagnóstico usando um painel de 77 amostras de soro/plasma de 44 indivíduos com COVID-19 e 52 controles negativos. Em seguida, compararam os ensaios LFRET com ensaios ELISAs e com um teste de microneutralização SARS-CoV-2 (MNT). Encontraram para os ensaios LFRET a sensibilidade de 90–95% e especificidade de 100%. Na identificação de indivíduos com ou sem uma resposta detectável de anticorpos neutralizantes, o LFRET superou o ELISA em especificidade de 91-96%, enquanto demonstrou uma sensibilidade igual 98%. Em conclusão, este estudo demonstra a aplicabilidade do LFRET, um ensaio de 10 minutos, para a detecção de anticorpos para SARS-CoV-2 (20/01/2021). Fonte: Viruses
Até o momento, não há um biomarcador prognóstico específico disponível para o SARS-CoV-2. Pesquisadores avaliaram se o valor do limiar do ciclo de PCR para SARS-CoV-2 (Ct) no momento do diagnóstico poderia predizer a gravidade da COVID-19, manifestações clínicas e sequelas de seis meses. Para tal, foi realizado um estudo retrospectivo transversal com dados de pacientes hospitalizados e ambulatoriais que foram amostrados aleatoriamente a partir dos diagnósticos de março de 2020 e os dados coletados aos 6 meses por entrevista. Os pacientes foram estratificados de acordo com sua Ct RNA-polimerase-RNA-dependente no swab nasofaríngeo no momento do diagnóstico, como segue: Grupo A ≤20,0, 20,0 <grupo B ≤28,0 e Grupo C> 28,0. A gravidade da doença foi classificada de acordo com uma escala composta avaliando admissão hospitalar, pior suporte de oxigênio necessário e sobrevivência. Duzentos pacientes foram incluídos, 27,5% nos Grupos A e B, 45,0% no Grupo C; 90% dos pacientes eram sintomáticos e 63,7% foram hospitalizados. O estudo concluiu que o Ct para o SARS-CoV-2 no diagnóstico está associado com a morte relacionada a COVID-19, gravidade da doença, número de sinais e sintomas e presença de sequelas de seis meses. A quantificação precoce do SARS-CoV-2 pode ser um marcador preditivo útil para informar estratégias diferenciais de manejo clínico e alocação de recursos (11/02/2021). Fonte: Viruses
22/02/2021
Dada a necessidade urgente de aumentar a cobertura de testes para COVID-19 e rastreamento de contato, pesquisadores examinaram a motivação dos indivíduos para fazer o autoteste e distribuir kits de autoteste. Este estudo de pesquisa usou dados do Mechanical Turk da Amazon (MTurk), uma plataforma online que fornece dados de alta qualidade relacionados à saúde. Os participantes receberam informações sobre os kits de autoteste e uma explicação de como os kits deveriam ser usados. Foi utilizada uma escala de 6 pontos (1 indicando extremamente improvável e 6 indicando extremamente provável) para medir os níveis de motivação para fazer o seguinte: (1) distribuir kits de autoteste para contatos se o indivíduo testasse positivo, (2) autoteste se o indivíduo recebeu um kit de um contato potencialmente infectado e (3) solicitar um kit de autoteste gratuito online se exposto à COVID-19. Na amostra de 586 adultos em análise, 59,7% eram do sexo masculino e a mediana de idade foi de 35 anos. A motivação para realizar cada uma das atividades de autoteste foi alta: 90,1% dos entrevistados foram motivados a distribuir kits de autoteste aos contatos; 86,1% estavam motivados para o autoteste se recebessem um kit de um contato potencialmente infectado, e 82,8% estavam motivados para solicitar um kit de autoteste online. Os autores concluem que a motivação é um pré-requisito para o comportamento voluntário e os seus achados sugerem que a distribuição dos kits de autoteste para COVID-19 pode contribuir para a detecção de casos (20/01/2021) Fonte: JAMA
17/02/2021
O alvo dos anticorpos neutralizantes geralmente está localizado na proteína do envelope na superfície viral, que medeia a entrada na célula. Como tal, a apresentação da proteína do envelope em uma partícula lentiviral representa uma alternativa conveniente ao manuseio de um vírus de contenção potencialmente alta ou para aqueles vírus sem sistema de cultura de células estabelecido. Neste artigo, pesquisadores apresentam uma visão geral do panorama das aplicações sorológicas de vetores lentivirais pseudotipados, com uma breve discussão sobre sua produção e análise da qualidade do lote. Finalmente, avaliaram seu papel como substitutos do vírus real e possíveis alternativas (31/01/2021). Fonte: Viruses
12/02/2021
Estudo desenvolve e testa um ensaio altamente sensível e robusto baseado na amplificação isotérmica mediada por loop de transcrição reversa (RT-LAMP) que usa reagentes prontamente disponíveis e um bloco de calor simples usando spike-in artificial e amostras clínicas reais. Este método de teste é baseado em RT-LAMP otimizado em um sistema escalonável que é suficientemente sensível e robusto para testar SARS-CoV-2 diretamente em amostras clínicas de esfregaço nasofaríngeo em meio de transporte viral em 30 min no ponto de atendimento sem a necessidade de um especialista ou equipamentos ou reagentes próprios (28/01/2021). Fonte: Nature

Estudo teve como objetivo investigar os cursos de tempo dos títulos de IgM e IgG anti SARS-CoV-2 e avaliar a sensibilidade e especificidade de testes usando métodos de imunoensaio quimioluminescente (CLIA) utilizando esferas magnéticas revestidas com proteína do nucleocapsídeo SARS-CoV-2 e proteína spike. De acordo com o dia específico após o início de COVID-19 entre uma população de pacientes no Japão. Dos resultados verificou-se que a sensibilidade do teste antes do dia 8 após o início dos sintomas era inferior a 50%; nos dias 9–10, obteve-se uma sensibilidade muito maior de 81,8% para IgM e IgG. 15 dias ou mais tarde após o início dos sintomas, o teste SARS-CoV-2 IgG teve uma sensibilidade de 100%. Esses resultados sugerem que, se o número de dias desde o início da doença for levado em consideração, esses testes de anticorpos podem ser muito úteis para o diagnóstico de COVID-19 e doenças semelhantes (02/02/2021). Fonte: Nature
Este estudo avalia vários protocolos para extração de RNA e RT-qPCR que são mais simples e menos caros do que os métodos predominantes. Primeiro, a precipitação com isopropanol é mostrada para fornecer um meio eficaz de extração de RNA de amostras de esfregaço de nasofaringe (NP). Em segundo lugar, a adição direta de amostras de swab NP a RT-qPCRs é avaliada sem uma etapa de extração de RNA. Uma solução simples e barata de coleta de esfregaço adequada para adição direta é validada usando amostras de esfregaço planejadas. Em terceiro lugar, uma master mix de código aberto para RT-qPCR que permite a detecção de RNA viral em amostras de swab NP é descrita. Por último, a imagem de fluorescência de ponto final fornece uma leitura diagnóstica precisa sem a necessidade de um termociclador qPCR. A adoção desses métodos simples e de código aberto tem o potencial de reduzir o tempo e as despesas dos testes COVID-19 (03/02/202). Fonte: PLOS ONE
10/02/2021
Pacientes com insuficiência respiratória aguda relacionada à COVID-19 requerem um diagnóstico imediato e preciso para triagem e manejo adequados. Os ensaios de PCR para RNA do SARS-CoV-2 podem ser realizados em amostras respiratórias superiores ou inferiores. Amostras de nasofaringe (NP) e de lavado broncoalveolar (BAL) geralmente têm boa concordância para infecções respiratórias virais. No entanto, relatórios descreveram pacientes com diagnóstico de SARS-CoV-2 por BAL após o teste NP negativo inicial. Neste artigo, pesquisadores estudaram dados de 123 pacientes que estavam gravemente enfermos (intubados) com uma preocupação clínica para COVID-19, que realizaram testes de PCR de NP e BAL para determinar as características e acurácia dos testes de NP e BAL. Setenta casos tiveram os testes NP e BAL positivos; 39 casos tiveram os testes NP e BAL negativos; 5 casos tiveram NP positivo e BAL negativo; e 9 casos tiveram NP negativo e BAL positivo. Os pesquisadores concluíram que os testes NP e BAL para detectar o SARS-CoV-2 têm uma concordância razoavelmente alta em pacientes com insuficiência respiratória quando testados dentro de 5 dias um do outro, mas ainda com alguma discordância. Portanto, pode ser razoável considerar a realização de BAL em pacientes com suspeita de infecção por COVID-19 após swabs NP negativos, e mesmo naqueles com swabs NP positivos, para avaliar a presença ou ausência de superinfecção bacteriana (01/01/2021). Fonte: American Journal of Respiratory and Critical Care Medicine
Swabs nasofaríngeos pareados (NPS) e espécimes de saliva foram coletados prospectivamente e testados por RT‐PCR de pacientes que se apresentaram em um pronto-socorro com sinais e sintomas compatíveis com COVID‐19. Um total de 348 amostras de 174 pacientes foram testadas por ensaios de RT‐PCR. Entre 174 pacientes com sintomas, 63 (36%) eram SARS‐CoV‐2 positivos em NPS usando a PCR otimizada. Destes 63 pacientes, 61 (98%) também eram positivos na saliva. Uma saliva SARS‐CoV‐2 positiva adicional foi detectada em um paciente com pneumonia. O RT‐PCR otimizado demonstrou maior sensibilidade analítica e clínica em comparação com o ensaio RT‐PCR comercial. Uma alta sensibilidade (98%) e concordância (kappa 0,96) em amostras de saliva em comparação com NPS foi demonstrada ao usar uma PCR otimizada, mesmo quando a carga viral na saliva era menor do que no NPS. Esta amostra não invasiva é fácil de coletar, evita desconforto aos pacientes e pode diminuir a exposição do pessoal de saúde (02/02/2021). Fonte: Journal of Medical Virology
05/02/2021
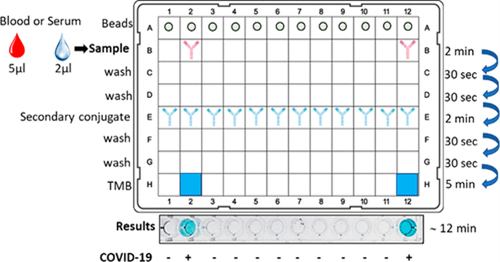
Pesquisadores da UFPR juntamente com pesquisadores alemães, desenvolveram um imunoensaio cromogênico simples baseado em esferas magnéticas que permite a detecção rápida, econômica e quantitativa de anticorpos humanos contra SARS-CoV-2 no soro, plasma ou sangue. A proteína recombinante do Nucleocapsídeo do SARS-CoV-2 marcada com 6xHis foi mobilizada na superfície de esferas magnéticas de Ni2+ e desafiada com amostras de soro ou sangue obtidas de controles ou casos COVID-19. O método foi validado por dois laboratórios independentes, e o desempenho para detectar a soroconversão de SARS-CoV-2 em humanos estava na mesma faixa obtida usando os imunoensaios padrão ouro ELISA e Luminex, embora exigindo apenas uma fração de material, instrumentação, tempo para entregar resultados e volume de amostra. Além disso, os resultados obtidos com o método descrito podem ser interpretados visualmente sem comprometer a precisão. A taxa de transferência do imunoensaio de esfera magnética pode ser personalizada sob demanda e é prontamente adaptada para ser usada com qualquer outra proteína ou peptídeo marcado com 6xHis como antígeno para rastrear outras doenças (26/01/2021). Fonte: ACS sensors
03/02/2021
Estudo utiliza uma tecnologia de microarray de proteínas para medições simultâneas e quantitativas de IgAs específicos para 8 patógenos respiratórios diferentes, incluindo adenovírus, vírus sincicial respiratório, vírus influenza tipo A, vírus influenza tipo B, vírus parainfluenza, Mycoplasma pneumoniae, Chlamydia pneumoniae e SARS‐CoV‐2 em amostra de soro de pacientes COVID‐19. Um total de 42 pacientes com COVID‐19 foram incluídos e classificados em casos graves (20 casos) e casos não graves (22 casos). Os resultados mostraram que a taxa de codetecção de IgA específica para SARS-CoV-2 com pelo menos um patógeno foi significativamente maior em casos graves do que em casos não graves (72,2% vs. 46,2%, p = 0,014). Os resultados indicam que a codetecção de anticorpos IgA para patógenos respiratórios pode fornecer valor diagnóstico para as clínicas e também ser informativo para estratificação de risco e gerenciamento de doença em pacientes com COVID-19 (27/01/2021). Fonte: Journal of Medical Virology
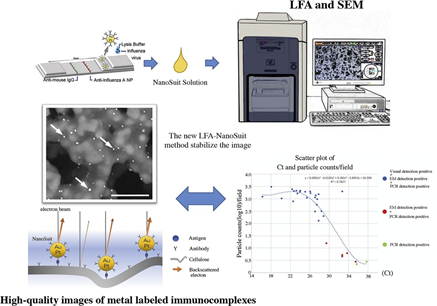
Devido à sua simplicidade e baixo custo, o ensaio de fluxo lateral (LFA) é uma das técnicas diagnósticas point-of-care mais utilizadas, apesar de sua baixa sensibilidade e má quantificação. Neste estudo pesquisadores relataram um método LFA-NanoSuit (LNSM) recentemente desenvolvido combinado com um microscópio eletrônico de varredura de mesa (SEM) para a observação direta de imunocomplexos marcados com um metal coloidal. O LNSM proposto suprime a deformidade da celulose, permitindo assim a aquisição de imagens de alta resolução de patógenos imunocomplexados marcados com ouro / platina, como o influenza A, sem tratamento condutor como no MEV convencional. O diagnóstico baseado em microscopia eletrônica da influenza A exibiu 94% de sensibilidade clínica e 100% de especificidade clínica, que foi mais sensível (71,4%) do que a detecção visual (14,3%), especialmente no grupo de menor número de cópias do A-RNA da influenza. A capacidade de detecção deste método foi quase comparável à do PCR. Este método de análise quantitativa simples e altamente sensível envolvendo LFA pode ser usado para diagnosticar várias doenças em humanos e animais, incluindo doenças altamente infecciosas, como a COVID-19 (26/01/2021). Fonte: Journal of Pharmaceutical and Biomedical Analysis
01/02/2021
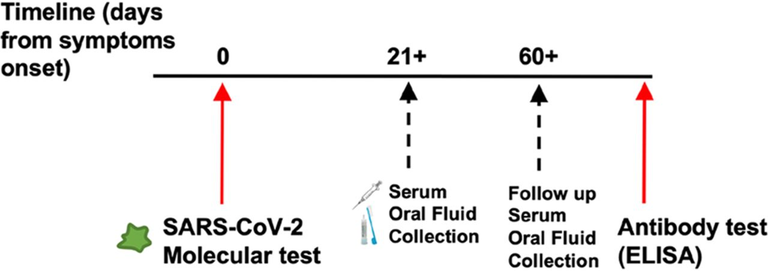
Os métodos atuais comercialmente disponíveis para detecção confiável de anticorpos contra a síndrome respiratória aguda grave coronavírus 2 (SARS-CoV-2) permanecem caros e inacessíveis devido à necessidade de coleta de sangue por pessoal treinado e equipamentos de proteção individual. Estudo avaliou uma abordagem de detecção de anticorpos usando o dispositivo de coleta de anticorpos orais da OraSure Technologies (OACD - oral antibody collection device) e seu ensaio de ELISA para de detecção de anticorpos totais contra o SARS-CoV-2. Descobrimos que o teste OraSure para detecção de anticorpos totais em fluido oral tinha sensibilidade e especificidade comparáveis aos ELISAs à base de soro disponíveis comercialmente para detecção de anticorpos de SARS-CoV-2, permitindo uma forma mais acessível de coleta de amostra com potencial para auto-coleta (21/01/2021). Fonte: J. Clin. Microbiol.
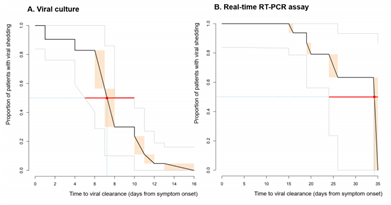
Em carta para editor pesquisadores discutem a duração da transmissibilidade da doença COVID-19 e o nível associado de contágio. Pesquisadores cultivaram o SARS-CoV-2 em amostras respiratórias em série, obtidas de pacientes hospitalizados com COVID-19 para avaliar a duração da eliminação do vírus viável. Foram estudados 21 indivíduos com COVID-19 confirmado pelo teste de RT-PCR hospitalizados. O ensaio Allplex 2019-nCoV (Seegene) para amostras de nasofaringe e orofaringe foi usado para o teste de RT-PCR em tempo real. O RNA viral foi quantificado com o uso do valor do limiar do ciclo para o gene N de SARS-CoV-2. As culturas virais foram conduzidas por meio de um ensaio de placa até que pelo menos duas culturas consecutivas não apresentassem crescimento. O SARS-CoV-2 foi cultivado em 29 das 89 amostras (33%). O tempo médio desde o início dos sintomas até a eliminação viral em cultura foi de 7 dias, e o tempo médio desde o início dos sintomas até a eliminação viral em RT-PCR em tempo real foi de 34 dias. A última cultura viral positiva foi 12 dias após o início dos sintomas (no Paciente 6). O vírus viável foi identificado até 3 dias após a resolução da febre (no Paciente 14). A cultura viral foi positiva apenas em amostras com um valor limite do ciclo de 28,4 ou menos. A incidência de positividade da cultura diminuiu com o aumento do tempo desde o início dos sintomas e com o aumento do valor do limiar do ciclo. Os resultados podem ser úteis para orientar os períodos de isolamento para pacientes com COVID-19 e para estimar o risco de transmissão secundária entre contatos próximos no rastreamento de contato (27/01/2021). Fonte: New Engl. J. Med.
29/01/2021
Estudo avalia a precisão diagnóstica do teste de amplificação de ácido nucleico (NAAT) da saliva para COVID-19. Para a revisão sistemática, foi realizada uma pesquisa das bases de dados MEDLINE e MedRxiv, visando encontrar estudos de precisão de testes diagnósticos. A meta-análise final foi realizada em 17 de novembro de 2020. Os estudos foram excluídos se a amostra contivesse menos de 20 participantes ou não fosse aleatória nem consecutiva. A estratégia de busca rendeu 385 referências e 16 estudos únicos foram identificados para síntese quantitativa. Oito estudos revisados por pares e 8 pre-prints foram incluídos nas meta-análises (5922 pacientes únicos). Houve variabilidade significativa na seleção do paciente, desenho do estudo e estágio da doença em que os pacientes foram matriculados. Quinze estudos incluíram pacientes ambulatoriais e 9 exclusivamente matriculados de uma população ambulatorial com sintomas leves ou sem sintomas. Na análise primária, a sensibilidade do NAAT da saliva foi de 83,2% e a especificidade agrupada foi de 99,2%. O NAAT de swab nasofaríngeo apresentou sensibilidade de 84,8% e especificidade de 98,9%. Os resultados foram semelhantes em análises secundárias. Os resultados sugerem, portanto, que a precisão diagnóstica do NAAT de saliva é semelhante à do NAAT de swab nasofaríngeo, especialmente no ambiente ambulatorial. Esses achados apoiam pesquisas em larga escala sobre o uso de saliva como uma alternativa aos cotonetes nasofaríngeos (15/01/2021). Fonte: JAMA
Pesquisadores avaliaram um teste de neutralização do vírus substituto (sVNT) desenvolvido recentemente em comparação com os testes de neutralização por redução de placa de 90% (PRNT90) em soros humanos, caninos, de gato e de hamster. Com PRNT90 como referência, o sVNT teve sensibilidade de 98,9% e especificidade de 98,8%. Usando um painel de soros imunes correspondentes a outros coronavírus, confirmou-se a falta de reatividade cruzada com outros coronavírus em SARS-CoV-2 sVNT e PRNT90, exceto para SARS-CoV-1 em sVNT (21/01/2021). Fonte: Journal of Clinical Microbiology
O RT-qPCR continua sendo o principal meio para diagnosticar o SARS-CoV-2, mas é demorado e caro. A amplificação da polimerase recombinante (RPA) é um ensaio de amplificação isotérmico que não requer uma máquina de PCR. É um ensaio acessível, rápido e simples. Neste estudo, pesquisadores desenvolveram e otimizaram um ensaio sensível de transcrição reversa (RT)-RPA para a detecção rápida de SARS-CoV-2 usando SYBR Green I e / ou fita de fluxo lateral (LF). A sensibilidade analítica e a especificidade do ensaio RT-RPA foram testadas usando RNA sintético diluído 10 vezes e RNA genômico de vírus semelhantes, respectivamente. A sensibilidade clínica e especificidade do ensaio RT-RPA foram realizadas usando amostras de nasofaringe 78 positivas e 35 negativas. A sensibilidade clínica e especificidade do RT-RPA foram 98% e 100%, respectivamente. O estudo mostrou que o RT-RPA representa uma alternativa viável ao RT-qPCR para a detecção do SARS-CoV-2, especialmente em áreas com infraestrutura limitada (06/01/2021). Fonte: PLOS ONE
27/01/2021
Estudo avalia os testes sorológicos que detectam anticorpos especificos para SARS-CoV-2 da Abbott anti-SARS-CoV-2 IgM e IgG , DiaSorin anti-SARS-CoV-2 IgG e Roche anti-SARS-CoV-2 frente ao testes PCR. As amostras de 175 pacientes com PCR positivo e 107 amostras de controle foram analisadas usando os ensaios Abbott IgM e IgG, DiaSorin IgG e Roche Total (IgA, IgG, IgM). Foram determinados a sensibilidade, especificidade, reatividade cruzada, concordância entre os ensaios, tendências ao longo do tempo, valor preditivo positivo (PPV) e valor preditivo negativo (NPV). Dos resultados a sensibilidade do Abbott IgM foi de 63,6% em 0 dias após a positividade do PCR, 76,5% em 1-5d, 76,3% em 6-14d, 85,2% em 15-30d e 63,6% em mais de 30 dias. Todos os ensaios exibiram maior sensibilidade 15 a 30 dias positividade pós-PCR (83,3-85,2%). A combinação de Abbott IgM e IgG melhorou a sensibilidade em 22,7% em comparação com IgG sozinho quando testado 0d pós-PCR de positividade. Todos os ensaios apresentaram especificidade de 100% e apenas Abbott IgG exibiu reatividade cruzada (anti-dsDNA) (19/01/2021). Fonte: Clinical Biochemistry
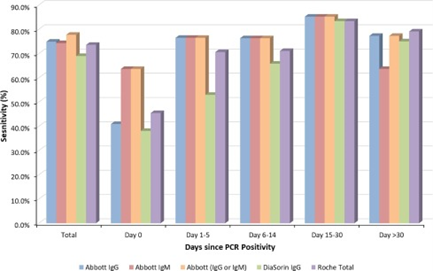
22/01/2021
Estudo desenvolveu um ensaio baseado em citometria de fluxo para detectar anticorpos da proteína spike de SARS-CoV-2 (proteína S) em pacientes COVID-19. O ensaio detecta IgM, IgA e IgG em pacientes COVID-19 e também a aquisição de todas as subclasses de IgG, com IgG1 sendo o mais dominante. A resposta do anticorpo é significativamente maior em um estágio posterior da infecção. Além disso, pacientes assintomáticos com COVID-19 também desenvolvem IgM, IgA e IgG específicos, com IgG1 como a subclasse mais dominante. Embora os níveis de anticorpos sejam mais baixos em infecções assintomáticas, o ensaio é altamente sensível e detecta 97% das infecções assintomáticas. Esses achados demonstram que o ensaio pode ser usado para análise sorológica de infecções sintomáticas, e também infecções assintomáticas, que podem, de outra forma, não ser detectado (12/01/2021). Fonte: Cell Reports Medicine
Recentemente, testes de diagnóstico que utilizam a técnica de amplificação de ácido nucleico LAMP receberam aprovação da FDA. Esta abordagem utiliza um corante indicador de pH para detectar queda no pH da hidrólise de nucleotídeo durante a amplificação do ácido nucleico. Este método só foi aprovado para uso com RNA extraído de amostras clínicas coletadas através de cotonetes nasofaríngeos. Neste estudo, foi desenvolvida uma estratégia quantitativa baseada na técnica de LAMP para detectar o RNA do SARS-CoV-2 na saliva. O sistema de detecção distinguiu positivo os tipos de amostra negativos usando um instrumento portátil que monitora alterações ópticas ao longo da reação LAMP. O protocolo de teste simplificado pode ser concluído em menos de duas horas para detectar diretamente SARS-CoV-2 inativado em saliva minimamente processada sem a extração de RNA, com um limite de detecção (LOD) de 50 cópias do genoma/reação. O método quantitativo detectou corretamente o vírus em 100% das amostras clínicas com SARS-CoV-2 inativados em 1X (50 genomas/reação) ou 2X (100 genomas/reação) do LOD (15/01/2021). Fonte: medRXiv
Pesquisadores fornecem um roteiro para mostrar como um instituto de pesquisa europeu pode ser reaproveitado em meio a esta crise, em colaboração com hospitais parceiros e um laboratório de diagnóstico estabelecido, aproveitando a experiência existente em manipulação de vírus, robótica, testes moleculares e informática para obter uma resposta rápida, de teste de diagnóstico contínuo de alto rendimento para detectar SARS-CoV-2 em indivíduos com suspeita de COVID-19. Segundo os autores, as vantagens potenciais da implementação de um canal de diagnóstico clínico em laboratórios de pesquisa são claras: um aumento substancial na capacidade de teste e a habilidade de adotar abordagens flexíveis e ágeis para testar em face das restrições globais (17/07/2020). Fonte: Nature Biotechnology
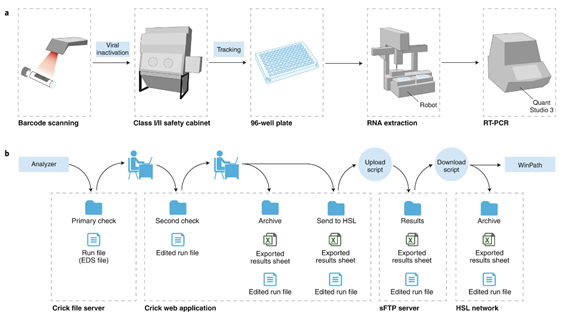
18/01/2021
Artigo apresenta biosensores de RNA ultrasensíveis para detecção de SARS-CoV-2 em um ensaio de cor simples e luminescência. No ensaio, a amplificação isotermal de um fragmento de RNA do SARS-CoV-2 juntamente com a ativação dos biosensores leva a um interruptor conformacional no sensor. Isso leva à tradução de uma proteína-repórter, por exemplo, LacZ que é facilmente detectada usando cor/luminescência. A resposta pode ser visualizada pelo olho humano, ou uma simples câmera de celular, bem como quantificada usando um espectrômetro/luminômetro. Otimizando a amplificação do RNA e o desenho do biosensor, foi desenvolvido um ensaio diagnóstico altamente sensível; com sensibilidade de detectar até 100 cópias de RNA do SARS-CoV-2. O método descrito detecta eficientemente a presença de RNA viral em amostras de pacientes humanos, com clara distinção a partir de amostras designadas negativas para o vírus. A resposta do biosensor correlaciona-se bem com os valores de TC e dos testes RT-qPCR e, portanto, apresenta uma estratégia poderosa e de fácil acesso para detectar a infecção por COVID-19 (08/01/2021). Fonte: medRXiv
Pesquisadores, com base na técnica de amplificação isotérmica e microfluídica de papel, criaram um teste portátil, no qual o RNA de SARS-CoV-2 é extraído, amplificado isotermicamente por RT-LAMP (Loop-mediated Isothermal Amplification) e detectado usando corantes intercalantes ou sondas fluorescentes. Dependendo da carga viral nas amostras testadas, a detecção leva entre vinte minutos e uma hora. Usando um conjunto de 16 pools de esfregaço nasofaríngeo, estimaram um limite de detecção comparável ao RT-PCR em tempo real e nenhuma reação cruzada com os oito principais vírus respiratórios circulando atualmente na Europa. Projetaram e fabricaram um dispositivo portátil fácil uso denominado “COVIDISC” para realizar o teste no local de atendimento. O baixo custo dos materiais, aliado à ausência de equipamentos complexos, vai agilizar a ampla disseminação desse dispositivo. O que o estudo propõe é uma nova ferramenta eficiente para ajudar a gerenciar as pandemias (11/01/2021). Fonte: PLOS

15/01/2021
Estudo busca analisar o potencial catalítico da DNAzyme semelhante à peroxidase através de um ensaio de detecção visual simples para o RNA SARS-CoV-2 usando um termociclador convencional pela geração induzida por PCR do sensor DNAzyme. O desempenho do sensor baseado em DNAzyme RT-PCR foi comparável ao do PCR em tempo real. DNAzyme mostrou 100% de sensibilidade e especificidade em amostras clínicas (swab nasofaríngeo), com uma boa correlação (Spearman) com o valor Ct da sonda de fluorescência PCR em tempo real. Os pesquisadores indicam que este teste de diagnóstico molecular barato, sensível e específico possa estender a capacidades de teste para a detecção de SARS-CoV-2 e assim reduzir a transmissão de COVID-19 (31/12/2020). Fonte: Frontiers in Molecular Biosciences
11/01/2021
O BioFire® COVID-19 Test é um teste qualitativo para uso nos sistemas FilmArray® 2.0 e Torch para a detecção de RNA SARS-CoV-2 em swabs nasofaríngeos (NPS) em meios de transporte. Este teste recebeu autorização de uso de emergência do FDA. Uma bolsa descartável fechada contém todos os reagentes necessários para a preparação da amostra, extração de ácido nucleico, transcrição reversa, reação em cadeia da polimerase (PCR) e detecção de ácido nucleico amplificado para identificar o RNA do vírus SARS-CoV-2 em uma amostra NPS. Os controles internos monitoram todas as etapas do processo de teste. Assim que uma amostra NPS (0,3 mL) é carregada na bolsa descartável do sistema, o teste totalmente automatizado retorna os resultados em uma hora (31/12/2020). Fonte: Open Forum Infectious Diseases

06/01/2021
Estudo avalia o desempenho do ensaio rápido do cartão de antígeno Abbott BinaxNOWTMCovid-19 para detecção de pessoas com altos níveis de vírus. Entre 3.302 pessoas testadas para SARS-CoV-2 por BinaxNOWTM e RT-PCR em um ambiente comunitário, a sensibilidade do ensaio rápido foi de 100% / 98,5% / 89% usando limiares de Ct de RT-PCR de 30, 35 e nenhum. A especificidade foi de 99,9%. O desempenho foi alto em todas as idades e naqueles com e sem sintomas (26/12/2020). Fonte: Clinical Infectious Diseases
30/12/2020
Pesquisadores apresentam um método para capturar e concentrar SARS-CoV-2 de amostras de saliva usando partículas de hidrogel magnético de captura por afinidade. Demonstraram que o método concentra vírus de amostras de 1 mL antes da extração de RNA, melhorando substancialmente a detecção de vírus usando RT-PCR em tempo real. Este método é compatível com os kits de extração de ácido nucleico comercialmente disponíveis (ou seja, da Qiagen). Além disso, testaram o método em amostras remanescentes de diagnóstico de meio de transporte que haviam sido previamente testadas para SARS-CoV-2, mostrando que o método não apenas identificou corretamente todas as amostras positivas, mas também melhorou substancialmente a detecção do vírus em amostras de baixa carga viral. A melhoria média no valor do limiar do ciclo em todos os títulos virais testados foi de 3,1. Finalmente, demonstraram que o método pode ser usado no teste agrupado, visto que foi observada uma melhora considerável na detecção do RNA do SARS-CoV-2 em volumes de amostra de até 10 mL (30/12/2020). Fonte: Scientific Reports (Nature)
18/12/2020
Estudo de análise longitudinal das taxas de infecção de COVID-19 usando testes de diagnóstico de PCR, imunoensaio de membrana e imunoensaio quimioluminescente de micropartículas (CMIA). Dos resultados os dados confirmam que os níveis de anticorpos diminuem três meses após o início dos sintomas. A comparação dos três métodos usados sugere que o teste quantitativo de CMIA pode detectar um número de indivíduos COVID-19 negativos maior do que realmente ocorre frente aos outros testes estudados (11/12/2020). Fonte: medRxiv
Pesquisadores desenvolveram um ensaio multiplex usando alvos SARS-CoV-2 bem estabelecidos juntamente com um controle celular humano (RPP30) e um controle da proteína S viral (Phorcine Herpes Virus 1 [PhHV-1]), que monitoram a qualidade da amostra e a eficiência de extração do ácido nucleico, respectivamente. Foi observado que este teste tem um desempenho tão bom quanto os ensaios comerciais amplamente usados, mas a um custo substancialmente reduzido. Além disso, há uma variabilidade (maior do que 1.000 vezes) no material coletado rotineiramente por swab combinado do nariz e da garganta e foi estabelecida uma correlação estatisticamente significativa entre o nível detectado de ácidos nucleicos humanos e SARS-CoV-2. A inclusão da sonda de controle humano neste ensaio fornece uma medida quantitativa da qualidade da amostra que pode ajudar a reduzir as taxas de falso-negativo. Foi demonstrada a viabilidade de um ensaio RT-qPCR robusto em aproximadamente 10% do custo de ensaios comerciais equivalentes, o que poderia beneficiar ambientes de poucos recursos e tornar acessível o teste de alto volume (15/12/2020). Fonte: PLOS
16/12/2020
Estudo de sorovigilância com uma amostra de 3.296 indivíduos selecionados aleatoriamente mostrou que a positividade do anticorpo COVID-19 IgG foi relatada em 7,37% (243) indivíduos. No entanto, quando 30 dias depois, oito dos 243 indivíduos positivos para anticorpos IgG para COVID-19 reclamaram de sintomas sugestivos de infecção por COVID-19 e foram confirmados como infecção por COVID-19 por reação em cadeia da polimerase de transcrição reversa (RT-PCR), seus anticorpos IgG COVID-19 foram testados novamente. Sete dos oito indivíduos previamente IgG positivos haviam perdido seus anticorpos protetores. Dos resultados apenas 28,36% mantiveram seus anticorpos IgG e 70,15% perderam seus anticorpos IgG. Três casos relataram resultados ambíguos no reteste (02/12/2020). Fonte: Cureus
10/12/2020
Estudo busca determinar a estabilidade do RNA do SARS-CoV-2 na saliva ao longo do tempo como a determinação do tempo ideal de armazenamento e transporte. Foi realizado estudo in vitro para avaliar se o SARS-CoV-2 poderia ser detectado em amostras de saliva artificial. As amostras de saliva estudadas compreendiam 10 ml de saliva combinada com SARS-CoV-2 com radiação gama para atingir uma concentração de 2,58 × 104 cópias/ml de SARS-CoV-2, que foi subsequentemente dividido em alíquotas de 2 ml compreendendo: (i) saliva pura; e uma diluição de 1: 1 com (ii) solução salina normal; (iii) meio de transporte viral e (iv) meio Amies líquido. O SARS-CoV-2 foi detectado em todas as amostras com adição de SARS-CoV-2 no ponto de tempo 0, dia 1, 3 e 7 em ambas as temperaturas de armazenamento usando o ensaio de RT-PCR do gene N e ponto de tempo 0, dia 1 e dia 7 usando o ensaio RT-PCR Xpert Xpress SARS-CoV-2 (03/12/2020). Fonte: Journal of Medical Microbiology
Estudo demonstra a aplicação potencial de anticorpos IgM e IgG e os antígenos virais para o diagnóstico e o curso da doença COVID-19, bem como a recorrência de testes de ácido nucleico positivos após a alta (02/12/2020). Fonte: Cell Biology International
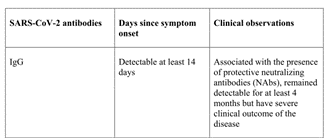
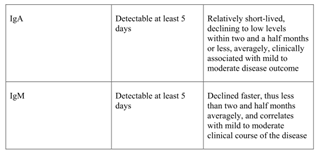
08/12/2020
Pesquisadores adaptaram um ensaio imunoenzimático (ELISA) à base de soro disponível comercialmente para uso com amostras de saliva, alcançando sensibilidade de 84,2% e especificidade de 100% em um conjunto de 149 amostras clínicas. Esta estratégia permitirá testes generalizados e acessíveis para pacientes que sofreram desta doença, ao mesmo tempo que minimiza o risco de exposição para profissionais de saúde (01/12/2020). Fonte: Scientific reports
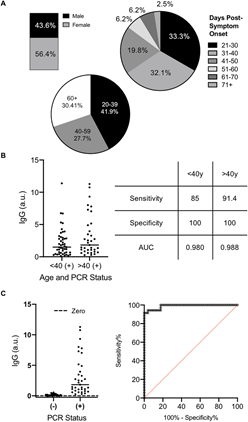
07/12/2020
Cientistas da Universidade de Oxford, no Reino Unido, usaram uma nova técnica para identificar danos não detectados por exames convencionais em 10 pacientes com idades entre 19 e 69. O método usa um gás chamado xenônio durante tomografias para produzir imagens que revelam a extensão do comprometimento dos pulmões mesmo após 3 meses da infecção por SARS-CoV-2. Os exames mostraram sinais de danos nos pulmões — destacando áreas onde o ar não flui facilmente para o sangue — em oito pessoas que relataram falta de ar (1/12/2020). Fonte: Terra

Estudo sugere que a detecção de RNA genômicos e subgenômicos do SARS-CoV-2 em amostras de diagnóstico não são um indicador de replicação ativa do vírus. Autores detectaram RNAs subgenômicos SARS-CoV-2 em amostras de diagnóstico até 17 dias após a detecção inicial da infecção e forneceram evidências de sua resistência à nuclease e proteção por membranas celulares, sugerindo que a detecção de RNAs subgenômicos em tais amostras pode não ser adequada como indicador de replicação ativa/infecção de coronavírus ativo (27/11/2020). Fonte Nature Communications
Teste usa técnica CRISPR e câmera de celular para detectar COVID-19. Pesquisadores combinaram crRNAs direcionados ao RNA de SARS-CoV-2 para melhorar a sensibilidade e especificidade e quantificaram diretamente a carga viral usando cinética enzimática. Isso acontece especificamente pela detecção do RNA viral na enzima Cas13, de modo que não é necessário fazer a transcrição do RNA em DNA, tampouco o processo de amplificação do teste PCR. Quando a Cas13 se liga ao RNA do vírus, ela cliva toda a sequência genética ao seu redor. Os pesquisadores desenvolveram uma sonda que, ao perceber essa reação, produz uma fluorescência detectada pela câmera, presa a um celular disposto logo acima do procedimento. Este ensaio tem o potencial de permitir um rastreamento rápido e de baixo custo no local de atendimento para SARS-CoV-2 (04/12/2020). Fonte: Cell
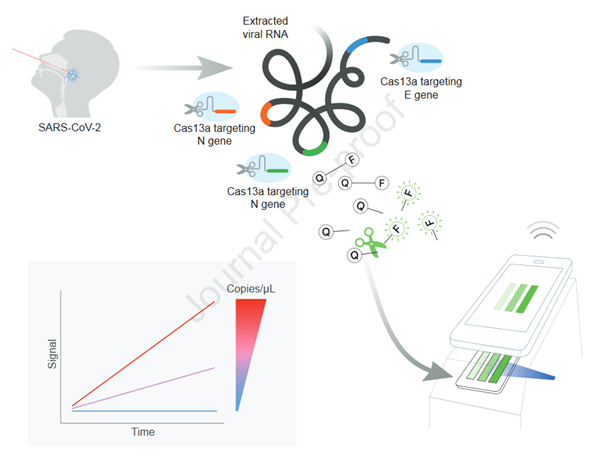
04/12/2020
Estudo apresenta a comparação do teste rápido de antígeno de SARS-CoV-2 com o RT PCR. 75 esfregaços nasofaríngeos SARS-CoV-2 positivos e 75 SARS-CoV-2 negativos foram analisados usando o SARS-CoV-2 Rapid Antigen Test (Roche). Das 75 amostras testadas para RNA SARS-CoV-2 negativo, 3 (três) tiveram um resultado positivo no SARS-CoV-2 Rapid Antigen Test, o que significa uma especificidade de 96%. Das 75 amostras SARS-CoV-2 positivo testadas, 53 tiveram um resultado positivo SARS-CoV-2 Rapid Antigen Test, o que significa uma sensibilidade de 70,7%. Como a sensibilidade geral é dependente da distribuição dos limiares do ciclo (Ct) na população de amostras, a sensibilidade foi recalculada de forma Ct-dependente. Para amostras com alta carga viral (Ct <25), a sensibilidade do teste rápido foi de 100%. A sensibilidade para amostras com carga viral média (Ct 25- <30), baixa (Ct 30- <35) e muito baixa (Ct>35) foi calculada para 95%, 44,8% e 22,2%, respectivamente (20/11/2020). Fonte: Journal of Virological Methods
02/12/2020
Estudo sugere que alguns testes rápidos para o coronavírus podem falhar em pessoas muito jovens e crianças, deixando infecções de baixo nível passar despercebidas. Artigo mostra avaliação do Binax NOW, um teste rápido fabricado pelo laboratório Abbott, com mais de 1.600 pessoas em Massachusetts. O teste detectou 96,5% das infecções por coronavírus encontradas por um teste laboratorial mais preciso em adultos com sintomas. Mas o teste rápido detectou apenas 77,8% dos casos sintomáticos em pessoas com 18 anos ou menos. Entre as pessoas sem sintomas, o teste teve performance ainda inferior, identificando 70,2% dos adultos e 63,6% das crianças (01/12/2020). Fonte: NYT
Neste estudo, as amostras de soro obtidas de 309 pessoas infectadas por SARS-CoV-2 e 324 de indivíduos saudáveis não infectados, bem como soro de 7 pacientes COVID-19 com 4-7 amostras, cada uma variando entre 1-92 dias após o primeiro PCR positiva foram testadas por um ELISA “interno” que detecta anticorpos IgM, IgA e IgG contra o domínio de ligação ao receptor (RBD) do SARS-CoV-2. Foram observadas sensibilidades de 47%, 80% e 88% e especificidade de 100%, 98% e 98% na detecção de anticorpos IgM, IgA e IgG, respectivamente. Os níveis de anticorpos IgG contra o RBD demonstraram ser regulados positivamente entre 1–7 dias após a detecção de COVID-19, mais cedo do que os anticorpos IgM e IgA. O estudo da cinética de anticorpos de sete pacientes COVID 19 revelou que, embora os níveis de IgG sejam altos e mantidos por pelo menos 3 meses, os níveis de IgM e IgA diminuem após 35–50 dias após a infecção. Em conjunto, esses resultados destacam a utilidade do ELISA baseado em RBD, que é fácil e barato de preparar, para identificar pacientes com COVID-19 mesmo na fase aguda. Os resultados desse estudo demonstram que apenas medir os níveis de IgG é suficiente e necessário para diagnosticar a exposição anterior ao SARS-CoV-2 (23/11/2020). Fonte: Plos One
USP disponibiliza teste para diagnosticar COVID-19 pela saliva. O teste foi desenvolvido no Centro de Pesquisa sobre o Genoma Humano e Células-Tronco da USP. O teste é baseado em uma técnica molecular amplamente utilizada para o diagnóstico de doenças infecciosas, como dengue, chikungunya, hepatite A e zika, chamada RT-LAMP (sigla em inglês de transcrição reversa seguida por amplificação isotérmica mediada por alça). A técnica molecular tem algumas semelhanças com o método RT-PCR, que utiliza como amostras para realização dos testes secreções do fundo da garganta e do nariz. Em ambas as técnicas são induzidas reações para a realização de uma fase de transcrição reversa (RT), na qual o RNA do vírus é transformado em DNA, e uma fase de amplificação, em que regiões específicas do vírus são replicadas milhões de vezes para que o patógeno possa ser identificado (01/12/2020). Fonte: Jornal Usp
30/11/2020
Neste estudo, avaliou-se o uso de bochecho oral (os voluntários foram solicitados a colocar 10 mL de água estéril na boca e com a boca fechada, agitar por 15 segundos, sem gargarejar e cuspir a água em recipiente estéril) e saliva orofaríngea posterior como alternativa aos métodos de coleta de swabs de profissionais de saúde sintomáticos e assintomáticos para a detecção do RNA do SARS-CoV-2 por RT-PCR. Para amostras de saliva, a concordância geral com esfregaços orofaríngeos foi de 93%, com uma sensibilidade de 96,7%. A concordância entre saliva e swabs nasofaríngeos foi de 97,7%, com sensibilidade de 94,1%. As bochechos orais (OR) foram comparadas com swabs nasofaríngeos (NPS) apenas, com uma concordância geral de 85,7% e uma sensibilidade de 63% . A concordância entre um teste desenvolvido em laboratório baseado no CDC RT-PCR e dois ensaios comerciais, o Xpert Xpress SARS-CoV-2 e o Cobas SARS-CoV-2, também foi avaliada. A concordância geral foi> 90%. Finalmente, o RNA do SARS-CoV-2 em amostras de saliva mostrou-se estável, sem alterações nas cargas virais ao longo de 24 horas à temperatura ambiente e 4°C. Embora a diluição de SARS-CoV-2 nos bochechos orais impessam sua aceitabilidade como tipo de amostra, a saliva orofaríngea posterior foi um tipo de amostra alternativa aceitável para detecção de RNA de SARS-CoV-2 (17/11/2020). Fonte: The Journal of Molecular Diagnostics
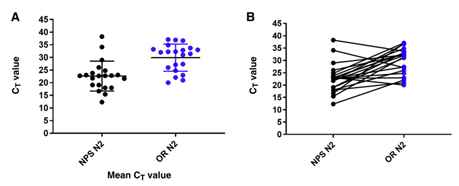
Estudo comparou o desempenho do teste de anticorpos SARS CoV2 e do teste RT-PCR para o diagnóstico da COVID-19. Para o propósito desta avaliação, usou o kit de teste de diagnóstico da Innovita® Biological Technology CO., LTD (China), com um total de 521 amostras de sangue que foram coletadas de pacientes que consentiram com o kit de diagnóstico rápido SARS COVID-19 e esfregaços orais e nasofaríngeos. A especificidade avaliada é considerada 100% para IgM e IgG, enquanto a sensibilidade avaliada foi de 87,3% para IgM e IgG. Os resultados mostraram uma sensibilidade geral muito baixa de IgM (14,4%) e IgG (15,6%). Em contraste com os resultados o estudo relata uma alta sensibilidade geral de teste de 88,7% e especificidade de 90,6% (27/11/2020). Fonte: medRxiv
27/11/2020
O teste multiplex permite maior sensibilidade e especificidade. Esta plataforma flexível, juntamente com uma metodologia de coleta discreta, seria crucial e amplamente útil para aumentar os testes em pandemias atuais e futuras. O volume mínimo de amostra que pode ser coletado usando cartões DBS pode ser processado neste formato de placa pilar multiplex, permitindo a capacidade de fornecer a confiabilidade de analisadores de alto rendimento, ao mesmo tempo que tem a facilidade de coleta semelhante aos testes rápidos (19/11/2020). Fonte: PlosOne
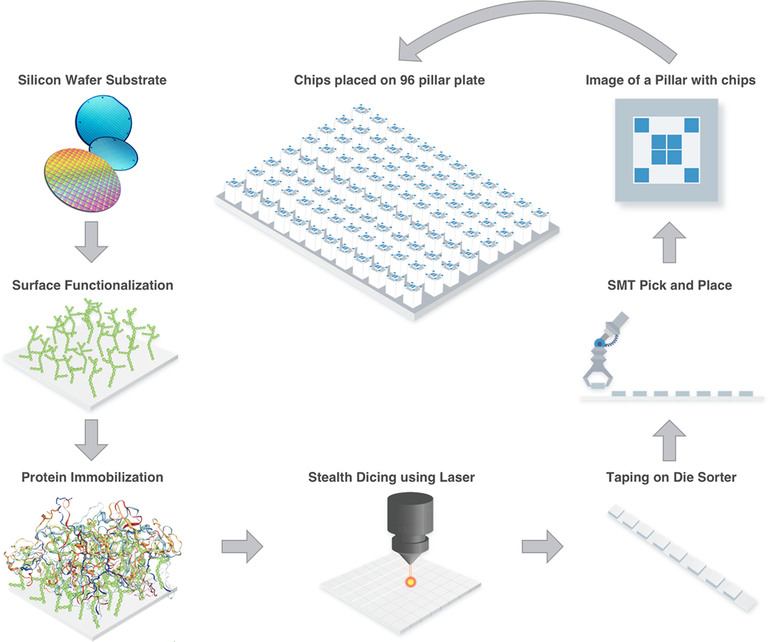
Pesquisadores desenvolveram um novo ensaio de papel quimioluminescente baseado em nanozima para detecção rápida e sensível do antígeno da proteína S de SARS-CoV-2, que integra nanozima e imunoensaio de quimioluminescência enzimática com a faixa de fluxo lateral. O núcleo do teste de papel é uma robusta nanozima Co-Fe @ hemin-peroxidase que catalisa a quimioluminescência comparável à peroxidase natural HRP e amplifica o sinal da reação imunológica. O limite de detecção para antígeno da proteína S recombinante de SARS-CoV-2 foi de 0,1 ng / mL, com uma faixa linear de 0,2-100 ng / mL. A tira reconheceu o antígeno SARS-CoV-2 especificamente e não houve reação cruzada com outros coronavírus ou subtipos de influenza A. Este teste pode ser concluído em 16 minutos. Além disso, a detecção de sinal é viável usando a câmera de um smartphone padrão e os ingredientes para a síntese das nanozimas são simples e prontamente disponíveis, reduzindo consideravelmente o custo geral. Em conclusão, o teste de papel fornece uma abordagem de teste de ponto de atendimento de alta sensibilidade (POCT) para a detecção do antígeno SARS-CoV-2, o que deve facilitar muito a triagem precoce de infecções por SARS-CoV-2 (13/11/2020). Fonte: Biosensors and Bioelectronics
Técnicas de detecção de vírus rápidas e robustas com ultra alta sensibilidade e seletividade são necessárias para o surto da doença coronavírus pandêmica 2019 (COVID-19) causada pelo SARS-CoV-2. Neste estudo, pesquisadores relatam que concentrações femtomolares de RNA de fita simples (ssRNA) de SARS-CoV-2 provocam transições em filmes de cristal líquido (LC) com surfactante catiônico e sonda de DNA de fita simples complementar 15-mer (ssDNA). Finalmente, os pesquisadores projetaram um kit de diagnóstico baseado em LC e um aplicativo baseado em smartphone (App) para permitir a detecção automática de ssRNA SARS-CoV-2, que poderia ser usado para autoteste confiável de SARS-CoV-2 em casa, sem a necessidade de equipamentos ou procedimentos complexos (17/11/2020). Fonte: Cell Reports Physical Science

17/11/2020
USP cria aparelho que fornece diagnóstico de COVID-19 em menos de um minuto. O dispositivo portátil faz a análise da presença do vírus SARS-CoV-2 no organismo em tempo real. Batizado de GRAPH COVID-19, o aparelho foi construído com base na plataforma DoC (Diagnostic On a Chip), uma tecnologia de biossensores avançados com nanocompósitos de óxido de grafeno. O GRAPH promete detectar e monitorar diversas doenças, principalmente a COVID-19, usando um baixo volume de amostra biológica, como apenas uma gota de sangue. Esta tecnologia traz benefícios significativos em relação a metodologias analíticas convencionais, tais como rapidez, alta sensibilidade e especificidade. Sua portabilidade permite diagnosticar o SARS-CoV-2 em qualquer local (07/11/2020). Fonte: Canaltech
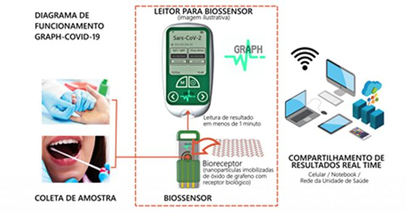
O teste desenvolvido pela Adaptive Biotechnologies seria o primeiro produto comercial a detectar a resposta de uma célula T ao vírus SARS-CoV-2. A empresa usou pequenas amostras de sangue de 1.000 pessoas em 25 áreas metropolitanas nos Estados Unidos, bem como outros 3.500 participantes da Europa para criar o teste, que pode detectar uma infecção recente ou passada do coronavírus (10/11/2020). Fonte: New York Times
A avaliação clínica intensiva da Public Health England e da Universidade de Oxford mostra que os testes de fluxo lateral são precisos e sensíveis o suficiente para serem usados na comunidade, inclusive para pessoas assintomáticas. Os testes de fluxo lateral são testes de resposta rápida que podem processar amostras de COVID-19 no local sem a necessidade de equipamento de laboratório, com a maioria gerando resultados em menos de meia hora. Esses novos testes estão sendo realizados em toda a Inglaterra, incluindo um piloto de duas semanas em uma cidade inteira em Liverpool, que foi lançado na semana passada. O esfregaço e o processamento desses testes devem ser realizados atualmente em um local de teste dedicado por uma equipe treinada. Os dispositivos são projetados para serem intuitivos e requerem treinamento mínimo para operar, e a PHE e a Universidade de Oxford estão agora analisando como esse teste pode ser autoadministrado (11/11/2020). Fonte: University Oxford
O Thermo Scientific OmnipathTM Combi SARS-CoV-2 IgG ELISA é um teste rápido projetado para ser executado em uma plataforma de instrumento aberta, relatando um ELISA anti-proteína S mensurando quantitativamente os anticorpos IgG para a proteína S do SARS-CoV-2 assim como é possivel identificar infecção anterior. Os desenvolvedores citam que a determinação do status dos anticorpos auxilia no diagnóstico e vigilância da doença durante os estágios agudos e de recuperação da infecção (10/11/2020). Fonte: University Oxford
16/11/2020
O teste de vírus viável amplamente aplicado junto com a serovigilância ajudará a reabrir a economia com mais precisão e velocidade e ajudará a orientar o isolamento, quarentena e protocolos de coorte em configurações de conglomerado, como instalações correcionais, enfermarias, escolas e viagens de longa distância (11/11/2020). Fonte: Viral Immunology
12/11/2020
Pesquisadores apresentam uma fórmula para estimar o tamanho do grupo ideal para pooling, o ganho de eficiência (pessoas testadas por teste) e o limite superior esperado de infecções perdidas no teste pool, tudo em função dos níveis de infecção de toda a população e das taxas de falso negativo / positivo em testes de PCR. Assumindo um nível de infecção de 0,1% e uma taxa de falsos negativos de 2%, o tamanho ideal do pool é de cerca de 34 e um ganho de eficiência de cerca de 15 pessoas/teste. Para um nível de infecção de 1%, o tamanho ideal do pool é 11, o ganho de eficiência é de 5,1 pessoas/teste. Para um nível de infecção de 10%, o tamanho ideal do pool reduz para cerca de 4, o ganho de eficiência é de cerca de 1,7 pessoas/teste. Para níveis de infecção de 30% e superiores, não há mais benefícios no pool (04/11/2020). Fonte: PLOS
Artigo descreve ensaios de tecnologia de matriz de suspensão quantitativa (qSAT) baseados na plataforma xMAP Luminex que superam as limitações dos testes de diagnóstico rápido e ELISA com maior precisão, faixa dinâmica, rendimento, miniaturização, custo-benefício e capacidade de multiplexação. Neste estudo foram desenvolvidos três ensaios qSAT para IgM, IgA e IgG para um painel de oito antígenos SARS-CoV-2, incluindo proteina spike (S), nucleoproteína (N) e construções de proteína de membrana (M). Os ensaios foram otimizados para minimizar o tempo de processamento e maximizar a relação sinal-ruído. O desempenho foi avaliado usando 128 plasmas pré-pandêmicos (controles negativos) e 104 plasmas de indivíduos com diagnóstico de SARS-CoV-2 (controles positivos), dos quais 5 eram assintomáticos, 51 apresentavam sintomas leves e 48 estavam hospitalizados. Anticorpos IgG pré-existentes que reconhecem as proteínas N, M e S foram detectados em controles negativos sugestivos de reatividade cruzada para coronavírus do resfriado comum. As assinaturas de anticorpo/antígeno com melhor desempenho tiveram especificidades de 100% e sensibilidades de 95,78% em ≥14 dias e 95,65% em ≥21 dias desde o início dos sintomas. A combinação de vários marcadores avaliados por ensaios qSAT tem a mais alta eficiência, amplitude e versatilidade para detectar com precisão respostas de anticorpos de baixo nível para obter dados confiáveis sobre a prevalência de exposição a novos patógenos em uma população. Estes ensaios permitirão obter informações sobre os correlatos de anticorpos da imunidade e sua cinética, necessários para o desenvolvimento de vacinas para combater a pandemia de COVID-19 (30/10/2020). Fonte: Journal of Clinical Microbiology
11/11/2020
Artigo descreve a produção escalonável e econômica de trímero de glicoproteína S do SARS‐CoV‐2 marcadas com His por células CHO que podem ser usadas para detectar anticorpos do SARS-CoV-2 em soros de pacientes com alta especificidade e sensibilidade. A produção foi aumentada significativamente (até 10,9 vezes) por uma redução na temperatura de cultura para 32 ° C para permitir culturas de duração prolongada. Com base nos dados, os pools de GS-CHO que produzem de forma estável o trímero da proteína S sob o controle de um forte promotor sintético foram cultivados em condições hipotérmicas com combinações de pequenas moléculas bioativas para aumentar o rendimento do produto purificado. O antígeno de trímero da proteína purificado a partir de células CHO foi usado em ensaio de imunoabsorção enzimática para detectar anticorpos imunoglobulina G contra SARS-CoV-2 em soros de coortes de pacientes previamente testados para infecção viral por PCR. O ensaio de anticorpos, validado para os padrões ISO 15189 Medical Laboratories, exibiu uma especificidade de 100% e sensibilidade de 92,3%. Os dados mostram que as células CHO são um hospedeiro adequado para a produção de grandes quantidades de trímero da proteina S recombinante que pode ser usado como antígeno para testes sorológicos em massa (31/10/2020). Fonte: Biotechnology and Bioengineering
10/11/2020
Estudo procura avaliar em que momentos durante a infecção o SARS-CoV-2 é detectável e não é mais detectável usando testes baseados em RT-PCR. Para isso foi realizada uma revisão sistemática dos dados individuais dos participantes (IPD) de estudos longitudinais de resultados de testes de RT-PCR em SARS-CoV-2 sintomático. Foram pesquisados os bancos de dados PubMed, LitCOVID, medRxiv e COVID-19 Living Evidence. Dos 5078 estudos selecionados, foram incluídos 32 estudos com 1023 participantes infectados com SARS-CoV-2 e 1619 resultados de testes, de - 6 a 66 dias após o início dos sintomas e hospitalização. A maior porcentagem de detecção de vírus foi de amostragem nasofaríngea entre 0 e 4 dias após o início dos sintomas em 89% caindo para 54% após 10 a 14 dias . Em média, a duração do vírus detectável foi maior com a amostragem do trato respiratório inferior (LRT) do que com a amostragem do trato respiratório superior (URT). A duração da detecção do vírus fecal e do trato respiratório variou muito entre os participantes individuais. Em alguns participantes, o vírus ainda era detectável 46 dias após o início dos sintomas. Os autores concluem que o RT-PCR falha na detecção de pessoas com infecção por SARS-CoV-2, no entanto a amostragem precoce minimiza diagnósticos falsos negativos. Os autores acreditam também que, dependendo do tempo de infecção e local de amostragem as taxas de positividade provavelmente estão superestimadas (04/11/2020). Fonte: BMC Medicine.
09/11/2020
Artigo apresenta uma abordagem melhorada para detectar ácido nucléico do SARS-CoV-2 com a capacidade de detectar apenas cinco equivalentes de genoma viral. A abordagem proporciona resultados sem a necessidade de purificar o RNA, reduz as etapas de manuseio, minimiza custos e permite a avaliação por equipamentos não especializados. O uso de amostras de swab não processadas é habilitado pela utilização de uma polimerase de DNA dependente de RNA e DNA, que executa a dupla tarefa de transcrição reversa rigorosa do RNA a temperaturas elevadas, bem como amplificação por PCR de um gene alvo específico do SARS-CoV-2. Como os resultados são obtidos dentro de 2 horas e podem ser lidos por uma tela LED portátil, este novo protocolo será de particular importância para a vigilância de vírus em larga escala em configurações economicamente restritas (02/11/2020). Fonte: PLoS One
06/11/2020
Novo ensaio simples, rápido e automatizado de neutralização do SARS-CoV-2 empregando uma abordagem ELISA (icELISA) in-cell. Após a otimização de vários parâmetros, como anticorpos específicos do vírus, linhagens celulares, doses de vírus e duração da infecção, as células infectadas pelo SARS-CoV-2 tornaram-se favoráveis como fonte direta de antígeno para o icELISA quantitativo. O novo teste SARS-CoV-2 icELISA permite rápida e automatizada (48 h no total, leitura em segundos) quantificação da infecção por vírus em uma cultura celular e pode ser utilizado para avaliar a eficácia dos anticorpos neutralizantes por vírus (Nabs) e medicamentos antivirais utilizando apenas reagentes e equipamentos presentes na maioria dos departamentos de diagnóstico (09/10/2020). Frontiers in Immunology
Através de um estudo de caso os autores propõem o uso da enolase específica do neurônio (NSE) como um biomarcador de lesão neuronal nas COVID-19 (19/10/2019). Fonte: CUREOS
Os autores apresentam a avaliação de um teste rápido de imunocromatografia para detecção viral com 75,5% de sensibilidade e 94.9% de especificidade (02/11/2020). Fonte: Journal of Clinical Microbiology
Os autores apresentam o desenvolvimento de um diagnóstico molecular de ácido nucleico baseado em CRISPR utilizando uma ribonuclease Cas13d derivada de Ruminococcus flavefaciens (CasRx) para detectar SARS-CoV-2, denominaram a abordagem SENSR (Sensitive Enzymatic Nucleic-acid Sequence Reporter). Demonstram que o SENSR detecta as sequências SARS-CoV-2 em amostras sintéticas e derivadas de pacientes (20/10/2020). Fonte: medRxiv
Pesquisadores desenvolveram um ensaio de anticorpo total SARS-CoV-2 e avaliaram a dinâmica da resposta do anticorpo ao longo do tempo em pacientes hospitalizados e não hospitalizados com COVID-19. Os ensaios de anticorpos totais sensíveis detectam anticorpos SARS-CoV-2 no domínio de ligação ao receptor (RBD) e proteína do nucleocapsídeo. A cinética dos anticorpos foi avaliada em pacientes com COVID-19 hospitalizados, confirmadas por PCR (n = 41) e três populações de pacientes com sintomas de COVID-19 que não requerem internação hospitalar: doadores convalescentes de plasma confirmados por PCR (n = 182) , trabalhadores hospitalares confirmados por PCR (n = 47) e um grupo de indivíduos sintomáticos amostrados longitudinalmente com alta suspeita de COVID-19 (n = 14). Em pacientes não hospitalizados, a resposta do anticorpo ao RBD é mais fraca, mas segue cinética semelhante à observada em pacientes hospitalizados. Em 11/14 dos casos suspeitos de COVID-19, a seroconversão no ensaio de ponte RBD pôde ser demonstrada antes do dia 12. Além disso, o estudo demonstrou a viabilidade da amostragem por picada de dedo para detecção de anticorpos contra SARS-CoV-2 usando esses ensaios. Em conclusão, os ensaios de ponte desenvolvidos detectam com segurança anticorpos SARS-CoV-2 em pacientes hospitalizados e não hospitalizados e, portanto, são adequados para conduzir estudos de soroprevalência (30/10/2020). Fonte: The Journal of Immunology
04/11/2020
Autores desenvolvem um método para medição ótica rápida e direta de partículas do vírus SARS-CoV-2 em uma etapa, quase sem qualquer preparação de amostra usando um biosensor de ressonância nanoplasmônica específico de proteína S. Foram detectados níveis de partículas virais tão baixo quanto 370 vp/mL em 15 min e a concentração de vírus pode ser quantificada linearmente na faixa de 0 a 107 vp/mL. As medições mostradas no leitor de microplaca genérico e em um dispositivo portátil conectado a um smartphone sugerem que o método de detecção rápido e de baixo custo pode ser adotado rapidamente em ambiente clínico regular e em configurações de recursos limitados (15/10/2020). Fonte: Biosensors and Bioelectronics
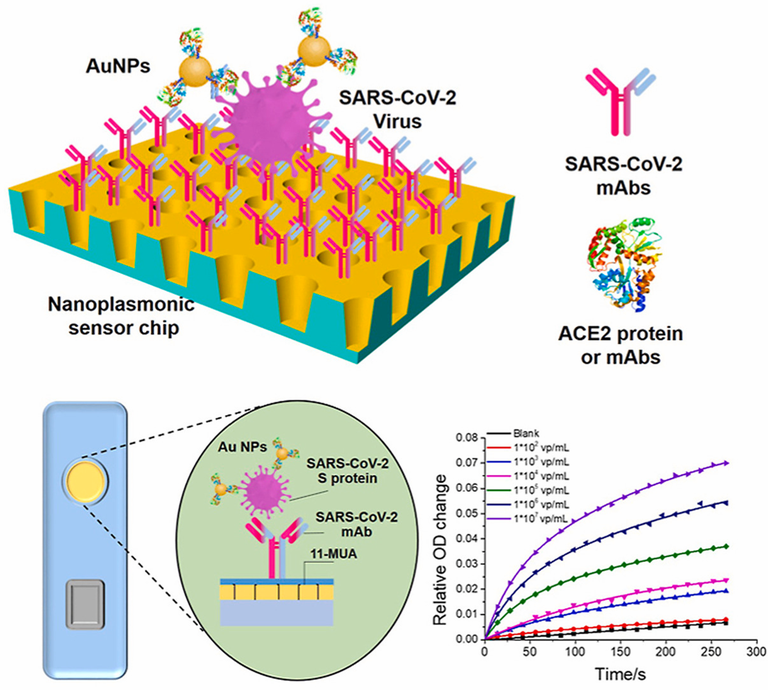
Estudo compara duas estratégias de agrupamento de amostras para detecção de RNA de SARS-CoV-2 para triagem eficiente de COVID-19. O teste de pooling pode oferecer uma abordagem econômica e eficaz para aumentar a capacidade de teste de vírus de laboratórios médicos sem exigir mais recursos de laboratório, como trabalhadores de laboratório, reagentes de teste e equipamentos. Neste estudo, os conjuntos de amostras de 6 e 10 foram detectados por um ensaio de RT-PCR direcionado aos genes ORF1ab e N do SARS-CoV-2 . Cada pool consistia em 5 ou 9 amostras negativas de SARS-CoV-2 e 1 contraparte positiva com cargas virais variáveis. Duas estratégias diferentes de agrupamento de amostras foram investigadas e os resultados foram comparados de forma abrangente. Uma abordagem foi agrupar o meio de transporte viral (VTM) das amostras no laboratório, e a outra foi agrupar as amostras de esfregaço durante o processo de coleta. Para a estratégia de pooling de swabs, os resultados qualitativos do RNA de SARS-CoV-2 (testes específicos de genes ORF1ab e N) permaneceram estáveis nos diferentes tamanhos de pool. Este estudo demonstra que a estratégia de coleta de swabs pode servir como uma abordagem eficaz e econômica para a triagem de infecções por SARS‐CoV‐2 em grandes populações, especialmente em países e regiões onde os recursos médicos são limitados durante a pandemia e podem, portanto, ser potenciais para aplicações clínicas de laboratório (27/10/2020). Fonte: Journal of Medical Virology
Pesquisa realizada para entender a correlação entre resultados de teste positivo de RNA viral prolongado, valores de limiar de ciclo (Ct) e crescimento de SARS-CoV-2 na célula. O PCR digital de gota (ddPCR) foi usado para avaliar a taxa de testes de diagnóstico COVID-19 falso-negativos. Em dois meses, 29.686 amostras foram testadas e 2.194 pacientes receberam testes repetidos. A liberação prolongada de RNA viral foi associada ao crescimento positivo do vírus em cultura de amostras coletadas até 20 dias após o primeiro resultado positivo, mas principalmente em indivíduos sintomáticos no momento da coleta da amostra. O sequenciamento do genoma completo forneceu evidências de que o mesmo vírus foi transportado ao longo do tempo. Os testes positivos após os testes negativos apresentaram valores de Ct superiores a 29,5 e não foram associados à cultura do vírus. ddPCR foi positivo em 5,6% das amostras negativas coletadas de pacientes com COVID-19 confirmados ou clinicamente suspeitos. Valores baixos de Ct em testes de diagnóstico de SARS-CoV-2 foram associados ao crescimento do vírus em cultura de células. Assim, os pesquisadores concluíram que pacientes sintomáticos com liberação prolongada de RNA viral também podem ser infecciosos (27/10/2020). Fonte: Clinical Infectious Diseases
03/11/2020
Estudo transversal para avaliar a prevalência de infecção por SARS-CoV-2 em 423 trabalhadores na província de Bérgamo que retornaram ao local de trabalho após o fim do bloqueio italiano em 5 de maio de 2020. Foi realizado um ensaio imunoenzimático (ELISA) para detectar a resposta humoral contra SARS-CoV-2 e um swab nasofaríngeo para avaliar a presença de RNA do SARS-CoV-2 por rRT-PCR. Dos resultados que o ELISA identificou tem-se 38,5% de indivíduos positivos, dos quais 51,5% foram positivos para IgG e IgM, 47,3% foram positivos apenas para IgG, mas apenas 1,2% foram positivos para IgM sozinho. Todos esses indivíduos rRT-PCR positivos já haviam experimentado soroconversão. Quando o ELISA foi usado como comparador, a especificidade e a sensibilidade estimadas do LFIA rápido para IgG foram de 98% e 92%, respectivamente (22/10/2020). Fonte: EBioMedicine
Estudo descreve um ensaio multiplex de ddRT-PCR em uma única etapa para quantificação confiável do RNA do SARS-CoV2. Ao determinar a abundância fracionária de RNA viral em relação a um gene humano de referencia, as cargas virais de diferentes amostras podem ser comparadas, o que poderia ser usado para investigar a infecciosidade e monitorar pacientes com COVID-19 (26/10/2020). Fonte: European Journal of Clinical Microbiology & Infectious Deseases.
29/10/2020
Estudo avaliou amostras de 175 pacientes com PCR positivo e 107 amostras de controles ensaios Abbott anti-SARS-CoV-2 IgM e IgG, DiaSorin anti-SARS-CoV-2 IgG e Roche anti-SARS-CoV-2 Total (IgA, IgG, IgM). Todos os ensaios exibiram maior sensibilidade 15-30d positividade pós-PCR (83,3-85,2%). Todos os ensaios apresentaram especificidade de 100% e apenas Abbott IgG exibiu reatividade cruzada (anti-dsDNA). Em conclusão, o ensaio Abbott IgM exibiu a resposta mais precoce e o maior sinal na maioria dos pacientes avaliados para amostragem seriada e teve o maior VPN <14 dias pós-PCR de positividade, sugerindo sua potencial utilidade como um teste adjunto para PCR no início do curso da doença (27/10/2020). Fonte: medRxiv
Pesquisadores coletam prospectivamente amostras nasofaríngeas (NPS) e amostras de saliva de um total de 300 pacientes adultos e pediátricos únicos. O RNA de SARS-CoV-2 foi detectado em 32,2% (97/300) dos indivíduos usando o TaqPath COVID-19 Combo Kit (Thermo Fisher). O desempenho da saliva e do NPS foi comparado com o número total de positivos, independentemente do tipo de amostra. A concordância geral para saliva e NPS foi de 91,0% e 94,7%, respectivamente. A concordância percentual positiva (PPA) para saliva e NPS foi de 81,4% e 89,7%, respectivamente. Em pacientes pediátricos sintomáticos e assintomáticos não previamente diagnosticados com COVID-19, os desempenhos da saliva e NPS foram comparáveis (PPA: 82,4% vs 85,3%). O PPA geral para adultos foi de 83,3% e 90,7% para saliva e NPS, respectivamente, com a saliva detectando 4 casos a menos do que NPS. No entanto, o desempenho da saliva em adultos sintomáticos foi idêntico ao NPS (PPA de 93,8%). Com menor custo e recursos de auto-coleta, a saliva pode ser uma escolha de amostra alternativa adequada ao NPS para detecção de SARS-CoV-2 em crianças e adultos (27/10/2020). Fonte: medRxiv
Estudo de coorte retrospectivo analisou 1114 pacientes com COVID-19 para identificação de tromboembolismo arterial ou venoso. Tromboembolismo arterial ou venoso, eventos cardiovasculares adversos maiores e tromboembolismo venoso sintomático ocorreram com alta frequência em pacientes com COVID-19, especialmente no ambiente de terapia intensiva, apesar de uma alta taxa de utilização de tromboprofilaxia (26/10/2020). Fonte: Journal of the American College of Cardiology.
27/10/2020
O teste meuDNA Covid, voltado para detectar o vírus em sua fase ativa é fruto de uma parceria do laboratório Mendelics com o Hospital Sírio-Libanês. O laboratório tem a capacidade de produzir 110 mil testes por dia. A amostra (saliva) é colhida pela própria pessoa por meio de um kit comprado pela internet. O exame usa o método PCR-Lamp (sigla em inglês de amplificação isotérmica mediada por loop), que identifica o RNA do vírus nas células da pessoa infectada e tem a mesma especificidade do RT-PCT, de 99%, e sensibilidade, de 80%. Além da capital São Paulo, o teste estará disponível para as cidades de Santo André, São Bernardo do Campo, São Caetano, Diadema, Osasco e Guarulhos. O exame custa R$ 169 e o resultado, que pode ser acessado pela internet, fica pronto em 24 horas (27/10/2020). Fonte: Terra
26/10/2020
Artigo propõe um algoritmo para agrupar subamostras baseado na geometria de um hipercubo que, em baixa prevalência, identifica com precisão os indivíduos infectados em um pequeno número de testes e rodadas de testes. São discutidos no artigo o tamanho ideal do grupo e relatados experimentos de prova de conceito nos quais uma subamostra positiva foi detectada mesmo quando diluída 100 vezes com subamostras negativas. Foi também quantificada a perda de sensibilidade devido à diluição e discutido como ela pode ser mitigada por frequentes novos testes de grupos, por exemplo. Com o uso desses métodos, o custo do teste de massa pode ser reduzido por um grande fator que, além disso, aumenta à medida que a prevalência cai. O uso de testes em grupo em grande escala para monitorar de perto e continuamente a infecção em uma população, junto com o isolamento rápido e eficaz das pessoas infectadas, fornece um caminho promissor para o controle de longo prazo de COVID-19 (21/10/2020). Fonte: Nature
23/10/2020
Estudo testou um método RT-LAMP em esfregaços nasais e faríngeos em 21 residentes de uma casa de cuidados de alta dependência, com dois casos de índice COVID-19, e comparou-o com a reação em RT-PCR. Os pesquisadores registraram os sinais vitais dos pacientes para correlacionar as informações clínicas e laboratoriais e calcular a sensibilidade, especificidade, valor preditivo positivo (PPV) e valor preditivo negativo (NPV) de um único swab usando RT-LAMP em comparação com o padrão atual, RT-PCR, de acordo com as diretrizes dos Padrões para Relatórios de Estudos de Precisão de Diagnóstico (STARD). O novo método detectou com precisão 8/10 casos positivos de RT-PCR e identificou mais 3 casos positivos. Oito outros casos foram negativos usando os dois métodos. A sensibilidade e especificidade de um único teste foram de 80 e 73%, respectivamente. A incorporação de reteste de positivos de RT-LAMP de baixo sinal melhorou a especificidade para 100%. Adicionalmente, especulou-se que a hipotermia pode ser um sinal clínico inicial significativo de COVID-19 (20/10/2020). Fonte: BMC
22/10/2020
Os testes rápidos de antígeno para o coronavírus fornecem resultados em 30 minutos. Mas nem todos os testes no mercado são igualmente eficazes na detecção do vírus. Estudo investigou 5 ensaios rápidos de antígeno comercialmente disponíveis em amostras de 1.754 pessoas com diagnóstico positivo para SARS-CoV-2, obtido por RT-PCR. Os dois testes mais sensíveis detectaram o vírus mais de 97% das vezes, enquanto o teste menos sensível o detectou em cerca de 75% dos casos. Os pesquisadores alertam que os testes rápidos podem ser menos eficazes em pessoas com baixos níveis de vírus (14/10/2020). Fonte: MedRxiv.
O objetivo deste estudo foi demonstrar que a saliva pode ser usada como um material eficaz para testes de SARS-CoV-2 e triagem de grandes grupos populacionais para identificar clusters de COVID-19. Dos resultados a saliva foi suficientemente estável para o teste por pelo menos 24 horas após a coleta. Os resultados obtidos na saliva de um paciente SARS-CoV-2 positivo foram consistentes com aqueles obtidos em swabs nasofaríngeos e orofaríngeos do mesmo paciente com sensibilidade de 90% e especificidade de 100% durante as primeiras duas semanas após o início dos sintomas (21/10/2020). Fonte: medRxiv
21/10/2020
Estudo teve como objetivo avaliar a utilização de pool de amostras como estratégia para otimizar o diagnóstico da SARS-CoV-2 por RT-qPCR. Um total de 220 amostras de esfregaço naso/orofaríngeo foi coletado e testado usando dois protocolos diferentes de agrupamento de amostras. Os resultados do protocolo A foram idênticos aos resultados individuais. Para os resultados do protocolo B, observou-se concordância reduzida (91%) em relação ao teste individual. As inconsistências observadas foram relacionadas aos resultados de RT-qPCR com limiares de ciclo mais elevados (16/10/2020). Fonte: European Journal of Clinical Microbiology & Infections Diseases
Ensaio baseado em RT-PCR de 50 min detecta o gene pan-sarbecovírus E e a região N2 do gene N como seu alvo específico para SARS-CoV-2. O ensaio testou 40 amostras nasofaríngeas que foram previamente confirmadas como positivas (n = 20) ou negativas (n = 20 ) usando o ensaio Da An Gene, na plataforma GeneXpert, usando o ensaio Xpert Xpress SARS-CoV-2. Descobriram que a sensibilidade do ensaio Xpert Xpress SARS-CoV-2 foi de 100% (20 de 20) e a especificidade foi de 80% (16 de 20) (19/10/020). Fonte: The Lancet Global Health
Pesquisadores apresentam uma comparação multicêntrica entre qRT-PCR padrão e DETECTR baseado em CRISPR para detecção rápida, sensível e específica de SARS-CoV-2 em amostras de 378 pacientes. O estudo conclui que o DETECTR pode ser rapidamente implementado como uma abordagem complementar tecnicamente independente para qRT-PCR, aumentando assim a capacidade de testes de laboratórios microbiológicos médicos e liberando as plataformas de PCR existentes para testagem de rotinas para diagnósticos (10/10/2020). Fonte: The Journal of Infectious Diseases
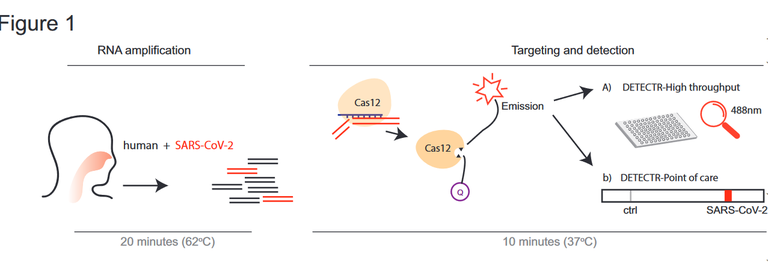
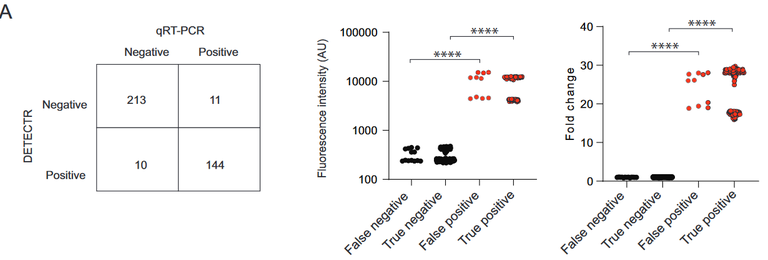
O teste RT-qPCR é um forte aliado para revelar a rápida disseminação geográfica de novos vírus. O estudo avaliou as variações da PCR no diagnóstico do SARS-CoV-2 ressaltando a importância do uso de abordagens filogenéticas não apenas para entender a evolução do vírus, mas também para projetar e revisar primers e sondas usados para o diagnóstico de SARS-CoV-2 via PCR (17/10/2020). Fonte: Journal of Molecular Medicine

19/10/2020
Artigo reflete o status atual, as perspectivas e os obstáculos práticos da tecnologia CRISPR/Cas para a detecção e inativação do SARS-CoV-2 (10/09/2020). Fonte: Frontiers in Molecular Biosciences
O estudo, conduzido por cientistas da Universidade da Califórnia, em San Francisco, está entre as primeiras comparações diretas entre um teste rápido BinaxNOW da Abbott e o RT-PCR. ferramenta de diagnóstico em condições do mundo real. No entanto, o número de participantes (878) foi comparativamente pequeno e os dados não foram revisados por pares ou publicados. Os testes têm como objetivo principal detectar a presença de níveis elevados do vírus, e não a sua ausência, e são autorizados apenas para avaliar pessoas sintomáticas. Dos dados dos 26 pacientes que obtiveram resultado positivo no RT-PCR o BinaxNOW identificou 15 (15/10/2020). Fonte: The New York Times
15/10/2020
Artigo apresenta uma metodologia para detecção e identificação de vírus que usa uma rede neural convolucional para distinguir entre imagens microscópicas de partículas intactas individuais de vírus diferentes. O estudo engloba rotulagem, imagem e identificação de vírus em menos de cinco minutos e não requer nenhuma etapa de lise, purificação ou amplificação. A rede neural treinada foi capaz de diferenciar o SARS-CoV-2 de amostras clínicas negativas, bem como de outros patógenos respiratórios comuns, como influenza e coronavírus humanos sazonais, com alta precisão (14/10/2020). Fonte: medRxiv e University of Oxford

Com base nos avanços mais recentes da pesquisa de tecnologias de ácido nucleico para SARS-CoV-2, este artigo apresenta os princípios e plataformas de tecnologia de detecção, comparou as vantagens e desvantagens de cada técnica e esclareceu o escopo de aplicações, fornecendo uma referência para selecionar a tecnologia de detecção de ácido nucleico apropriada para SARS-CoV-2. Além disso, o artigo fornece uma perspectiva para o desenvolvimento de tecnologias de detecção de patógenos semelhantes ao SARS-CoV-2 (05/10/2020) Fonte: Chinese Journal of Analytical Chemistry
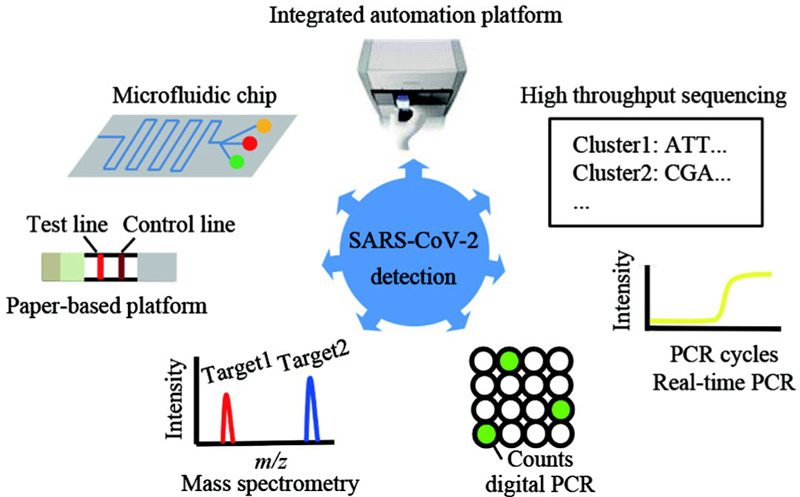
Revisão dos métodos atuais de diagnóstico que vem sendo realizado em diversos países como França, Austrália, China, Espanha comparando a sensibilidade / especificidade e identificando as lacunas no conhecimento sobre os testes de anticorpos para COVID-19 (13/10/2020). Fonte: Baylor University Medical Center Proceedings
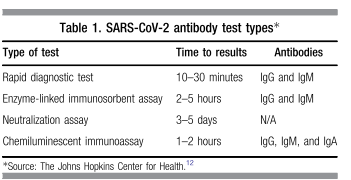
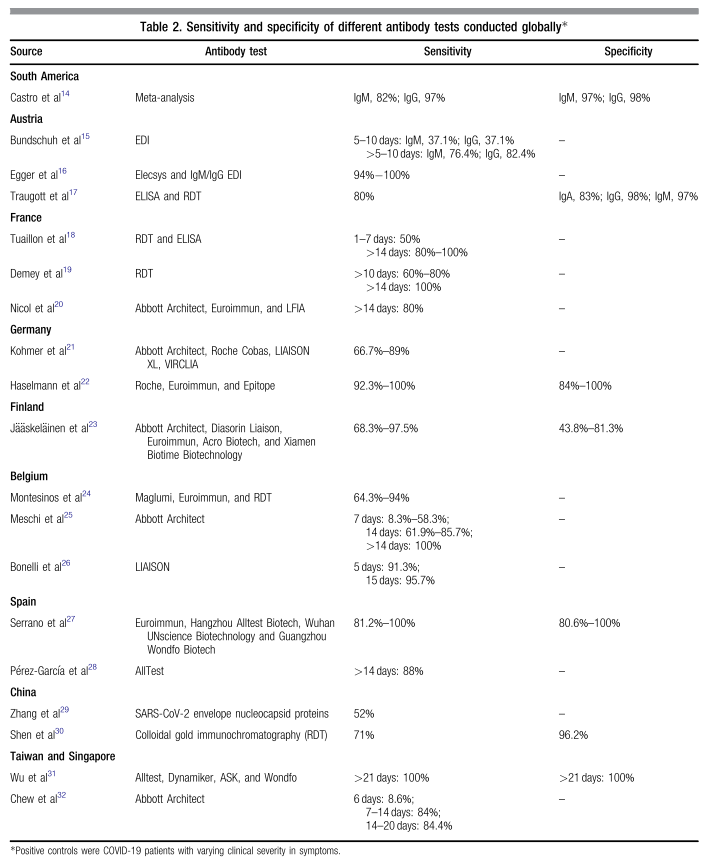
14/10/2020
Revisão avalia o estado atual do progresso no desenvolvimento de tecnologias de ponto de atendimento para o diagnóstico de doenças virais. Estudo aborda a necessidade para automatizar a preparação das amostras e outras recomendações especificas para enfrentar outras pandemias (11/10/2020). Fonte: Analytica Chimica Acta
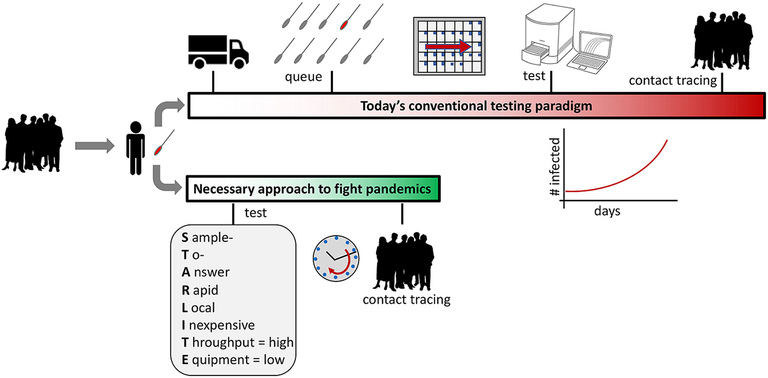
09/10/2020
Pesquisadores desenvolvem teste de diagnóstico em que o RNA do SARS-CoV-2 é detectado a partir de amostras nasofaríngeas por meio de um ensaio direto RT-qPCR que omite completamente a etapa de extração de RNA. A abordagem direta de RT-qPCR identificou corretamente 92% de um conjunto de referência de amostras cegas de NP (n = 155) que demonstrou ser positivo para RNA de SARS-CoV-2 por diagnóstico clínico tradicional RT-qPCR que incluiu uma extração de RNA. É importante ressaltar que o método direto teve sensibilidade suficiente para detectar com segurança os pacientes com cargas virais que se correlacionam com a presença de vírus infecciosos. Portanto, essa estratégia tem o potencial de expandir substancialmente a capacidade de teste e triagem da COVID-19 e deve ser aplicável em todo o mundo (02/10/2020). Fonte: PLOS Biology
08/10/2020
A multiplexação foi destacada, em vários estudos, como método de diagnóstico que economiza custos, aumenta o rendimento da amostra e maximiza o número de alvos que podem ser detectados com sensibilidade em uma pequena amostra. Este estudo, desenvolveu ensaios simplex (1 alvo), duplex (2 alvos), mistura de sondas triplex (3 alvos) e fourplex (4 alvos) com base em um sistema ddPCR de duas cores para detecção de SARS-CoV-2. Os resultados mostraram que o ensaio fourplex tinha limites de detecção e precisão semelhantes aos dos ensaios multiplex inferiores. A análise de 94 isolados clínicos demonstrou que o ensaio de mistura de sonda triplex ddPCR teve melhor sensibilidade do que o ensaio RT-qPCR (07/10/2020). Fonte: medRXiv
07/10/2020
Estudo demonstra que diagnósticos rápidos e confiáveis são necessários para SARS-CoV-2 neste contexto sugerem que a proteína do nucleocapsídeo (NP) do SARS-CoV-2 é um alvo ideal para a detecção baseada no antígeno viral. Um método rápido e conveniente foi desenvolvido com base no ensaio imunocromatográfico de fluorescência (FIC) para detectar o antígeno NP de SARS-CoV-2. O teste foi avaliado com 253 pacientes com o ensaio RT-PCR como padrão de referência. O teste do antígeno NP pelo ensaio FIC mostra alta especificidade e sensibilidade no diagnóstico de SARS-CoV-2 na fase inicial da infecção (05/10/2020). Fonte: Clinical Microbiology and Infection
Estudo apresenta um caso de COVID-19 em um paciente imunocompetente com fatores de risco para doença grave que se recuperou após positividade prolongada do swab de 61 dias após o início dos sintomas, sem disfunção respiratória e orgânica significativa. Estudo apresenta as razões por trás de sua positividade prolongada do swab no contexto do conhecimento atual da SARS-CoV-2 (04/10/2020). Fonte: BMJ
Neste estudo, pesquisadores projetaram crRNAs com alta sensibilidade e especificidade para detectar ácidos nucleicos usando CRISPR-Cas12a. Os ensaios de detecção baseados em CRISPR desenvolvidos anteriormente foram otimizados e combinados com o crRNA projetado no presente estudo com extensões de DNA para criar uma tecnologia CRISPR-ENHANCE (análise aprimorada de ácidos nucléicos com extensões de CrRNA). Em seguida, o CRISPR-ENHANCE foi aplicado para detecção aprimorada de uma variedade de alvos clinicamente relevantes, incluindo PCA3, HIV, HCV e SARS-CoV-2. Notavelmente, ao combinar uma etapa de amplificação isotérmica, este sistema mostra detecção aprimorada de RNA de SARS-CoV-2 com sensibilidade e especificidade melhoradas em um ensaio baseado em fluorescência e um ensaio de fluxo lateral baseado em papel (30/09/2020). Fonte: Nature Communications
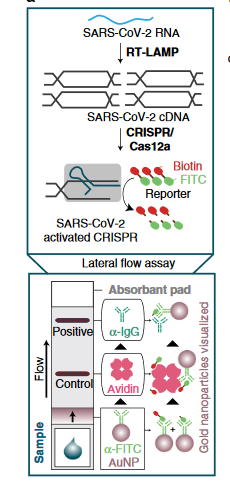
Logo depois que a pandemia da COVID-19 foi reconhecida pelos epidemiologistas, um grupo de biólogos que faz parte da Rede ARTIC desenvolveu um protocolo de reação em cadeia da polimerase multiplexada (PCR) e um conjunto de iniciadores para amplificação do genoma inteiro direcionado de SARS-CoV-2. O conjunto de primers ARTIC amplifica 98 amplicons, que são separados apenas em dois PCRs, em quase todo o genoma viral. No entanto, conforme a carga viral da amostra fica baixa, uma rápida diminuição na abundância de vários amplicons foi observada. Neste relatório, pesquisadores mostram que as formações de dímero entre alguns primers são a principal causa de viés de cobertura no PCR multiplex. Com base nisso, foram propostos 12 primers alternativos no total no conjunto de primers ARTIC que foram previstos para estar envolvidos em 14 interações de primers. O conjunto de primer resultante, versão N1 (NIID-1), exibe cobertura geral melhorada em comparação com o conjunto de primer original (V1) e modificado (V3) da Rede ARTIC (18/09/2020). Fonte: PLOS ONE
Artigo apresenta um ensaio All-In-One Dual CRISPR-Cas12a (AIOD-CRISPR) para detecção visual de SARS-CoV-2 e ultrassensível em um único recipiente. Tendo como alvo o gene da nucleoproteína de SARS-CoV-2, dois RNAs CRISPR são introduzidos para desenvolver o ensaio AIOD-CRISPR e detectar os ácidos nucleicos com uma sensibilidade de poucas cópias. O ensaio foi validado usando amostras de esfregaço clínico de COVID-19, para as quais foram obtidos resultados consistentes com o ensaio RT-PCR. Além disso, um aquecedor de baixo custo (~ $ 0,3) é usado como uma incubadora do ensaio AIOD-CRISPR para detectar amostras clínicas em 20 minutos, permitindo uma detecção visual de SARS-CoV-2 no local de atendimento. Assim, pesquisadores afirmam que este método desenvolvido por eles tem potencial significativo para fornecer um teste rápido e sensível para SARS-CoV-2 (18/09/2020). Fonte: Nature
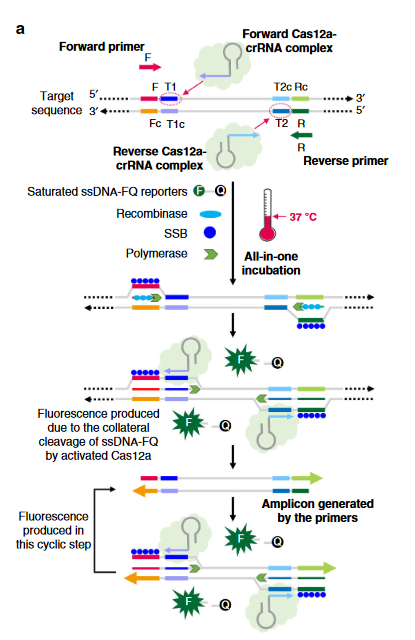
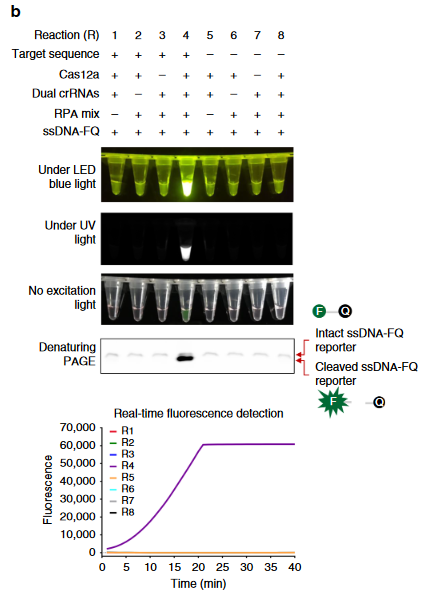
06/10/2020
O padrão de alta de um paciente deve ser rigoroso, pois tem grande importância para a prevenção e controle da epidemia, portanto, o objetivo do estudo foi formular padrões de alta mais rigorosos e científicos. Foram incluídos neste um total de 845 pacientes com COVID-19 leve que tiveram alta hospitalar. O tempo médio desde o início do COVID-19 até a ocorrência de dois testes consecutivos de ácido nucleico negativos nesses pacientes foi de 21 dias. Em 223 dos 845 pacientes que foram testados após dois testes de ácido nucleicos negativos consecutivos apresentaram testes positivos correspondendo a um total de 17,49% e o restante negativo, o tempo médio desde o início do COVID-19 até a ocorrência de três testes de ácido nucleico negativos consecutivos foi de 23 dias (intervalo: 3– 56 dias). Assim, os pesquisadores sugerem que o paciente deveria ser negativo em pelo menos 3 testes de ácido nucléico consecutivos antes da alta, e o tempo de teste não deveria ser anterior ao 23º dia desde o início da doença (02/10/2020). Fonte: Plosone
Os autores testaram e compararam o desempenho de um imunoensaio por quimiluminescência (CLIA), dois ensaios imunoenzimático (ELISA) e um imunoensaio por eletroquimioluminescência (ECLIA). O ensaio sorológico ECLIA teve o melhor desempenho e é apontado como um método de triagem válido para infecção por SARS-COV-2. Os autores apontam também que a IgA detectada pelo ensaio ELISA pode ser um marcador sorológico inicial mais confiável e estável do que o IgM. Em vez disso, os IgGs, como esperado, mostraram nível estável após 10 dias do início dos sintomas. O método ECLIA poderia ser usado como teste de triagem, considerando o excelente desempenho e o custo por teste único; enquanto o ensaio ELISA para IgG e IgA, que estão presentes em um nível superior ao de IgM e duram mais, pode ser usado como teste confirmatório (Outubro/2020). Fonte: Clinica Chimica Acta
Um teste indiano que promete acelerar e baratear o diagnóstico de COVID-19. Produto é baseado na tecnologia CRISPR, de edição de genes — e faz parte de 'terceira onda' no desenvolvimento de ferramentas de diagnóstico para COVID-19. Os cientistas estimam que o kit — chamado Feluda — daria resultados em menos de uma hora e custaria 500 rúpias (cerca de R$ 38). Pesquisadores do Instituto CSIR de Genômica e Biologia Integrativa, em Déli, onde o Feluda foi desenvolvido, fizeram experimentos com cerca de 2 mil pacientes. O novo produto mostrou ter sensibilidade de 96% e especificidade de 98% (06/10/2020). Fonte: R7
05/10/2020
Revisão dos avanços recentes nas estratégias relatadas por pesquisadores e engenheiros internacionais sobre como lidar com COVID-19 por meio de testes rápidos, principalmente por meio de testes de ácido nucleico e anticorpos. Os papéis dos biossensores como ferramentas analíticas são enfatizados para a detecção de RNAs virais, antígenos de superfície, partículas virais inteiras, anticorpos e outros biomarcadores potenciais em espécimes humanos. Além disso, esta revisão descreve possíveis estratégias futuras para detecção rápida de vírus (01/10/2020). Fonte: Biosensors and Bioeletronics
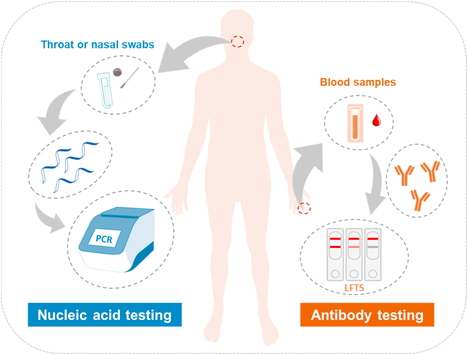
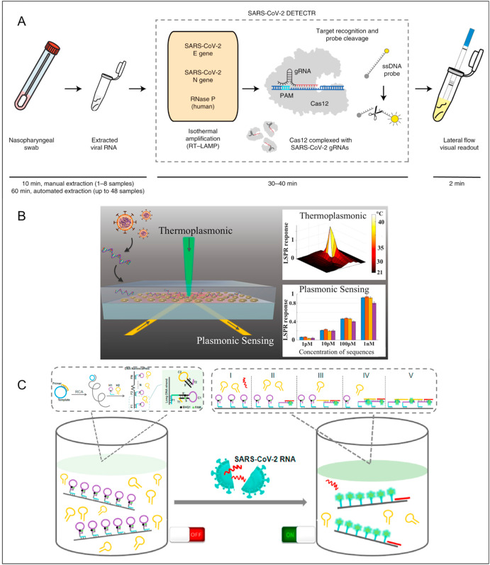
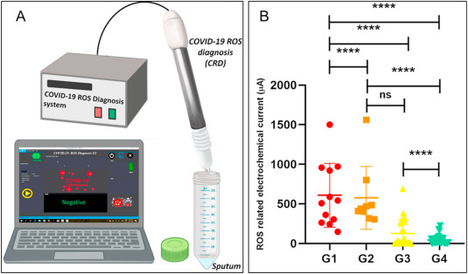
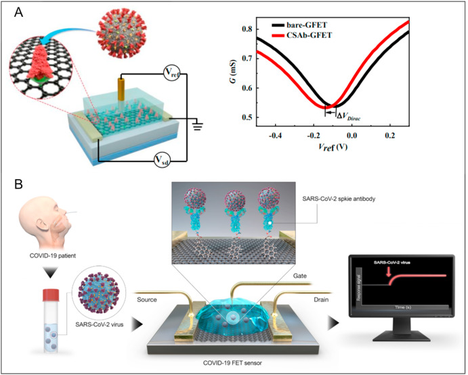
02/10/2020
Artigo questiona o uso de testes RT-PCR como ferramenta de vigilância sanitária no controle da COVID-19, pois o ensaio, além do seu alto custo e demora para resultado, apresenta sensibilidade muito alta, levando à detecção de quantidades muito pequenas de vírus. De fato, já se verificou que em mais de 50% das infecções identificadas por vigilância sanitária com base em PCR, os limites de ciclos passavam de 30, indicando baixa contagem viral. Embora a baixa contagem viral possa indicar início da infecção, o longo tempo de duração do chamado período “cauda de RNA positivo” sugere que a maior parte das pessoas já ultrapassou o período infeccioso. Economicamente, isto significa que pessoas estão sendo mantidas em isolamento por 10 dias, embora não se encontrem em fase de transmissão do vírus. Para um filtro efetivo de COVID-19, os autores sugerem testes capazes de detectar pessoas que são infecciosas e que o ensaio baseado em tecnologia CRISPR pode ser uma opção (30/09/2020). Fonte: New England Jornal of Medicine
Avaliação de desempenho do ensaio Panther Fusion SARS ‐ CoV ‐ 2 para detecção de SARS ‐ CoV ‐ 2 em amostras de saliva profunda da garganta, nasofaríngea e do trato respiratório inferior. O ensaio Panther Fusion SARS-CoV-2 tem desempenho comparável com o método de referência. Com sua capacidade de acesso aleatório e alto rendimento, o que maximiza a flexibilidade do teste SARS-CoV-2 em laboratório clínico (30/09/2020). Fonte: Journal of Medical Virology
01/10/2020
Estudo investigou a viabilidade e a precisão de uma abordagem de agrupamento de amostras para triagem populacional em larga escala para COVID-19. Um total de 940 amostras de esfregaço nasofaríngea (934 negativas e 6 positivas) previamente testadas para SARS-CoV-2 foram desidentificadas e designadas aleatoriamente em números para análise 94 conjuntos de 10 amostras foram gerados. A extração automatizada de RNA, seguida de RT-PCR, foi realizada em uma placa de 96 poços. Os pools positivos foram identificados e as amostras individuais foram reanalisadas. Dos 94 pools / poços, quatro foram positivos. Dos resultados gerais mostraram concordância 91,6% positiva e 100% negativa em comparação com a abordagem de teste individual (01/10/2020). Fonte: Journal of Molecular Diagnostics
29/08/2020
Pesquisadores desenvolveram uma plataforma para detecção rápida e de baixo custo de RNA viral com nanoswitches de DNA que se reconfiguram mecanicamente em resposta a vírus específicos. Usando o vírus Zika como sistema modelo, foi demonstrada a detecção não enzimática de RNA viral com detecção seletiva e multiplexada entre vírus relacionados e cepas virais. Para sensibilidade de nível clínico em fluidos biológicos foi realizado o ensaio com a preparação de amostra usando extração de RNA ou pré-amplificação isotérmica. O teste requer infraestrutura laboratorial mínima e é adaptável a outros vírus, conforme demonstrado pelo rápido desenvolvimento de nanoswitches de DNA para detectar o RNA do SARS-CoV-2 na saliva (25/ 09/ 2020). Fonte: Science Advances
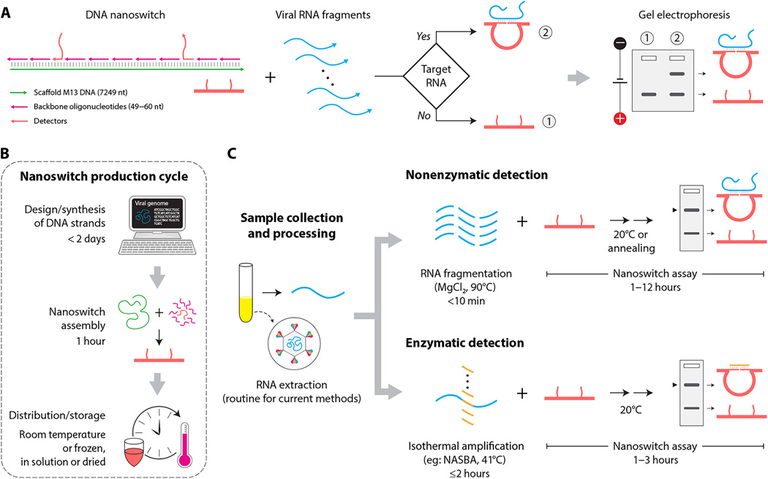
O recente aumento no número de pacientes com a COVID-19 testados como reação em RT-PCR positiva para SARS-CoV-2 após a recuperação causou dilema em relação as medidas e políticas médicas. Os pesquisadores avaliaram a dinâmica da carga viral e dos anticorpos anti-SARS-CoV-2 em 4 pacientes com resultados positivos de RT-PCR após a recuperação. Em todos os pacientes, os anticorpos IgG e IgM atingiram seu máximo cerca de um mês após o início dos sintomas iniciais. Então, os títulos de IgG estabilizaram e os títulos de IgM diminuíram, independentemente dos resultados de RT-PCR. Os anticorpos IgG e IgM não aumentaram após os resultados de RT-PCR positivos-negativos positivos em nenhum dos pacientes. Os dados reforçaram que os resultados positivos pós-negativos de RT-PCR podem ser devidos à detecção de partículas de RNA em vez de reinfecção ou recorrência em indivíduos que se recuperaram de COVID-19 (25/09/2020). Fonte: ClinOwl
Para atender à demanda urgente e massiva de rastreamento e diagnóstico de indivíduos infectados, muitos ensaios de diagnóstico in vitro usando testes de ácido nucleico (NATs) foram autorizados com urgência por reguladores em todo o mundo. Neste trabalho, realizou-se um estudo colaborativo para estimar as unidades detectáveis por NAT como quantidade equivalente genômica viral (GEQ) de um candidato a padrão de referência de vírus inteiro inativado SARS-CoV-2 usando PCR digital (dPCR) em várias plataformas comercializadas. O estudo demonstra que um vírus inteiro inativado quantificado por dPCR pode servir como um padrão de referência e fornece uma solução unificada para desenvolvimento de ensaio, controle de qualidade e vigilância regulatória (18/09/2020). Fonte: MedRxiv
28/09/2020
O estudo retrospectivo pre print realizado no auge da pandemia de COVID-19 em Moscou (Rússia) destaca a necessidade do diagnóstico da soroconversão da SARS-CoV-2 em pacientes com pneumonia (25/09/2020). Fonte: medRxiv
Estudo preprint faz uma avaliação dos imunoensaios SARS-CoV-2 comerciais quanto à sua capacidade de fornecer informações confiáveis sobre a atividade neutralizante do soro. Avaliou-se o desempenho de dois ensaios imunocromatográficos de fluxo lateral (LFIC) disponíveis comercialmente (teste Wondfo SARS-CoV-2 Anticorpo e o teste INNOVITA 2019-nCoV Ab) em comparação com um ensaio pseudotipado de neutralização SARS-CoV-2 para COVID-19 em pacientes hospitalizados. Noventa soros foram incluídos de 51 pacientes com COVID-19 moderado a grave dos resultados o uso dos ensaios LFIC avaliados se mostraram positivos e podem ser usados para prever altos títulos de anticorpos neutralizantes de SARS-CoV-2-S (25/09/2020). Fonte : medRxiv
A OMS vai disponibilizar 120 milhões de testes rápidos de COVID-19 para 133 países de baixa e média renda. O teste consiste em detectar antígenos(as proteínas do novo coronavírus Sars-CoV-2) e deverá mostrar resultados em 15 a 30 minutos. Assim como os testes PCR, os testes de antígenos identificam o vírus diretamente, porque detectam proteínas específicas que ele produz e que aparecem na superfície dele. Os testes serão fabricados pelas empresas SD Biosensor e Abbot, e o volume será garantido por meio da Fundação Bill e Melinda Gates. Cada teste custará US$ 5, cerca de R$ 28 (28/09/2020). Fonte: G1
Este estudo avalia um sistema de detecção molecular baseado em SARS-CoV-2 RT-LAMP rápido e completo, incluindo extração de RNA, para ponto de atendimento ou teste em massa de swabs nasofaríngeos. O formato de ponto de atendimento usa LoopX ©, um pequeno dispositivo portatil que garante a reação LAMP ideal e leitura automática com sensibilidade e especificidade alta (25/09/2020). MedRxiv
25/09/2020
Teste de CovidNudge RT-PCR rápido em tempo real, que não requer manipulação laboratorial ou pré-processamento de amostra. A plataforma é composta por dois componentes: o DnaCartridge e uma unidade de processamento. Um esfregaço nasofaríngeo ou orofaríngeo é inserido imediatamente, diretamente na câmara de esfregaço da unidade de preparação de amostra no momento da coleta. O swab é quebrado, deixando a ponta do swab e a amostra dentro da câmara, que é então selada. Os cartuchos são colocados na unidade de processamento que fornece o sistema pneumático, térmico, de imagem e mecânico necessários para executar uma reação RT-PCR em tempo real fora de um ambiente de laboratório (17/09/2020). Fonte: The Lancet Microbe
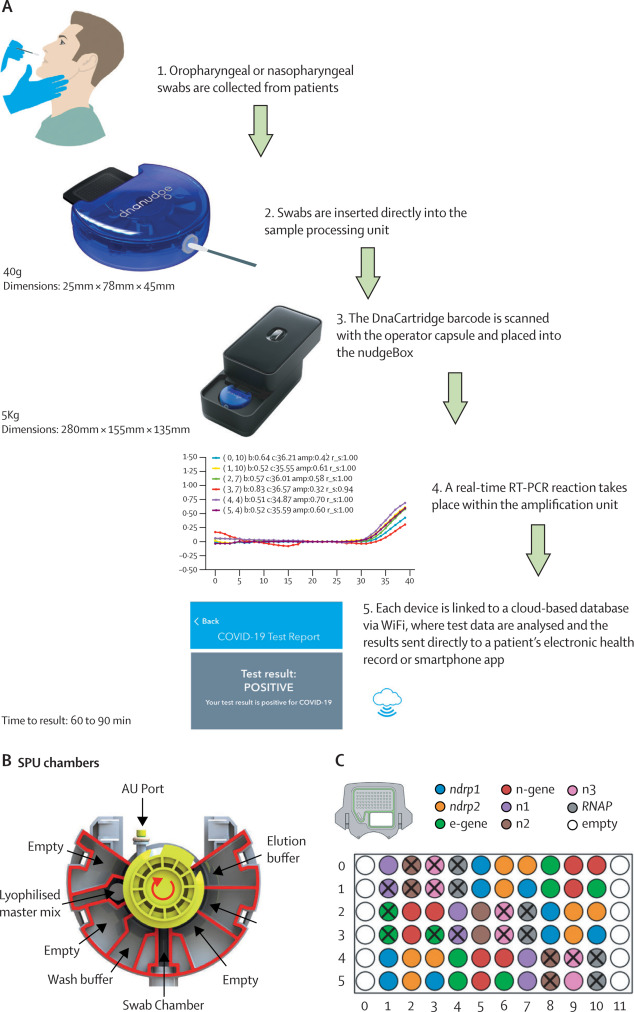
24/09/2020
Pesquisadores afirmam que as análises do RNA da SARS-CoV-2 na nasofaringe, frequentemente denominada de forma inadequada “carga viral”, não mostraram associações consistentes com doença assintomática versus doença sintomática ou com gravidade da doença sintomática. Segundo eles, medir o RNA viral no local da infecção inicial pode não fornecer uma avaliação precisa da replicação viral no trato respiratório inferior ou disseminação do vírus através do sangue para outros órgãos. Para muitas infecções, incluindo HIV e Ebola, a quantidade do patógeno no sangue é um forte indicador de prognóstico. Embora os dados atuais não sugiram que o vírus se replique de forma significativa nas células do sangue periférico, o vírus pode se disseminar para outros órgãos através do suprimento de sangue. Nessa linha, alguns grupos já relataram a detecção do RNA do SARS-CoV-2 no plasma. Para os cientistas algumas questões ainda precisam ser respondidas: O ácido nucleico viral indica a presença de partículas virais e/ou células infectadas? Se os vírions estiverem presentes, eles são infecciosos? E se houver células infectadas, elas estão produzindo vírus infeccioso? A detecção de RNA viral no plasma pode sinalizar infecção não controlada e risco de complicações que requerem intervenção precoce? As terapias que previnem ou reduzem a viremia podem estar associadas a uma melhora no resultado? (08/09/2020). Fonte: Clinical Infectious Diseases
Artigo tenta demonstrar a importância da realização do RT-PCR em casos de alto índice de suspeita para COVID-19 e apresenta o caso de um homem de 47 anos internado por febre e pneumonia bilateral diagnosticado via tomografia computadorizada do peito no auge do pico da pandemia de COVID-19, sugerindo uma infecção SARS-CoV-2. Dois resultados de RT-PCR de amostras de swab nasofaríngeo foram negativos. A broncoscopia foi então realizada, e testes de RT-PCR em amostras de lavagem broncoalveolar produziram resultados positivos, confirmando o diagnóstico de COVID-19. O caso demonstra que amostras de RT-PCR do trato respiratório inferior provavelmente contêm uma maior carga do vírus e, portanto, retêm uma sensibilidade maior para a detecção de SARS-CoV-2 (21/09/2020). New Microbes and New Infections
23/09/2020
Artigo porpõe um método para aprimorar o processamento de grandes quantidades de amostras coletadas. O método é baseado na mistura de amostras em tubos de teste (pooling) em uma configuração específica, ao invés de testar amostras únicas em cada tubo, e reconhecer amostras infectadas de variações das taxas de infecção total em cada tubo. A aplicação do método proposto permite testar muito mais pacientes usando o mesmo número de tubos de teste, onde todos os positivos são identificados sem falsos negativos e sem necessidade de testes independentes, e o tempo de teste efetivo pode ser reduzido drasticamente, mesmo quando a incerteza no teste é relativamente alta (13/09/2020). Fonte: Health Systems

Revisão é parte do "Open Evidence Review on Transmission Dynamics of COVID-19" (Transmission Dynamics of COVID-19 – CEBM) e tem por objetivo analisar estudos de cultura de SARS-CoV2, o melhor indicador para definir infecção ativa e capacidade de infecção, a partir amostras obtidas de pacientes com resultados de RT-PCR (reverse transcriptase-polymerase chain reaction) positivo. Os estudos foram selecionados em LitCovid, medRxiv, Google Scholar e Google por COVID-19 para cultura viral ou replicação viral e sinônimos associados, até 31 de agosto de 2020. Foram realizadas correspondência de citações e foram incluídos estudos que relataram tentativas de cultura ou observação de correspondência de SARS-CoV-2 com pontos de corte para positividade de RT-PCR. Foram incluídos 25 estudos que relataram cultura ou invasão de tecido por SARS-CoV em escarro naso ou orofaringe, urina, fezes, sangue e amostras ambientais de pacientes com diagnóstico de COVID-19. A amplificação da sequência genômica do vírus no RT-PCR é medida pelo limite de ciclos (Ct). Os dados sugerem uma relação entre o momento desde a coleta da amostra até o teste de RT-PCR, o valor limite de ciclos e a gravidade dos sintomas. Quanto menor o valor limite de ciclos e o tempo desde o início dos sintomas, maior o potencial de infecção. A duração da liberação de RNA detectada por PCR foi muito maior em comparação com a detecção de cultura viva. Seis em oito estudos relataram liberação de RNA por mais de 14 dias. No entanto, a capacidade de infecção diminui após o dia 8, mesmo entre os casos com altas cargas virais em curso. Uma proporção muito pequena de pessoas com novo teste positivo após a alta hospitalar ou com Ct alto são provavelmente infecciosas. Os testes de rotina prospectivos de amostras de referência e de cultura são necessários para cada país envolvido na pandemia para estabelecer a utilidade e confiabilidade do PCR para diagnóstico da COVID-19 e sua relação com o estado dos pacientes. A infecciosidade está relacionada à data de início dos sintomas e ao valor limite de ciclos. Uma abordagem binária “Sim/Não” para a interpretação do resultado do RT-PCR não validado contra cultura viral resultará em falsos positivos com segregação de um grande número de pessoas que não são mais infecciosas e, portanto, não são uma ameaça à saúde pública (03/09/2020). Fonte: Medrxiv.
16/09/2020
Revisão dos métodos disponíveis para a detecção de infecções virais em humanos. São discutidas as técnicas de diagnóstico molecular, técnicas de base imunológica entre outros tipos de técnicas (04/09/2020). Fonte: International Journal of Microbiology
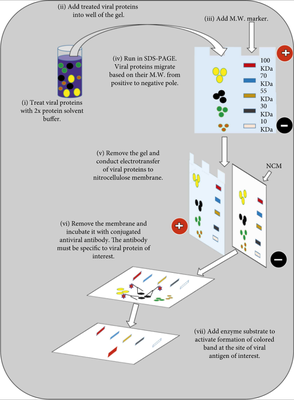
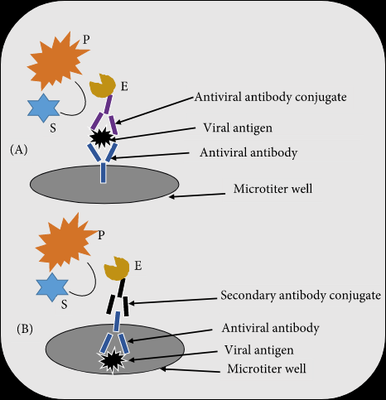
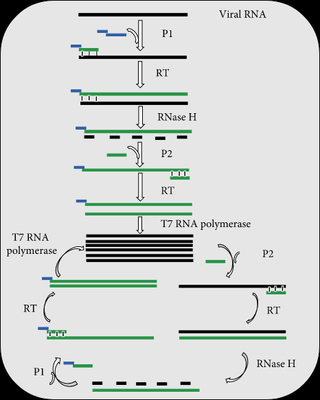
15/09/2020
Artigo oferece uma abordagem para o teste de anticorpos em indivíduos com e sem sintomas sugestivos de infecção por SARS-CoV-2 (08/09/2020). Fonte: BMJ
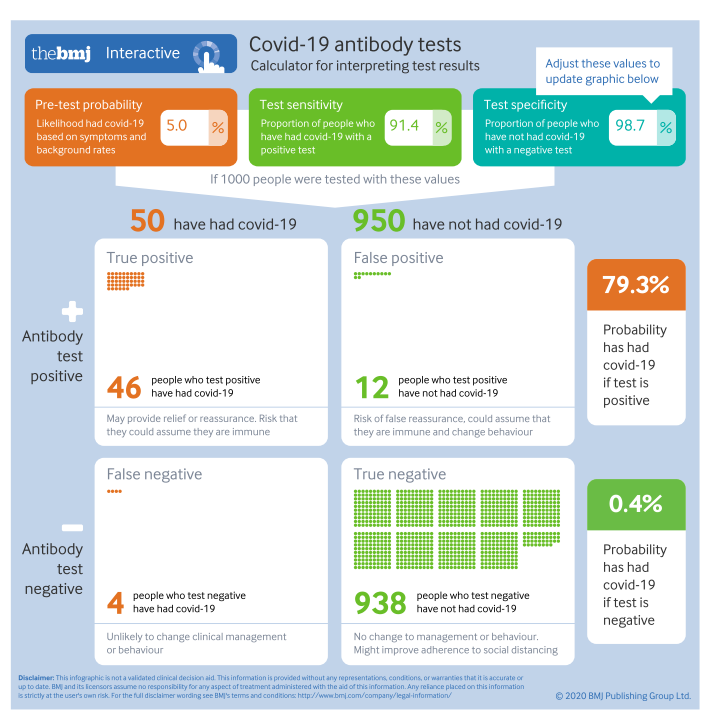
14/09/2020
As práticas padrão para a triagem rápida de risco de COVID-19 são as imagens de TC ou RT-PCR. No entanto, esses métodos exigem esforços de profissionais na aquisição de imagens de tomografia computadorizada e amostras de saliva, certo tempo de espera além de taxas de exame proibitivas em alguns países. Recentemente, alguns estudos têm mostrado que os pacientes com COVID-19 geralmente são acompanhados por manifestações oculares consistentes com a conjuntivite, incluindo hiperemia conjuntival, quemose, epífora ou aumento de secreções. Após mais de quatro meses de estudo, foi descoberto que os casos confirmados de COVID-19 apresentam símbolos patológicos oculares consistentes. Neste estudo os autores sugerem um novo método de triagem para analisar as imagens da região do olho, capturadas por câmeras CCD e CMOS comuns, que fazem uma triagem de risco rápida de COVID-19 com precisão muito alta. Para avaliar melhor o algoritmo foi conduzido um estudo de análise das imagens da região ocular de 303 pacientes (104 COVID-19, 131 pulmonares e 68 pacientes oculares), bem como 136 pessoas saudáveis. Notavelmente, os resultados de pacientes COVID-19 apresentam consistentemente símbolos patológicos oculares semelhantes; e resultados de teste muito altos foram alcançados em termos de sensibilidade e especificidade (10/09/2020). Fonte: MedRXiv
Mais de 300 testes sorológicos SARS-COV-2 foram desenvolvidos recentemente usando a fosfoproteína do nucleocapsídeo (N), a subunidade da glicoproteína spike (S1) e, mais recentemente, o domínio de ligação ao receptor (RBD). A maioria dos ensaios relata características de desempenho clínico muito boas em ambientes clínicos bem controlados. No entanto, acredita-se que as boas características de desempenho obtidas durante os ensaios de desempenho clínico podem não ser suficientes para fornecer bons resultados diagnósticos quando feitos de forma ampla na população, que geralmente é caracterizada por ter baixa soroprevalência. Neste artigo, desenvolvemos um ensaio sorológico contra N, S1 e RBD usando uma plataforma multiplex. Mesmo que os ensaios baseados em leituras de antígeno único tenham um desempenho semelhante nas amostras clínicas, houve uma diferença notável entre os antígenos quando analisada a população. Indivíduos assintomáticos com baixos títulos de anticorpos e especificidade de ensaio subótima podem contribuir para as grandes discrepâncias em estudos populacionais com baixa soroprevalência. Um ensaio multi-antígeno que requer acordo parcial entre as leituras de RBD, N e S1 exibiu especificidade aprimorada, menos dependência dos valores de corte do ensaio e um desempenho geral mais robusto (10/09/2020). Fonte: MedRXiv
11/09/2020
Estudo compara oito ensaios comerciais (Abbott Architect, DiaSorin Liaison®, bioMérieux Vidas®, Roche Elecsys Cobas®, Siemens Atellica®, BioRad Platelia ELISA, Epitope Diagnostics ELISA e Wantai ELISA), de alto rendimento, automatizados ou ELISA que detectam SARS-CoV-2 IgG ou anticorpo total. A população testada incluiu 86 amostras de 40 indivíduos hospitalizados e 28 pacientes ambulatoriais em momentos diferentes do início dos sintomas. A taxa de positividade variou dependendo do ensaio, mas foi maior para todos os ensaios em pacientes hospitalizados do que em não hospitalizados. Apesar de uma boa correlação entre os ensaios, ocorreram discrepâncias, sem origem sistemática, mesmo para amostras colhidas mais de 20 dias após o início dos sintomas. Segundo os pesquisadores, qualquer que seja o ensaio escolhido, um resultado falso negativo pode precisar ser descartado com outro teste em uma situação de risco (07/09/2020). Fonte: Journal of Clinical Virology
10/09/2020
Estudo faz uma avaliação do teste de imunoensaio IgG da Abbott SARS-CoV-2 IgG. A especificidade do ensaio foi de 99,8% e a sensibilidade foi de 45,9-96,7%. O ensaio Abbott SARS-CoV-2 IgG mostra excelente desempenho em pacientes ≥14 dias após (08/09/2020). Fonte: Clinica Chimica Acta
Artigo compara cinco reagentes RT-qPCR com o kit SuperScript ™ III Platinum ™ qRT-PCR de uma etapa (Invitrogen) considerado como o de referência na França no início da pandemia para detecção do SARS-CoV-2 em amostras respiratórias usando ensaio desenvolvido em laboratório visando o gene viral RNA polimerase dependente de RNA (RdRp). As percentagens de concordância foram todas acima de 95% para os cinco reagentes podem ser considerados como reagentes alternativos à referência para a detecção de RNA SARS-COV-2 (08/09/2020). Fonte: Journal of Clinical Virology
Estudo compara os testes de PCR e sorologia através de um ensaio Single Molecule Array (Simoa) para detectar quantitativamente a proteína S de SARS-CoV-2, subunidade S1 e antígenos de nucleocapsídeo no plasma de pacientes com COVID-19. Dos resultados os antígenos SARS-CoV-2 S1 e N foram detectados em 41 de 64 pacientes COVID-19 positivos. O ensaio de antígeno Simoa SARS-CoV-2 relatado é o primeiro a detectar antígenos virais no plasma de pacientes COVID-19 positivos até o momento. Esses dados mostram que os antígenos virais SARS-CoV-2 no sangue estão associados à progressão da doença, como insuficiência respiratória (08/09/2020). Fonte: Clinical Chemistry
Artigo descreve teste rápido e quantitativo para detecção de IgG em soro de pacientes convalescentes da COVID-19. Considerando que o soro convalescente com alta abundância de IgG neutralizante é um agente terapêutico promissor para a recuperação de pacientes com COVID-19 em estágio crítico, saber a concentração de IgG específico para SARS-CoV-2 S1 é crucial na seleção de doadores de soro convalescentes apropriados. Estudo apresenta um teste de ELISA microfluídica portátil para detecção rápida (15 min), quantitativa e sensível de IgG anti-SARS-CoV-2 S1 em soro humano com apenas 8 μL de volume de amostra. Foi demonstrado que a tecnologia pode detectar com sensibilidade antígenos SARS-CoV-2 (proteínas S1 e N) com níveis de sensibilidade pg / mL em 40 min, facilitando a análise rápida, sensível e quantitativa de marcadores relacionados ao COVID-19 para fins terapêuticos, diagnósticos, epidemiológicos e prognósticos (In press). Fonte: Biosensors and Bioelectronics
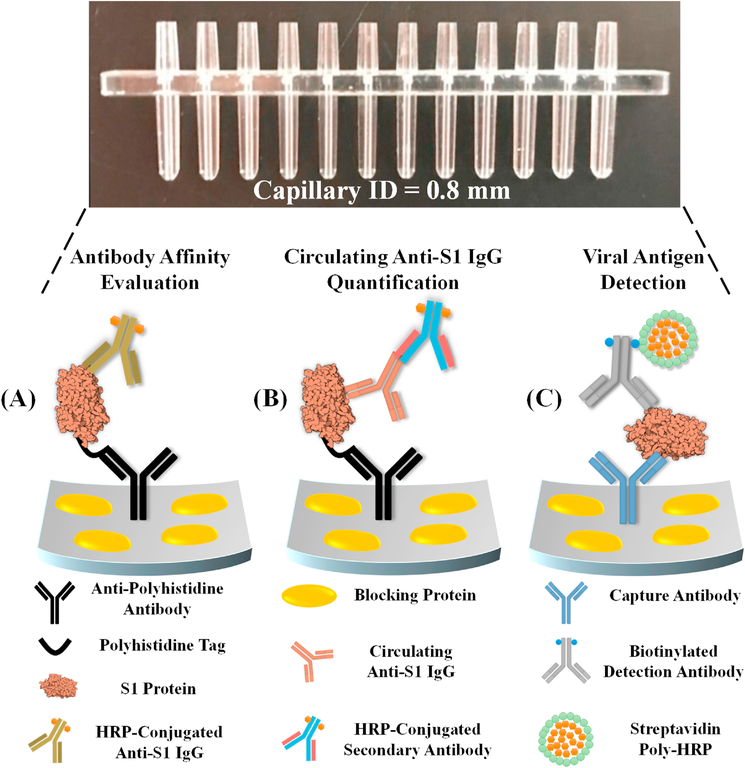
09/09/2020
Artigo faz uma revisão sobre a acurácia dos testes de PCR para o diagnóstico da COVID-19 através da análise de vários estudos científicos. Os autores concluíram que a acurácia do teste de PCR para o diagnóstico do coronavírus pode mudar de acordo com a prevalência da doença, por exemplo; (i) com prevalência de 50%, comum entre profissionais de saúde com sintomáticos respiratórios, encontramos probabilidade pós-teste de 96%, (ii) com prevalência de 20%, a probabilidade pós-teste foi de 84%; e (iii) com uma prevalência de 5%, existe uma probabilidade pós-teste de 55%, e sugerem que quando houver incerteza quanto ao diagnóstico, uma segunda coleta de amostra pode ser indicada para confirmação do diagnóstico (24/08/2020). Fonte: Rev. Assoc. Med. Bras.
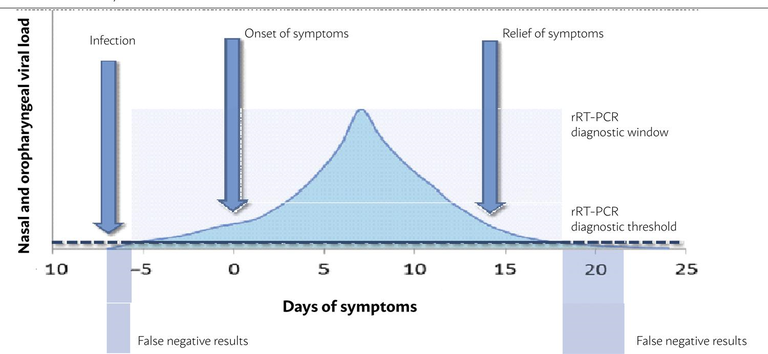
Pesquisadores fornecem e validam uma detecção de RNA de SARS-CoV-2 rápida, conveniente e eficiente, denominada COVID-quick-DET. Este método direto opera com tratamento simples de proteinase K e etapas de aquecimento repetitivas com uma sensibilidade de 94,6% em comparações com métodos de isolamento baseados em kit. Este resultado é apoiado por dados obtidos de estoques de vírus SARS-CoV-2 diluídos em série. Dada a sua operação econômica, o COVID-quick-DET é adequado para países com escassez geral ou escassez aguda temporária de recursos e equipamentos (03/09/2020). Fonte: Journal of Virological Methods
08/09/2020
Estudo tem por objetivo validar a utilização da saliva como amostra biológica para o diagnóstico de COVID-19. Participaram do teste 155 indivíduos em que amostras de pares de NPS/OPS e saliva foram coletadas. A sensibilidade e especificidade do RT-PCR usando amostras de saliva foram 94,4% e 97,62%, respectivamente. Houve alta concordância geral (96,1%) entre os dois testes. O uso de amostras de saliva coletadas pela própria pessoa é uma alternativa fácil, conveniente e de baixo custo aos testes moleculares convencionais baseados em swab. Esses resultados podem permitir um uso mais amplo de testes moleculares para o manejo da pandemia de COVID-19, especialmente em ambientes com recursos limitados (31/08/2020) Uncorrected Proof. Fonte: The Brazilian Journal of Infectious Diseases
04/09/2020
A escassez de conhecimento sobre a dinâmica da resposta imune à infecção levou à hesitação em recomendar o uso de testes de imunodiagnóstico rápidos, embora os testes de sorologia rápida estejam comercialmente disponíveis e sejam escaláveis. Artigo discorre sobre a resposta imunológica frente à COVID-19, discute os prós e contras dos testes sorológicos e as estratégias ideais de testagem (17/07/2020). Fonte: The Lancet Infectious Diseases
Neste estudo procurou utilizar o princípio da ressonância de plasmon de superfície localizada (LSPR) para desenvolver uma plataforma de detecção opto-microfluídica com nanopontos de ouro, fabricados por eletrodeposição, para detectar a presença e quantidade de anticorpos específicos para a proteína S do SARS-CoV-2. Os autores demonstram que a plataforma opto-microfluídica oferece uma ferramenta de teste de ponto de atendimento promissora para complementar os ensaios sorológicos padrão e tornar o diagnóstico quantitativo de SARS-CoV-2 mais fácil, barato e rápido (03/09/2020). Fonte: Biosensors and Bioeletronics

03/09/2020
Anunciada a competição COVID-19 XPRIZE, OpenCovidScreen (https://opencovidscreen.org/), para identificar opções de teste economicamente viáveis, de alta qualidade e escaláveis. Primeiramente os competidores serão selecionados com base em seus resultados, métodos, custo, escalabilidade e velocidade do teste. Depois serão enviadas a eles amostras cegas para analisar. Os resultados serão enviados para o site XPRIZE e analisados em função do desempenho geral, limite de detecção (LoD) e falsos positivos. Os finalistas, irão para a rodada de validação clínica, na qual o OpenCovidScreen seguirá os métodos estabelecidos pelos concorrentes para avaliar a reprodutibilidade de seus resultados. As melhores equipes desta rodada de validação receberão um prêmio e serão selecionadas para configurar e implantar sites de teste, onde o OpenCovidScreen ajudará a escalar seus testes e expandi-los para mais locais, bem como para coordenar com esforços governamentais, industriais e sem fins lucrativos. A competição é aberta a participante de todo o mundo(https://xprize.org/testing) (20/08/2020). Fonte: Nature Biotechnology

Artigo relata a validação clínica do teste por desbloqueio enzimático específico de alta sensibilidade (SHERLOCK) utilizando a enzima Cas13a da Leptotrichia wadei para a detecção do SARS-CoV-2 em 154 amostras de swab nasofaríngeo e garganta coletadas no Hospital Siriraj, Tailândia. Dentro de um limite de detecção de 42 cópias de RNA por reação, SHERLOCK se mostrou 100% específico e 100% sensível com a leitura de fluorescência, 100% específico e 97% sensível com a leitura de fluxo lateral. Para toda a gama de carga viral nas amostras clínicas, a leitura da fluorescência foi 100% específica e 96% sensível. Para 380 amostras pré-operatórias negativas para SARS-CoV-2 de pacientes submetidos à cirurgia, SHERLOCK estava 100% de acordo com RT-PCR. O ensaio, deve facilitar a detecção do SARS-CoV-2 em configurações com recursos limitados (26/08/2020). Fonte: Nature Biomedical Engineering
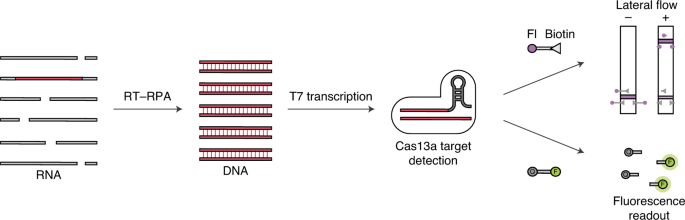
Um estudo com ensaio sorológico à base da ligação Luminex foi desenvolvido e usado para avaliar simultaneamente a presença de anticorpos específicos de COVID-19 em soro e plasma humanos. A diferenciação clara foi alcançada entre as 25 amostras de indivíduos infectados e não infectados, e uma ampla gama de níveis de anticorpos séricos / plasmáticos foi delineada em indivíduos infectados. Todas as amostras de pacientes com COVID-19 foram positivas nos ensaios com ambas as proteínas, o pico trimérico e o domínio de ligação ao receptor. Nenhuma das amostras de indivíduos não infectados apresentou anticorpos para qualquer um dos antígenos. Houve uma diferença estatistica significativa entre os níveis de anticorpos das amostras infectadas com COVID-19 e não infectadas. O ensaio de anticorpos tem alto rendimento, é preciso, requer apenas 2,5 horas para o resultado e usa 5 nanogramas de antígeno por teste (29/08/2020). Fonte: The Journal of Infectious Diseases
A crescente demanda por rastreamento rápido e identificação de COVID-19 fez os autores desenvolverem um diagnóstico isotérmico baseado em CRISPR para COVID-19 com sensibilidade quase de cópia única. Os desempenhos de diagnóstico de todas as três plataformas de tecnologia foram comparados e o CRISPR-COVID demonstrou um alto nível de sensibilidade e foi altamente específico sem reação cruzada com patógenos relacionados levando apenas 40 minutos e não requerendo termocicladores sofisticados, fornecendo uma alternativa valiosa para o ensaio RT-PCR convencional (27/08/2020). Fonte: Plos Pathogens
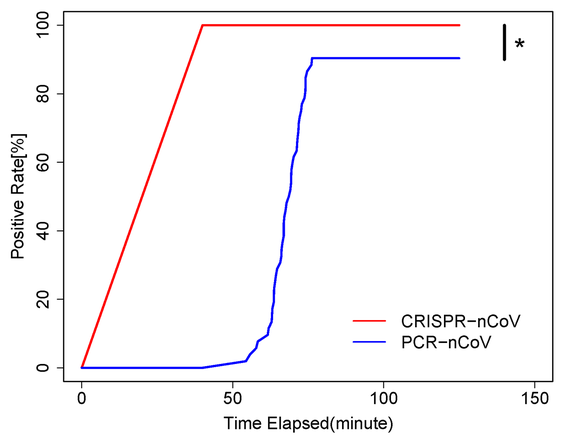
Estudo de validação de ensaios diagnósticos Vitros ANTI-SARS-CoV-2(COV2T) frente aos testes sorológicos quantitativos de anticorpos SARS-CoV-2. Foi usado amostras previamente testadas para SARS-CoV-2 por transcrição reversa-reação em cadeia da polimerase (RT-PCR). O ensaio Vitros CoV2T exibiu precisão aceitável e não exibiu reatividade cruzada com outras infecções virais respiratórias agudas. O ensaio CoV2T exibiu 100% de concordância preditiva negativa e 71% de concordância preditiva positiva com RT-PCR em todas as amostras de pacientes e foi concordante com outros testes sorológicos (31/08/2020). Fonte: Oxford Academic
A empresa norte-americana Abbott Laboratories divulgou na semana passada um novo teste para o coronavírus que mostra resultados em apenas 15 minutos, inclusive já recebeu a autorização de uso da FDA. O novo teste custa U$5 é muito parecido com o PCR tradicional e envolve um swab nasal que segundo a Abbott, tem precisão de 97,1% em caso de resultado positivo e 98,5% em caso negativo. A empresa também lançou um aplicativo que é sincronizado com o teste e para os casos negativos, o app fornece um “passe digital de saúde”, que poderia ser utilizado para a entrada dos viajantes nos países. (31/08/2020). Fonte: Isto é
28/08/2020
Artigo descreve o impacto da implementação de testes de RT-PCR de SARS-CoV-2 em ambiente hospitalar na redução do tempo de retorno do resultado, duração do isolamento, pedido de teste de patologia e uso de antibióticos em pacientes que não têm COVID-19. Os autores concluem que com a pandemia de COVID-19 em andamento, suas descobertas apóiam os benefícios do estabelecimento mais rápido de testes de RT-PCR SARS-CoV-2 no in loco em centros capazes de fazê-lo (24/08/2020). Fonte: Infection Control & Hospital Epidemiology (Cambridge Coronavirus Collection)
Artigo descreve os vários métodos de diagnóstico para COVID-19 descrevendo as limitações e nuances. Entre todas as tecnologias convencionais, o RT-PCR em tempo real fornece uma identificação rápida e confiável da infecção por SARS-CoV-2, mas não é tão barato. O teste sorológico permite monitorar a resposta imunológica do paciente e revela a imunidade da população , mas não é recomendado para a identificação da infecção atual por SARS-CoV-2. No futuro, o diagnóstico molecular ainda será o método padrão ouro para o diagnóstico de COVID-19 (26/08/2020). Fonte: Expert Review of Molecular Diagnostics
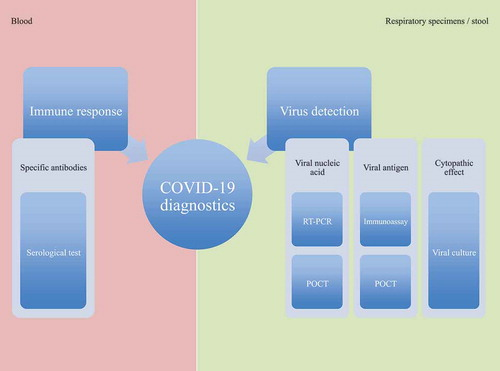
27/08/2020
Cientistas da Universidade de Ciência e Tecnologia da China desenvolveram uma matriz de sensores baseados em nanomateriais que pode detectar a presença do vírus na respiração exalada, como um “bafômetro”. O método se baseia em compostos orgânicos voláteis (VOCs) emitidos na presença do coronavirus e sua reação com sensores de nanoparticulas de ouro. Através de machine learning foi possível determinar uma “assinatura” para o coronavirus. O dispositivo mostrou 76% de precisão em distinguir casos da COVID-19 de pessoas saudáveis e 95% de acurácia em discriminar casos da COVID-19 de outras infecções pulmonares. Além disso, esse sensor pode distinguir, com precisão de 88%, a diferença entre pacientes com a COVID-19 e os casos recuperados (18/08/2020). Fonte: ACS Nano
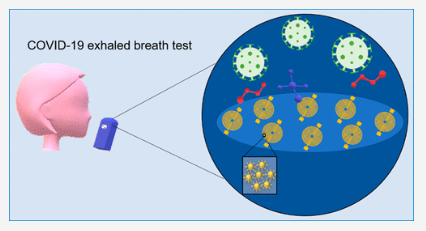
26/08/2020
Pesquisadores da UFRJ desenvolveram um teste diagnóstico tipo ELISA, denominado teste S-UFRJ. A proteína SARS-COV-2 spike (S) trimérica foi produzida em células HEK293 adaptadas a suspensão, sem soro. Dos resultados obteve-se 99% de especificidade, com sensibilidade de >90% para amostras acima de 10 dias de início dos sintomas e de 100% para amostras com mais de 20 dias do início dos sintomas. O diferencial deste teste encontra-se no fato de que de que pode ser realizado com diferentes tipos de amostras: (i) plasma ou soro de sangue venoso; (ii) manchas de sangue seco de gotas de sangue coletadas por picada no dedo (02/08/2020). Fonte: medRxiv
25/08/2020
Artigo demonstra que um biomarcador de diagnóstico de gravidade altamente confiável, a proteína induzida por fator de transformação de crescimento beta de 676 lisina acetilada (TGFBIp K676Ac) foi consistentemente elevado no sangue de pacientes com pneumonia por SARS-CoV-2 especialmente em pacientes na unidade de terapia intensiva (UTI) em comparação com pacientes não-UTI sugerindo que está proteína pode ser uma promessa de biomarcador confiável para COVID-19 grave (31/07/2020). Fonte: Science Advances
24/08/2020
Um lote piloto do kit sorológico IgG para COVID-19, teste para detecção do novo coronavírus baseado no método ELISA, acaba de ser concluído pelo Centro Tecnológico de Vacinas da UFMG que conta com a parceria de pesquisadores da Fiocruz e de Bio-Manguinhos. Os protótipos do kit prontos, serão submetidos a experimentos fora do ambiente do laboratório da Fiocruz e enviadas amostras para a Anvisa. Após a submissão do protótipo a testes e aprovação da Anvisa, o produto poderá ser produzido em larga escala, e serão estudadas parcerias com órgãos de distribuição não comerciais (24/08/2020). Fonte: UFMG
21/08/2020
Estudo investiga a estabilidade do RNA do SARS-CoV-2 e a detecção do vírus infeccioso na saliva sem suplementação. Testou-se a estabilidade do RNA por longos períodos de tempo (2-25 dias) e em temperaturas que representam o armazenamento em casa e temperaturas elevadas que podem ocorrer quando o transporte da cadeia de frio pode não estar disponível. Descobriu-se que o RNA do SARS-CoV-2 na saliva de indivíduos infectados é estável a 4 ° C, à temperatura ambiente (~ 19 ° C) e a 30°C por períodos prolongados, com evidências limitadas de replicação viral na saliva. Este trabalho demonstra que opções caras de coleta de saliva envolvendo estabilização de RNA e buffers de inativação de vírus nem sempre são necessárias, permitindo o uso de opções de coleta mais baratas e o desenvolvimento de testes mais acessíveis (04/08/2020). Fonte: medRxiv
20/08/2020
Estudo com 58 pacientes com pneumonia advinda da COVID-19 após 8 a 12 dias do início dos sintomas e 12 pacientes controles saudáveis foram analisados para detecção do SARS-CoV-2 no plasma através de PCR digital baseada em gotículas a fim de obter detecção sensível e precisa da carga viral plasmática. Dos resultados de SARS-CoV-2 RNAemia foi detectada em 74,1% pacientes. E a prevalência de SARS-CoV-2 RNAaemia positiva correlacionada com a gravidade da doença, variou de 53% em pacientes leves a moderados e a 88% em pacientes críticos (17/08/2020). Fonte: Clinical Infections Diseases
Estudo investiga o impacto potencial de diferentes testes de diagnóstico e estratégias de isolamento na transmissão do coronavírus (SARS-CoV-2). Autores desenvolveram um modelo matemático de transmissão de SARS-CoV-2 com base na infecciosidade e na sensibilidade do teste de PCR ao longo do tempo desde a infecção, estimaram a redução no número de reprodução efetiva (R) alcançada por meio de testes e isolamento de indivíduos sintomáticos, triagem regular de grupos de alto risco independentemente dos sintomas e quarentena de contatos de casos confirmados por laboratório identificados por meio de protocolos de teste e rastreamento (18/08/2020). Fonte: The Lancet
Pesquisadores brasileiros lideram estudos sobre como marcadores no sangue podem prever a gravidade da COVID-19 e, assim, auxiliam no desenvolvimento e melhoria de tratamentos e prognósticos de pacientes infectados (19/08/2020). Fonte: National Geographic
Sensores eletroquímicos de DNA / RNA versáteis são uma alternativa tecnológica promissora ao diagnóstico baseado em PCR. Em um sensor eletroquímico de DNA, um evento de hibridização de ácido nucleico é convertido em um sinal eletroquímico quantificável. Um desafio crítico dos sensores eletroquímicos de DNA é a detecção sensível de um baixo número de cópias de DNA / RNA em amostras, como é o caso do início precoce da doença. As abordagens de amplificação de sinal são uma ferramenta importante para superar esse problema de sensibilidade. Nesta revisão, os autores discutem as mais recentes estratégias de amplificação de sinal empregadas no diagnóstico eletroquímico de DNA / RNA de patógenos. Fonte: Sensors
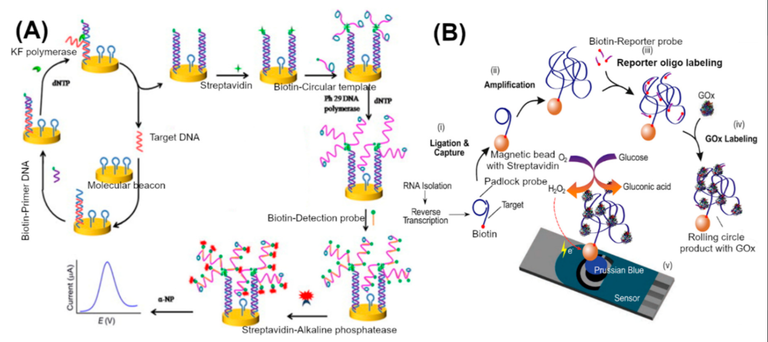
19/08/2020
Pesquisadores relatam o desempenho de um imunoensaio quimioluminescente automatizado (CLIA) em 276 amostras de soro. 100 amostras obtidas de indivíduos negativos para COVID‐19 foram analisadas para avaliar a especificidade diagnóstica da detecção de anticorpos (Ab). Posteriormente, 125 amostras obtidas pacientes com COVID-19 confirmado foram selecionadas para avaliar a sensibilidade diagnóstica do CLIA. No 18º dia desde o início dos sintomas, alcançou-se uma sensibilidade diagnóstica ideal (mais de 95,0%), que aumentou ao longo do tempo e entre 15 a 25 dias após o início dos sintomas e atingiu 95,5%. O novo analisador CLIA automatizado é um método robusto e confiável para medir Ab específico contra COVID-19 em um alto rendimento, porém os dados sugerem que a combinação de Ab e detecção de ácido nucleico pode aumentar a sensibilidade diagnóstica (14/08/2020). Fonte: Journal of Medical Virology
18/08/2020
A criação de dispositivo inédito, capaz de realizar teste para diagnóstico da COVID-19 com o uso de um aparelho celular está em desenvolvimento no Instituto de Ciências Biológicas (ICB) e nas escolas de Engenharia e Veterinária da UFMG. A ideia é que seja um teste rápido, portátil, de menor custo e, principalmente, preciso para o diagnóstico da COVID-19, por meio da detecção de partícula viral na secreção das vias respiratórias do paciente. O processo é simples, tem-se a coleta do material, que deve ser feita por profissional treinado, com a técnica do swab, após a coleta da secreção das vias aéreas, o material é colocado sobre um dispositivo, que visualmente se assemelha às lâminas utilizadas atualmente nos testes rápidos para COVID-19, contendo moléculas para capturar o vírus. A revelação do diagnóstico fica vinculada à presença dessas moléculas. E é nessa etapa que será desenvolvida pelos pesquisadores da UFMG: são nanossensores oticamente ativados pela luz LED do aparelho celular. O celular será usado para captura, processamento e análise dos dados do exame. As imagens capturadas serão tratadas, no próprio celular, por aplicativo de imagem que converte rapidamente (de 1 a 5 minutos) uma informação obtida em resultado final, que aparece no visor do aparelho, resultado qualitativo (positivo e negativo) e também semiquantitativo de covid-19 (nível baixo, médio ou alto de infecção viral) (18/08/2020). Fonte: UFMG

Pesquisadores desenvolveram e avaliaram um ELISA para a detecção das classes de imunoglobulinas A, G e M dirigidas contra a glicoproteína S do SARS-CoV-2. Para esta análise, incluíram 110 soros de pacientes com sintomas de COVID-19 ou de doadores de sangue sem sintomas. Além disso, os resultados foram comparados com quatro ELISAs baseados em IgG comercialmente disponíveis, com um ELISA baseado em IgA / IgG e com um ensaio micro-ELISA baseado em IgG multiplexado. Todos os ensaios avaliados no decorrer deste estudo demonstraram valores adequados de sensibilidade e especificidade para a identificação de pacientes que tiveram uma infecção anterior com SARS-CoV-2 (11/08/2020). Fonte: Journal of Clinical Virology
Artigo resume os principais achados clínicos e de imagem dos pacientes de COVID-19 e discute os avanços, características, vantagens e limitações de diferentes métodos laboratoriais utilizados para o diagnóstico SARS-Cov-2(04/08/2020). Fonte: ACS infectious diseases
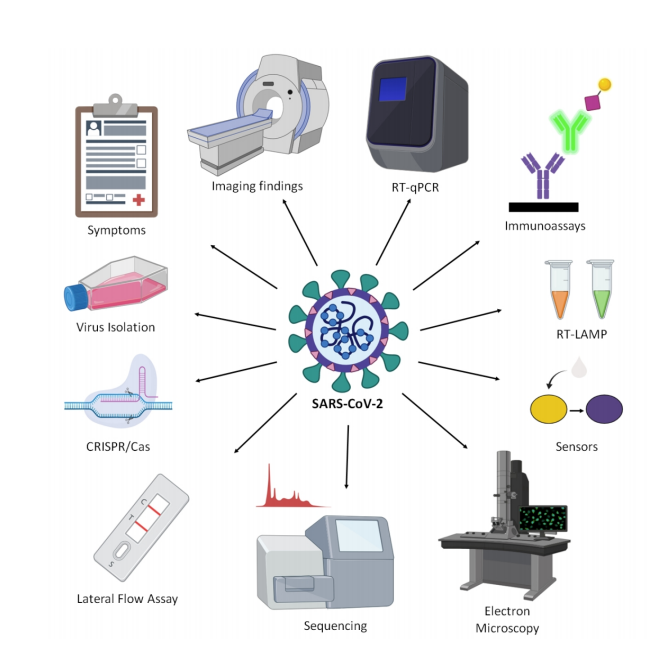
A artigo identifica os anticorpos IgA para SARS-CoV-2 em uma população IgM soronegativo. A partir dos resultados estudo os autores recomendam a inclusão da determinação dos anticorpos IgA entre os testes sorológicos do diagnóstico COVID-19 podendo os mesmos ajudar a fechar a lacuna sorológica da COVID-19 (13/08/2020). Fonte: Journal of medical virology
17/08/2020
Nos Estados Unidos da América, grupo de profissionais, liderado por um epidemiologista, defende que, antes do desenvolvimento da vacina, a pandemia pode ser controlada através de testes de diagnóstico que deveriam ser inseridos no dia-a-dia da vida dos americanos. Através de um teste barato e de baixa sensibilidade que consiste em uma tira de papel fina que fornece o resultado em 15 minutos, dezenas de milhões por dia poderiam ser testadas. Antes que se entre em qualquer espaço público, o indivíduo deveria ser testado, sendo liberada a entrada somente para àqueles com teste negativo. A proposta é que quase todos sejam testados quase todos os dias (14/08/2020). Fonte: The Atlantic
Artigo de comentário onde o autor aborda diversas áreas de debate sobre testes diagnósticos, incluindo 1) o papel dos ensaios moleculares na definição da duração do isolamento/quarentena, 2) se o valor do limiar do ciclo PCR deve ser incluído nos relatórios dos pacientes, 3) se a junção de espécimes e testes por equipe de pesquisa representam soluções aceitáveis para expandir a triagem, e 4) se o teste de uma grande porcentagem da população é viável e representa uma estratégia viável para acabar com a pandemia. Na opinião dos autores é improvável que uma estratégia de "testar todos" seja viável e impedirá o acesso à recursos limitados aos que mais precisam de testes. Os testes devem ser priorizados para as situações em que o resultado informará a gestão do paciente, o uso de equipamentos de proteção individual e as decisões de isolamento (12/08/2020). Fonte: Journal of Clinical Microbiology
Pesquisadores da Universidade de Oxford desenvolveram um teste de diagnostico que ao invés de usar a plataforma de reação em cadeia da polimerase (PCR), o teste usa amplificação mediada por loop de transcrição reversa (RT-LAMP) para detectar RNA viral. A Universidade de Oxford superou enormes desafios para desenvolver RT-LAMP em um método robusto, sensível, específico e confiável para detectar SARS-CoV-2 e eliminar o problema comum de falso positivo e reações não específicas. Os kits são formulados de forma que possam ser armazenados e fornecidos sem refrigeração e em um formato de produto econômico e prontamente distribuível em quantidade (17/08/2020). Fonte: University of Oxford
Estudo avaliou o teste “Abbott SARS-CoV-2 IgG” para detecção de anticorpos anti-SARS-CoV-2 IgG testando 3 populações distintas de pacientes. Foram testadas 1.020 amostras de soro coletadas antes da circulação do SARS-CoV-2 nos Estados Unidos e encontrou-se um falso positivo, indicando uma especificidade de 99,90%. Foram testados 125 pacientes com teste de RT-PCR positivo para SARS-CoV-2 e a sensibilidade atingiu 100% no dia 17 após o início dos sintomas e no dia 13 após a positividade da PCR (23/07/2020). Fonte: Journal of Clinical Microbiology
13/08/2020
Estudo avaliou ensaio sorológico baseado no Imunoensaio de Micropartículas de Quimioluminescência (CMIA) para detecção de anticorpos contra SARS-CoV-2. Em 206 pacientes com infecção confirmada por SARS-CoV-2 foram inscritos para investigar o valor diagnóstico de CMIA. Também avaliaram a variação dinâmica de IgM e Ab e os fatores de influência da produção de anticorpos. Dos resultados verificou que a sensibilidade do Ab (90,8%) foi significativamente maior do que a do IgM (72,3%) (30/07/2020). Fonte: Journal of Clinical Virology
Estudo sinaliza que a detecção do SARS-CoV-2 pela saliva parece ser muito promissora, embora obstáculos como a técnica e o local da coleta e o tamanho da amostra das pesquisas realizadas até o momento possam apresentar uma limitação para seu uso (07/08/2020). Fonte: Pesquisa Brasileira em Odontopediatria e Clínica Integrada
Autores avaliaram seis alternativas diferentes de RT-qPCR para o diagnóstico de SARS-CoV-2 / COVID-19 com base em extrações de RNA padrão. Uma grande variabilidade na sensibilidade das soluções de RT-qPCR associadas a uma gama de falsos negativos de 2% a até 39,8% foi encontrada, evidenciando limitações de sensibilidade das soluções RT-qPCR utilizadas atualmente. Os resultados ajudarão a calibrar o impacto de diagnósticos falsos negativos de COVID-19 e a detectar e controlar novos surtos de SARS-CoV-2 e transmissões comunitárias (01/08/2020). Fonte International Journal of Infectious Diseases
11/08/2020
Estudo da USP apresenta método mais simples e barato de PCR para detectar o novo coronavirus sem perder a confiabilidade. Pesquisadores calculam que cada teste custaria até R$15, enquanto a testagem padrão-ouro custa R$70. Existem diversas formas de PCR, e o método que acabou se tornando o padrão desde os primeiros meses de pandemia é o da RT-qPCR em tempo real, que exige insumos que não são fabricados no Brasil, aparelhos caros e pessoal treinado, pré-requisitos raros. A abordagem não mostrou grandes diferenças de precisão em relação à forma mais sofisticada de PCR. Os pesquisadores da USP também desenvolveram outro formato de teste, baseado na detecção de anticorpos que o organismo produz contra o SARS-CoV-2, com custo estimado de R$ 20 para cada testagem, a análise de anticorpos foi validada a partir de amostras de 934 pessoas, das quais 9,3% apresentaram sinais de ter desenvolvido imunidade (10/08/2020). Fonte: Folha de São Paulo
O surgimento de SARS-CoV-2 em áreas endêmicas do vírus da dengue (DENV) complica o diagnóstico de ambas as infecções. Os casos de COVID-19 podem ser diagnosticados erroneamente como dengue, principalmente quando se trata de DENV IgM, que pode permanecer positivo meses após a infecção. Para estimar a extensão deste problema, avaliamos o soro de 42 pacientes confirmados com COVID-19 para evidências de infecção por DENV. Nenhum caso de coinfecção SARS-CoV-2 e DENV foi identificado. No entanto, infecção recente de DENV, indicada pela presença de DENV IgM e / ou alto nível de anticorpos IgG, foi encontrada em sete pacientes. O vírus da dengue IgM e / ou alto título de IgG não deve excluir COVID-19. O teste RT-PCR do SARS-CoV-2 é apropriado quando a proteína 1 não estrutural da dengue (NS1) ou RT-PCR é negativo. Dada a possibilidade de coinfecção, o teste para DENV e SARS-CoV-2 é merecido no cenário da pandemia atual (05/08/2020). Fonte: The American Journal of Tropical Medicine and Hygiene
O objetivo do estudo foi avaliar a sensibilidade, especificidade e capacidade de uma plataforma de diagnóstico baseada em PCR de alto rendimento em tempo real, totalmente automatizada, de acesso aleatório para a detecção de SARS-CoV-2. O sistema NeuMoDx N96 exibiu uma taxa de detecção igual ou melhor para SARS-CoV-2 em comparação com o sistema LightCycler 480II e apresentou uma especificidade de 100%. O tempo médio de execução de PCR para todas as 28 execuções de PCR foi de 91 (IQR 84–97) minutos. Os autores citam que a capacidade do NeuMoDx N96 pode superar a capacidade da maioria dos sistemas de teste molecular usados atualmente e reduzir significativamente o tempo de rotação (29/07/2020). Fonte: Virulence
Artigo demonstra que as características de desempenho dos ensaios sorológicos COVID-19 foram geralmente inferiores às relatadas pelos fabricantes. O momento da coleta da amostra em relação ao início da doença ou infecção é crucial para relatar as características de desempenho dos ensaios sorológicos COVID-19 (06/08/2020). Fonte: The Journal of Infectious Diseases
10/08/2020
Os autores fazem um comparativo entre os testes disponíveis comercialmente e imunoensaios de laboratório (ensaios de imunoabsorção enzimática ou imunoensaios de quimioluminescência) para SARS-CoV-2 (30/07/2020). Fonte: Journal of Infection
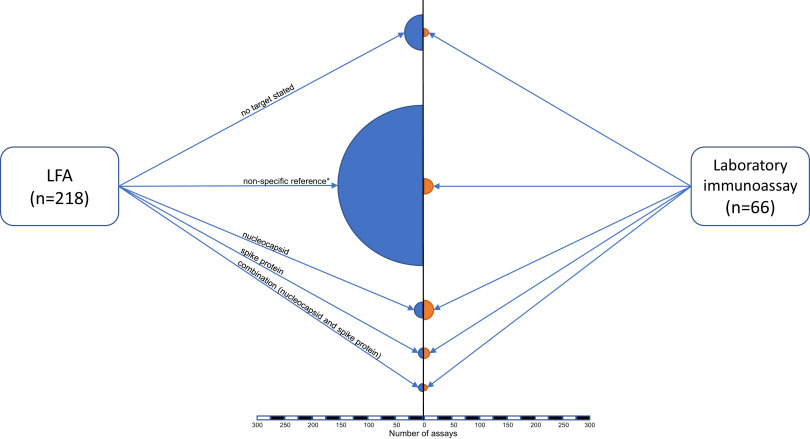
Estudo demonstra que as infecções gastrointestinais são secundárias às infecções pulmonares e, durante o período de recuperação dos pacientes, o vírus pode ainda existir no trato gastrointestinal do paciente por mais de 7 dias. Autores apresentam um método bidirecional transmissão através dos olhos-oral. Ao associar os sintomas da infecção às rotas de transmissão do vírus e ao curso da doença do paciente, ele fornece diretrizes para o diagnóstico clínico e a base para suprimir a disseminação do vírus e o tratamento antiviral (10/07/2020). Fonte: Frontiers in Cell and Developmental Biology

07/08/2020
Os autores apresentam três métodos baseados em deep learning para a detecção e diagnóstico de pacientes COVID-19 com o uso de imagens de raios-X de pulmões. Para o diagnóstico da doença, apresentam dois algoritmos que incluem rede neural profunda (DNN) na característica fractal de imagens e métodos de rede neural convolucional (CNN) com o uso de imagens pulmonares, diretamente. A classificação dos resultados mostra que a arquitetura CNN apresentada com maior acurácia (93,2%) e sensibilidade (96,1%) está superando o método DNN com acurácia de 83,4% e sensibilidade de 86%. No processo de segmentação, apresentam uma arquitetura CNN para encontrar tecido infectado em imagens de pulmão. Os resultados mostram que o método apresentado pode quase detectar regiões infectadas com alta precisão de 83,84%. Esse achado também pode ser usado para monitorar e controlar o crescimento da região infectada em pacientes (07/2020). Fonte: Chaos, Solitons & Fractals
06/08/2020
Estudo compara a resposta imune humoral em pacientes com COVID-19 graves, (hospitalizados) e leves (não hospitalizados). Observou-se que pacientes graves (n = 38) desenvolvem uma resposta robusta de anticorpos para SARS-CoV-2, incluindo anticorpos IgG e IgA. O título médio de neutralização do vírus nestes pacientes é de 1:240, enquanto que os indivíduos infectados com SARS-CoV-2 (n = 24), com sintomas leves que não requerem hospitalização, 75% desenvolvem anticorpos, mas com baixa/ausência de neutralização do vírus (60% <1:20). O monitoramento a longo prazo mostrará se essas respostas geram proteção contra infecções futuras (29/07/200). Fonte: The Journal of Infectious Diseases
05/08/2020
Durante a pandemia COVID-19, os autores detectaram um novo padrão de imunofluorescência (IF) na triagem dos autoanticorpos séricos (autoAb) de pacientes com COVID-19 confirmados laboratorialmente. O padrão IF foi composto de coloração de fígado e mucosa gástrica em seções de rim/fígado/estômago de rato. Foram comparados 12 pacientes positivos para o auto anticorpo sérico com um grupo de 43 pacientes com COVID-19 hospitalizados que testaram negativo para este anticorpo, tendo sido encontrada uma associação entre a presença do auto anticorpo com complicações neurológicas ou trombóticas. Em amostras sequenciais pré e pós-COVID-19, foi confirmada a soroconversão auto Ab indicando que que a triagem automática de pacientes COVID-19 pode ser realizada por IF e alertar para complicações, como eventos trombóticos ou neurológicos (01/08/2020). Fonte: The Journal of Infectious Disease
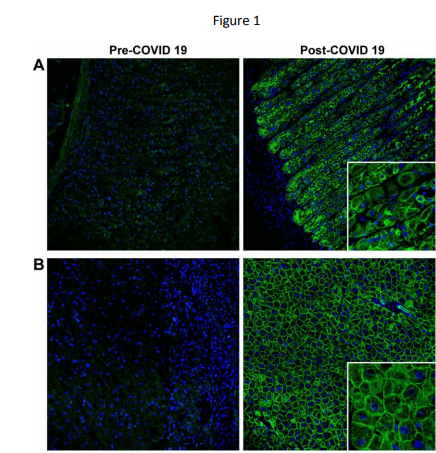
Os autores apresentam duas técnicas de detecção rápida e sensível de anticorpos IgG e IgM específicos para SARS-CoV-2 usando tecnologia Imunocromatográfica de ouro coloidal. O teste de detecção rápida pode ser útil para COVID-19 diagnóstico clínico e vigilância epidemiológica (24/07/2020). Fonte: Chinese medical journal
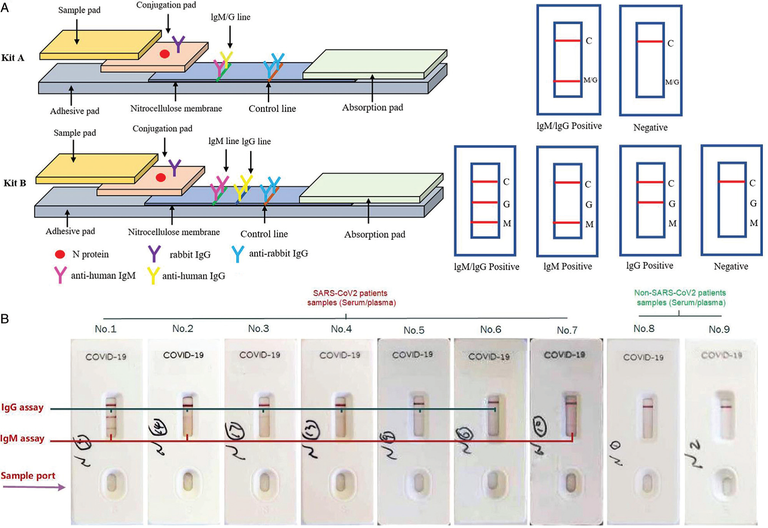
Pesquisadores do Laboratório de Genômica e bioEnergia da Universidade Estadual de Campinas (Unicamp) estão desenvolvendo um novo modelo de teste para diagnóstico da COVID-19, chamado de Coronayeast, que promete ser rápido e barato. A ideia é inserir na levedura um gene que produz a proteína humana ECA-2, substância que facilita a entrada do SARS-CoV-2. Na presença do vírus, após minutos de incubação, a angiotensina 2 passa a ser produzida, hormônio que é identificado por estruturas da levedura. O reconhecimento ativa genes que fazem a levedura ficar vermelha a olho nu e fluorescente. A equipe já pediu a patente da invenção, o que garante exclusividade para explorá-la comercialmente, mas ainda busca financiamento de R$ 500 mil a R$ 1 milhão para levar o produto no mercado em até seis meses (04/08/2020). Fonte: OSul.
04/08/2020
Os autores discutem que os derivados da proteína S são componentes de candidatos a vacina e ensaios de diagnóstico, bem como ferramentas para pesquisa na biologia e imunologia da SARS-CoV-2. Projetam mutações na proteína S que permitem a produção de trímeros de proteína S ligados por dissulfeto e termoestáveis. As estruturas das proteínas estabilizadas com dissulfeto e não dissulfeto revelam conformações fechadas e bloqueadas distintas do trímero S. Demonstram que o trímero S fechado, termostável e projetado pode ser usado em ensaios sorológicos. Esta proteína tem aplicações potenciais como reagente para sorologia, virologia e como imunógeno (31/07/2020). Fonte: Nature Structural & Molecular Biology

Artigo descreve um método para detectar SARS-CoV-2 em cotonetes nasais usando espectrometria de massa de Ionização/Dessorção de Matriz Assistida por Laser (MALDI-MS) e análise de aprendizado de máquina. Esta abordagem utiliza equipamentos e expertises comumente encontradas em laboratórios clínicos em países em desenvolvimento. Foram analisados espectros de massa de um total de 362 amostras (211 SARS-CoV-2 positivos e 151 negativos por RT-PCR) sem preparação prévia de amostras de três laboratórios diferentes e testados dois métodos de seleção e seis abordagens de aprendizado de máquina para identificar as abordagens de análise de melhor desempenho e determinar a precisão da detecção do SARS-CoV-2. O modelo proporcionou a maior precisão (93,9%), com 7% de falsos positivos e 5% falsos negativos sugerindo que MALDI-MS e análise de aprendizado de máquina podem ser usados para detectar de forma confiável SARS-CoV-2 em amostras de swab nasal (30/07/2020). Fonte: Nature Biotecnology
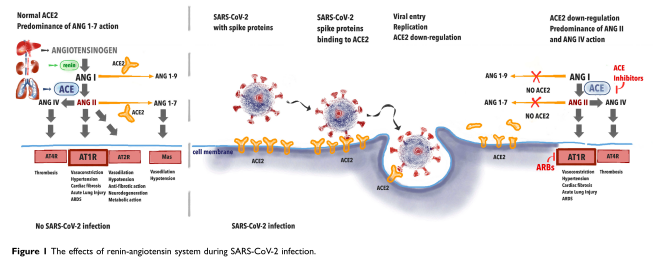
31/07/2020
Pesquisadores estabelecem um ensaio real-time reverse-transcription recombinase-aided amplification assay (RT-RAA) para detectar rapidamente o SARS-CoV-2. Os iniciadores e a sonda foram projetados com base na sequência do gene da proteína do nucleocapsídeo (gene N) da SARS-CoV-2. O limite de detecção foi de 10 cópias por reação neste ensaio, que pode ser realizado em 15 minutos a uma temperatura constante (39 °C), sem nenhuma reação cruzada com outros patógenos do trato respiratório, como outros coronavírus. Além disso, comparado com o ensaio comercial de RT-PCR em tempo real, mostrou um valor kappa de 0,959 (p <0,001) de 150 amostras clínicas. Os resultados indicaram que esse teste RT-RAA em tempo real pode ser uma ferramenta valiosa para a detecção de SARS-CoV-2 (29/07/2020). Fonte: Virology
Novo ensaio de imunodetecção à base de enzimas que quantifica diretamente a proteína S viral sintetizada dentro de células fixas e permeabilizadas. O teste do tipo ELISA permite a detecção rápida e quantitativa da infecção por SARS-CoV-2 no formato de microtitulação, independentemente do isolado do vírus ou da cultura de células alvo. O método estabelecido de realização de ensaios ELISA não requer instrumentação cara e permite, por exemplo, determinar TCID50 de estoques de vírus, eficiências antivirais (valores de IC50) de medicamentos ou atividade neutralizante de soros (29/07/2020). Fonte: Antiviral Research
A RT-PCR em tempo real da saliva pura apresentou uma sensibilidade geral para a detecção de RNA do SARS CoV-2 de 85,7% quando comparada aos swab de esfregaços nasofaríngeos coletados simultaneamente. O estudo destacou a necessidade de otimizar a coleta e o processamento antes que a saliva possa ser usada para testes de alto volume (31/07/2020). Fonte: Journal of Clinical Virology
As abordagens para detectar o RNA viral com base na amplificação isotérmica mediada por alça de transcrição reversa (RT-LAMP) têm potencial como métodos de teste simples, escalonáveis e amplamente aplicáveis. Comparados aos métodos baseados em RT-qPCR, os ensaios RT-LAMP requerem incubação a uma temperatura constante, eliminando assim a necessidade de instrumentação sofisticada. O estudo testa um protocolo de ensaio RT-LAMP de duas cores para detectar RNA viral SARS-CoV-2 usando um conjunto de iniciadores específico para o gene N (27/07/2020). Fonte: Science Translational Medicine
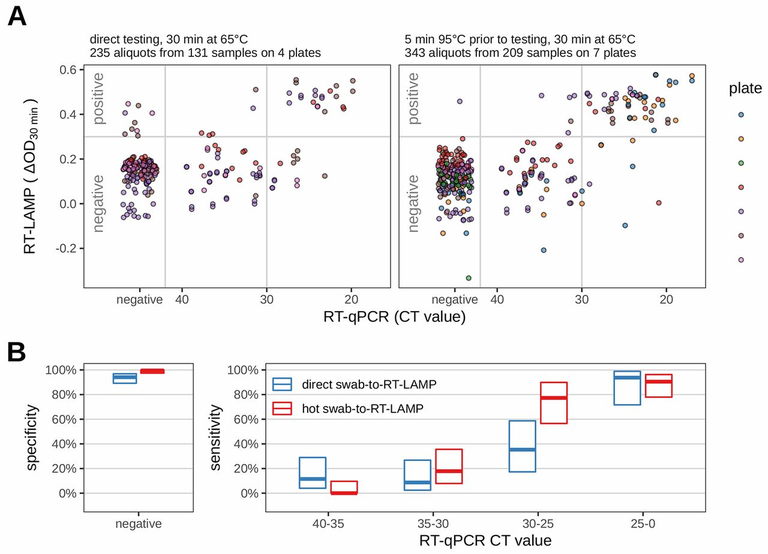
30/07/2020
Artigo propõe método simples e específico para detecção de RNA do SARS-CoV-2. O método leva 10 minutos e pode ser realizado entre 15-35ºC. O ensaio é baseado em nanoscaffold de DNA (DNHCR), onde as nanoscaffolds de DNA foram construídas pela auto-montagem de longos fios de DNA e sondas auto-sacientes (H1). Em seguida, é realizada a hibridização do RNA do SARS-CoV-2 com as sondas de DNA H1 e H2 ao longo da nanoscaffold, e um nanostring de DNA iluminado é imediatamente obtido. Além disso, a confiabilidade do método DNHCR em amostras de soro e saliva também foi validada. Portanto, espera-se que o método baseado em DNHCR forneça uma alternativa simples e mais rápida ao ensaio tradicional SARS-CoV-2 qRT-PCR.(29/07/2020) Fonte: Biosensors and Bioelectronics
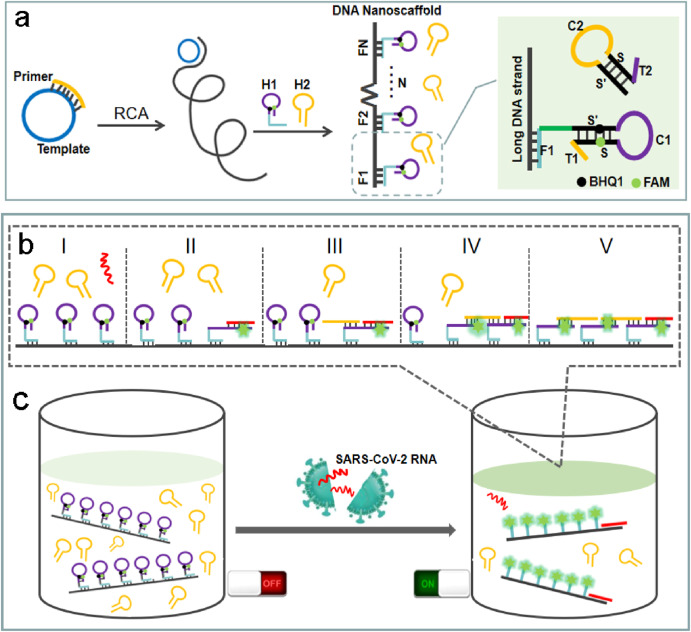
Os autores discutem os avanços alcançados com os testes de PCR e PCR multiplex no diagnóstico da COVID-19, apresentam a tecnologia de PCR LAMP. Afirma que o tempo de diagnóstico foi reduzido e com dispositivos muito pequenos. Como novas tecnologias, discutem os métodos de diagnóstico CRISPR e os dispositivos portáteis de sequenciamento de DNA. Abordam também os sistemas de imunoprecipitação que utilizam antígenos marcados com luciferase, onde não só a identificação, mas também a quantificação pode ser monitorada (07/2020). Fonte: Derleme Review
Revisão de todos os estudos publicados que documentavam os níveis séricos de ferritina em pacientes com COVID-19 grave e não grave. Estudos em pacientes com COVID-19 relataram os níveis de alguns marcadores inflamatórios, como procalcitonina, proteína C reativa, taxa de sedimentação de eritrócitos e amilóide sérica A. No entanto, pouca atenção foi dada à ferritina, embora a hiperferritinemia tenha sido associada com complicações em outras doenças virais, como a dengue e a concentração circulante de ferritina poderia ser usada para prever a progressão do COVID-19 e associar a hiperferritinemia ao desenvolvimento da tempestade de citocinas (21/06/2020). Fonte: NCBI

O pool de amostras oferece enormes vantagens em comparação com o qRT-PCR de teste único, pois reduz os custos de diagnóstico, tempo da equipe, a exaustão dos profissionais de saúde e tempos de execução analíticos. Artigo cita exemplos de países como Gana, Malawi, África do Sul e Zimbábue que vem implementando o pool de amostras para rRT-PCR em vez de testes de diagnóstico rápido por anticorpos como mecanismo na avaliação da COVID-19 (07/2020). Fonte: mSphere
29/07/2020
Revisão descreve testes de diagnóstico atualmente disponíveis para detectar o vírus SARS-CoV-2 ou a resposta imunológica induzida pelo patógeno, particularmente os mecanismos pelos quais os testes funcionam. A análise compara o desempenho destes testes e é útil na seleção daqueles mais apropriados para determinada aplicação, como por exemplo, para estudos epidemiológicos ou pesquisa geral de pandemia, triagem populacional, testes hospitalares, testes domiciliares e em locais de atendimento e ensaios terapêuticos. Também foram destacadas as deficiências de certos testes e necessidades futuras (25/07/2020). Fonte: iScience.
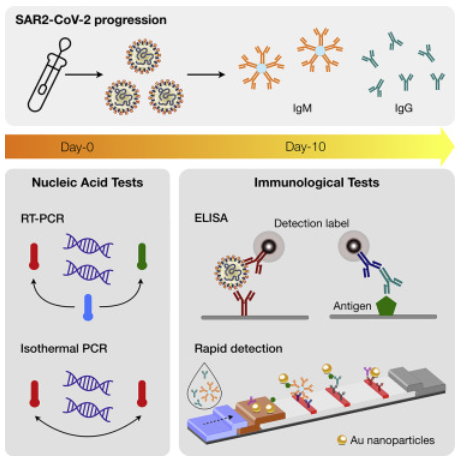
Estudo utiliza 34.348 resultados de testes de amplificação de ácido nucléico (NAAT) de SARS CoV-2 em dois sistemas de saúde e estima a que o NAAT de SARS CoV-2 tem uma sensibilidade de 82 a 97% para o diagnóstico de COVID-19 entre pacientes sintomáticos (24/07/2020). Fonte: Oxford Academic
28/07/2020
Nesta revisão, os autores fazem uma discussão apresentam o desenvolvimento de biossensores utilizando grafeno. Fazem uma discussão sobre a evolução da nanotecnologia, grafeno e derivados de grafeno de tamanho nanométrico que tem sido utilizados na construção de biossensores devido às suas propriedades físico-químicas e biocompatibilidade. Argumentam que a combinação de biomoléculas com os recursos específicos de reconhecimento e materiais de grafeno fornece uma estratégia promissora para construir biossensores mais estáveis e sensíveis. Que podem ser utilizados para a detecção de patógenos. Apresentam o desenvolvimento de biossensores de grafeno para a detecção de patógenos bacterianos e virais. Discutem os desafios e a perspectiva de desenvolvimento de biossensores para detecção de patógenos e a contribuição para a prevenção de epidemias (25/07/2020). Fonte: Biosensors and Bioelectronics

Artigo apresenta novo protocolo para detecção do SARS-CoV-2 por qRT-PCR diretamente do swab da nasofaringe sem necessidade de extração do RNA, mantendo alta sensibilidade e especificidade na detecção de RNA de SARS-CoV-2. A extração de RNA é preferível ao uso de amostras diretas porque o processo de extração concentra e purifica os alvos de RNA e exclui substâncias inibidoras do PCR. No entanto, a abordagem apresentada conseguiu, ao pular a etapa de extração de RNA, reduzir significativamente o custo e melhora o tempo de resposta do ensaio com taxa de inibição de RT-qPCR semelhante à de uma abordagem padrão (24/07/2020). Fonte: PLosOne
A Secretaria de Estado de Saúde (SES) assinou um termo de cooperação com o Dados do Bem, iniciativa sem fins lucrativos desenvolvida pelo Instituto D'Or de Pesquisa e Ensino (IDOR) e pela Zoox Smart Data, que vai permitir triplicar o número de testes imunosorológicos para COVID-19 oferecidos pelo estado. O Dados do Bem é um aplicativo que permite um imenso ganho tecnológico para a marcação e a realização dos testes e um mapeamento mais preciso da curva do novo coronavírus no Rio de Janeiro. Ele combina inteligência epidemiológica, geolocalização e big data para acompanhamento, em tempo real, da distribuição da pandemia nos centros urbanos. Os resultados vão auxiliar o Governo do Estado na tomada de decisões em relação ao enfrentamento da pandemia (07/07/2020). Fonte: O Fluminense
Estudo mostra que amostras de saliva diretamente lisadas podem servir como uma fonte adequada para a detecção de RNA viral que é uma forma mais barata para se testar SARS-CoV-2 sendo tão eficiente quanto o protocolo clássico (RT-qPCR) que envolve a purificação em coluna do RNA viral (23/07/2020). Fonte: Journal Clinical microbiology
27/07/2020
Os autores fazem uma revisão avaliando o perfil de coagulação nos casos graves de COVID-19, mostrando a complexidade e destacando formas diferentes de progressão do quadro. Destacam que muitos pacientes podem apresentar estado hipercoagulável devido a resposta inflamatória, comorbidades, imobilização, uso de ventilação mecânica e / ou oxigenação extracorpórea por membrana, entre outras. Afirmam que um ponto chave nesses pacientes é definir as melhores estratégias de teste para avaliar o risco de um evento tromboembólico com foco em testes de coagulação (07/2020). Fonte: Revista Brasileira de Terapia Intensiva
A identificação e isolamento de pacientes infectados com SARS-CoV-2 é essencial para controlar a pandemia de COVID-19. Muitas empresas e institutos estão buscando métodos eficazes para a detecção rápida do RNA do SARS-CoV-2, anticorpos, antígenos e vírus. Nesta revisão, são discutidas a estrutura do vírus SARS-CoV-2, o genoma e as características da expressão genética e a atualização da detecção de RNA, anticorpos, antígenos e vírus SARS-CoV-2. Por fim, o artigo fornece uma revisão dos biossensores com potencial promissor para a detecção de pacientes com COVID-19. Dessa forma, a revisão fornece uma visão geral para os cientistas da comunidade de pesquisa em biossensores e da indústria de biossensores, com foco no desenvolvimento de sistemas de detecção da COVID-19 (21/07/2020). Fonte: Biosensors and Bioelectronics.
24/07/2020
Está revisão resume o estado da arte da detecção de vírus diferentes com os métodos de detecção eletroquímica atualmente disponíveis. Além disso, discute diferentes técnicas de fabricação, princípios de detecção e aplicações de vários biossensores de vírus. E destacam pesquisas com o uso de biossensores eletroquímicos na fabricação de um kit de detecção de para a identificação rápida do COVID-19 (07/2020). Fonte: Biosensors and Bioelectronics
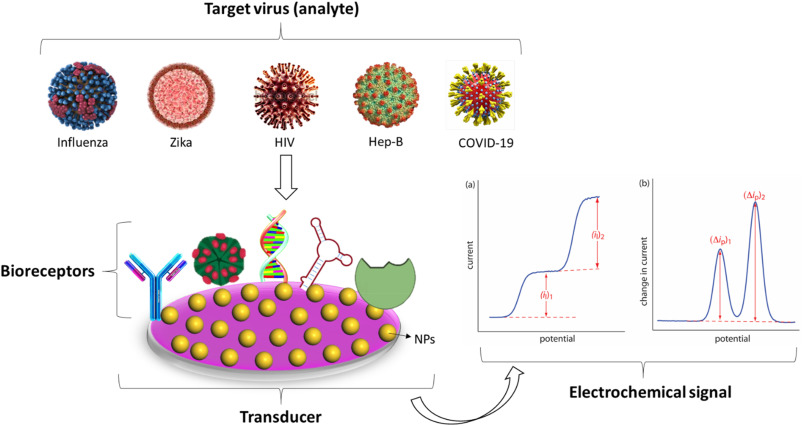
Os autores apresentam um nova metodologia qRT-PCR multiplex para a detecção simultânea do genoma SARS-CoV-2 (gene N) e do gene RNAse P humano como controle interno. Apontam que o qRT-PCR multiplex foi eficaz na detecção da infecção por SARS-Cov-2 em amostras humanas com 100% de sensibilidade. Notavelmente, pacientes com poucas cópias do RNA da SARS-CoV-2 (<5 cópias / reação) foram detectados com sucesso pelo novo método qRT-PCR multiplex. Finalmente, avalia-se a eficácia do qRT-PCR multiplex em swabs nasofaríngeos humanos sem extração de RNA (17/07/2020). Microorganisms
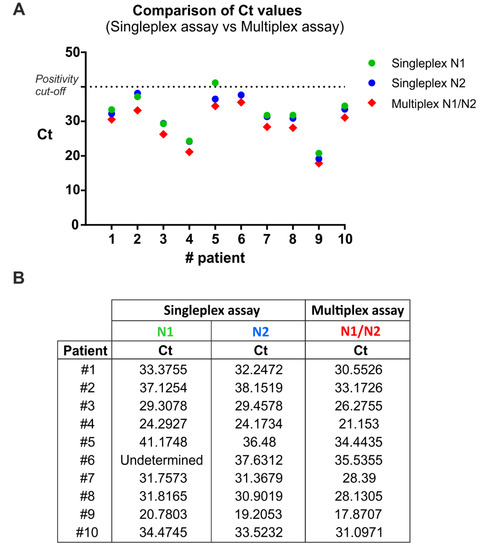
23/07/2020
Artigo analisa o método para detectar a presença do SARS-CoV-2 usado como padrão-ouro e os problemas que podem surgir nesse método de detecção e demonstra a biologia do vírus e os pontos fortes e fracos do método de detecção que são importantes para o gerenciamento do paciente e para a superação da pandemia (20/07/2020). Fonte: Clinical Pharmacology & Therapeutics
22/07/2020
Os autores fazem uma revisão sobre o uso da nanotecnologia para o desenvolvimento de biossensores visando aumentar a especificidade e a sensibilidade das plataformas diagnósticas para o SARS-CoV-2 (17/07/2020). Fonte: Bioconjugate Chemistry
Estudo relata a detecção seletiva e visual a olho nu do SARS-CoV-2, sem a necessidade de técnica instrumental. O diagnóstico consiste em ensaio colorimétrico baseado em nanopartículas de ouro (AuNPs) revestidas com oligonucleotídeos antisense modificados por tiol (ASOs) específicos para o gene N (fosfoproteína nucleocapsídica) do SARS-CoV-2. A técnica pode ser usada para diagnosticar COVID-19 em 10 minutos, em amostras isoladas de RNA. As AuNPs revestidas pelo ASO aglomeram-se seletivamente na presença da sequência de RNA alvo do SARS-CoV-2 e sofrem uma alteração em sua ressonância plasmônica de superfície. Além disso, a adição de RNaseH cliva a cadeia de RNA do híbrido RNA-DNA levando a um precipitado visualmente causado pela aglomeração adicional entre os AuNPs (21/05/2020). Fonte: ACSNano.
21/07/2020
Autores desenvolveram ensaios sorológicos para detecção de anticorpos neutralizantes específicos para a proteínas S e o nucleocapsídeo do SARS-CoV-2. Os testes foram validados e testados para vários antígenos em diferentes ELISAs internos e comerciais. O estudo demonstrou que a maioria das pessoas com SARS-CoV-2 confirmadas pelo PCR foi seroconvertida 2 semanas após o início da doença. Verificou-se que os testes ELISA de IgG ou IgA comerciais eram de menor especificidade, e a sensibilidade variava entre os 2 ensaios; o IgA ELISA mostrou maior sensibilidade. No geral, os ensaios validados descritos podem ser usados na detecção de anticorpos SARS-CoV-2 específicos. para estudos de diagnóstico, soroepidemiológico e avaliação de vacinas (21/06/2020). Fonte: Emerg Infect Dis
20/07/2020
A aprovação do promeiro produto de diagnóstico baseado em CRISPR pela FDA (EUA) - teste de uma hora da Sherlock Biosciences - para SARS-CoV-2 e o recente acordo da Mammoth Biosciences com a GlaxoSmithKline para desenvolver um teste de 20 minutos baseado em CRISPR para o mesmo vírus, destaca um novo fundamento na tecnologia de identificação de patógenos. A COVID-19 está sobrecarregando os esforços de pesquisa e desenvolvimento para estabelecer novas abordagens de testes que sejam mais rápidos, mais simples, mais baratos e mais escalonáveis do que os métodos existentes e com a mesma precisão. Biologia de sistemas, nanobiotecnologia, biofotônica e engenharia nanofluídica são apenas algumas das disciplinas que alimentam esse amplo esforço (08/07/2020). Fonte: Nature Biotechnology
17/07/2020
Os pesquisadores da Monash University desenvolveram um teste pode determinar se a pessoa está infectada no momento e se já teve COVID-19 no passado. O teste de aglutinação baseia-se nos métodos de tipagem sanguínea comumente empregados como uma opção viável. Eles descrevem a aplicação de ensaios de aglutinação ao teste sorológico de SARS-CoV-2 combinando testes de aglutinação de coluna com bioconjugados peptídeo-anticorpo, que facilitam a reticulação de glóbulos vermelhos na presença de plasma contendo anticorpos contra SARS-CoV-2 (16/07/2020). Fonte: ACS Sen, Monash University
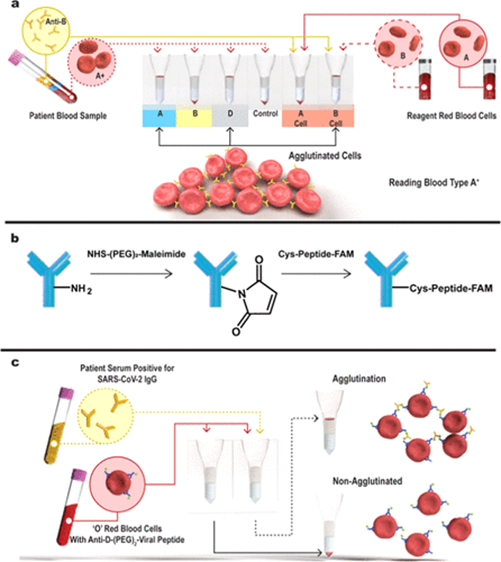
Artigo descreve método de detecção direta “in-the-spot” do SARS-CoV-2 em pacientes. O protocolo apresentado para a técnica de RT-LAMP é realizado diretamente no swab nasal sem necessidade de purificação de RNA. O protocolo foi testado com 180 pacientes e comparado ao método padrão de RT-PCR e verificaram ainda que o protocolo pode ser aplicado também em amostras de saliva. (16/07/2020) Fonte: Experimental Biology and Medicine
Estudo para avaliar do desempenho analítico e clínico de 2 testes ELISA que detectam anticorpos que agem contra a proteína nucleocapsídeo do vírus: O teste NovaLisa® SARS‐CoV‐2 IgG, IgA e IgM (NovaTec®) que permite uma detecção separada de cada anticorpo e o teste Plaquelia® SARS‐CoV‐2 Total Ab (Bio‐Rad®) que detectam anticorpos totais (IgM, IgA e IgG). Os testes NovaLisa® e Plaquelia® tiveram desempenhos analíticos satisfatórios e desempenhos clínicos excelentes para IgG, IgA e anticorpos totais (15/07/2020). Fonte: Journal of Medical Virology
Pesquisadores desenvolvem um método de detecção direta de SARS-CoV-2 por eletroforese capilar por PCR fluorescente do genoma viral. O RNA nasofaríngeo de 20 amostras positivas e 10 negativas foi isolado. O cDNA foi sintetizado e dois fragmentos do SARS-CoV-2 foram amplificados. Um dos iniciadores para cada par foi marcado com fluorocromo na extremidade 5 '. As amplificações foram submetidas à eletroforese capilar em sequenciadores ABI3130 para visualizar os picos fluorescentes. O método alternativo desenvolvido identifica o genoma SARS-CoV-2 que pode ser dimensionado para a análise de aproximadamente 100 amostras em menos de 5 h (10/07/2020). Fonte: Journal of Virological Methods
Os autores abordam o desenvolvimento e a validação do IMMUNO-COV ™, um teste clínico de alto rendimento para medir quantitativamente anticorpos neutralizantes para SARS-CoV-2, o subconjunto específico de anticorpos anti-SARS-CoV-2 que bloqueiam a infecção viral. Os resultados mostram que o ensaio IMMUNO-COV ™ quantifica com precisão os anticorpos neutralizantes de SARS-CoV-2 em soros humanos. O ensaio pode fornecer informações vitais para comparar as respostas imunes às várias vacinas SARS-CoV-2 que estão atualmente em desenvolvimento ou para avaliar a elegibilidade de doadores em estudos de terapia com plasma convalescente (27/05/2020). Fonte: BioRxiv
UFMG vai detectar comportamento e alcance do coronavírus em Betim através de um projeto que combina o método otimizado do teste RT-PCR, oferecido pela UFMG, e o teste de soroprevalência, estudado pela Secretaria Municipal de Saúde. A intenção é fazer a testagem para o coronavírus em 5,4 mil pessoas em Betim. São cinco etapas, que abrangem 1.080 pessoas cada uma, em intervalos de 21 dias. Em cada abordagem, são feitos o teste rápido sorológico e uma coleta da swab nasal, com cotonete, que posteriormente é examinada em laboratório (17/07/2020). Fonte: UFMG
16/07/2020
O teste RT-PCR é o método mais usado até agora para detectar infecções pelo SARS-CoV-2. No entanto, vários outros ensaios mais rápidos e precisos estão sendo desenvolvidos para o diagnóstico da COVID-19 com o objetivo de controlar a propagação da infecção através da identificação dos pacientes e seu isolamento imediato. Nesta revisão, os autores discutem os vários métodos de detecção do vírus SARS-CoV-2, incluindo os recentes desenvolvimentos em ensaios imunológicos, técnicas de amplificação, bem como biosensores (14/07/2020). Fonte: Talanta
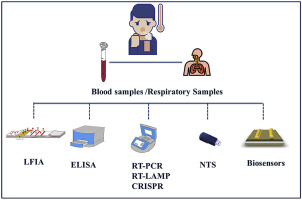
UFMG cria método inédito para diagnosticar COVID-19 e outras doenças virais com uso de inteligência artificial. A plataforma, batizada de PoLiVirUS, faz o diagnóstico por meio da comparação entre células infectadas e amostras não infectadas a partir de um swab nasal. Os testes clínicos com amostras de pacientes reais começaram há duas semanas e apresentaram precisão de quase 90% (16/07/2020). Fonte: UFMG

Os autores abordam a questão do limite de detecção dos testes de RT-PCR (LoDs) em amostras nasofaríngeas, padrão ouro. Apontam que os LoDs dos ensaios atualmente aprovados variam mais de 10.000 vezes. Abordam essa questão usando mais de 27.500 resultados de testes para pacientes de toda a nossa rede de saúde testados usando o Abbott RealTime SARS-CoV-2 EUA. Sugerem que cada aumento de 10 vezes na LoD a taxa de falsos negativos aumenta em 13%, perdendo uma taxa adicional em oito pacientes infectados (40/06/2020). Fonte: BioRxiv
15/07/2020
Residentes em estabelecimentos de cuidados de longo prazo (asilos) têm um risco particularmente alto de infecção e desfechos ruins associados à COVID-19. No entanto, a recomendação é que os testes sejam feitos somente em pacientes sintomáticos. Em 11 instituições de Maryland (USA) os autores realizaram testes em todos os residentes não testados ainda e mapearam os seus sintomas no momento do teste. Dos 893 residentes testados, 354 casos adicionais (39,6% dos testados) foram identificados com testes não incluídos dos testes iniciais baseados em sintomas. Esses resultados ressaltam a importância de testar em larga escala, pois abordagens baseadas em sintomas podem perder um número substancial de casos. Casos assintomáticos não reconhecidos entre os residentes podem perpetuar a transmissão dentro das instalações (14/07/2020). JAMA Internal Medicine
A identificação precoce de indivíduos infectados é considerada um dos pré-requisitos mais importantes para combater a pandemia da COVID-19. Porém, testes em larga escala estão enfrentando vários desafios, incluindo a escassez de ferramentas de coleta de amostras e de reagentes biológicos moleculares. Neste estudo, pesquisadores apresentam uma plataforma bem-sucedidda de teste SARS-CoV-2 que abrange o registro de probandos, coleta e envio de amostras, teste de amostras e emissão de relatórios. A detecção do vírus foi baseada em RT-PCR e foi amplamente validada (sensibilidade (96,8%) e especificidade (100%)). O estudo exemplifica como o teste preventivo de SARS-CoV-2 pode ser configurado de maneira rápida e flexível. A estratégia delineada pelo presente estudo pode servir como um plano para a implementação de testes preventivos em larga escala de SARS-CoV-2 em outras localidades (08/07/2020). Fonte: Diagnostics
Para traçar o perfil das respostas IgG e IgM específicas de SARS-CoV-2, os autores construíram um microarray de proteoma SARS-CoV-2 com 18 das 28 proteínas previstas. Um conjunto de 29 soros convalescentes usado foi usado para testagem, o perfil global de IgG e IgM foi obtido simultaneamente por meio de uma estratégia de dupla cor. Os dados mostraram claramente que tanto a proteína N quanto a S1 eram adequadas para o diagnóstico, enquanto a S1 purificada a partir da célula de mamífero pode possuir melhor especificidade. Os autores propõem o uso deste microarray para determinação de perfis profundos de resposta a IgG e IgM. E apontam que os resultados deste estudo irão lançar luz sobre o desenvolvimento de um kit de diagnóstico mais preciso, tratamento mais apropriado e vacina mais eficaz (14/07/2020). Nature
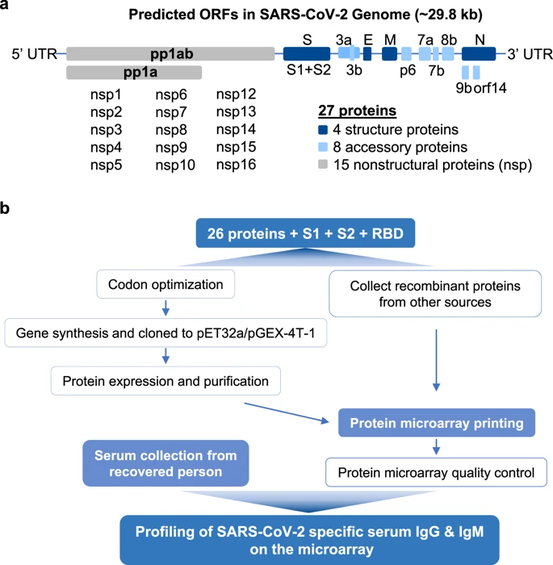
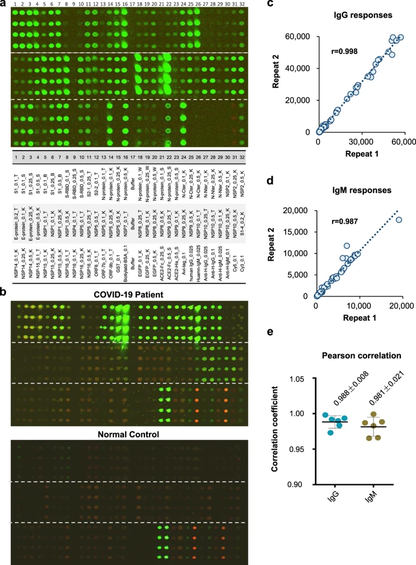
14/07/2020
Trabalho fornece um novo método RT‐qPCR, denominado GPS™ CoVID‐19 dtec‐RT‐qPCR, altamente específico e validado para detecção de SARS‐CoV‐2 (11/07/2020). Fonte: Journal of Applied Microbiology
A startup Cellco Biotec, de São Carlos (SP), desenvolveu um método que ajuda a baratear o teste molecular de COVID-19. Os testes de RT-qPCR são realizados hoje, em sua maioria, em um modelo chamado singleplex, em que material genético do vírus SARS-CoV-2 é processado em quatro tubos, com diferentes marcadores de detecção. Esse procedimento torna o exame caro e demorado, limitando a aplicação. A Cellco Biotec está desenvolvendo um kit de diagnóstico de COVID-19 por RT-qPCR pelo método multiplex, em que todas as reações ocorrem em único tubo, possibilitando não só realizar testes de RT-qPCR de uma amostra muito maior de pacientes de uma única vez como também barateá-los, uma vez que a quantidade de reagentes utilizados será menor (08/07/2020). Fonte: Agencia FAPESP
Artigo apresenta primeiro teste diagnostico para COVID-19 baseado em NGS (next-generation sequencing). O teste emprega 98 fragmentos de DNA, para cobrir as cerca de 30 quilobases do genoma SARS-CoV-2. Com a reação de multiplex, mais de 3.000 testes de amostras nasofaríngeas ou orofaríngeas podem ser executados de uma só vez em 24 horas. A empresa afirma que o teste requer pelo menos 1.000 cópias do genoma viral por mililitro e apresenta 98% de sensibilidade e 97% de especificidade. Além do teste rápido e em larga escala a técnica ainda fornece informações das sequencias de RNA do vírus, contribuindo para avaliação das taxas de mutação do vírus e rotas de transmissão. O teste ainda precisa da aprovação do FDA. (08/07/2020) Fonte: Nature Biotechnology
13/07/2020
Os autores fazem uma revisão das metodologias detecção sorológico de anticorpos anti-SARS-CoV-2, fazendo um comparativo sobre a performance das metodologias empregadas (14/06/2020).Fonte: Diagnostics
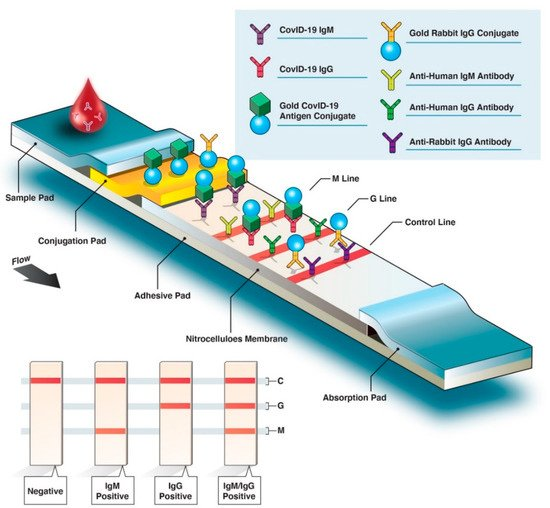 1
1
10/07/2020
Artigo demonstra que a exposição intrafamiliar ao SARS-CoV-2 pode induzir a resposta imune celular sem soroconversão. Para isso foram investigadas as respostas imunes humoral e celular ao SARS-CoV-2 em 9 pacientes “index” (diagnosticados com COVID-19 leve) e 8 pessoas de contato de 7 domicílios. Todos os pacientes “index” desenvolveram anticorpos e células T específicas SARS-CoV-2, com as respostas direcionadas contra múltiplas proteínas estruturais e acessórias. No entanto, nenhum dos pacientes de contato tinha anticorpos detectáveis ao SARS-CoV-2. Apesar da falta de soroconversão, as células T específicas SARS-CoV-2 foram detectadas em 6 pacientes de contato em frequências semelhantes às de pacientes “index”, sugerindo que os testes para células T específicas para SARS-CoV-2 podem ser melhores do que testes sorológicos para avaliação de infecção prévia e imunidade ao vírus. No entanto, um estudo mais aprofundado é justificado para descartar a reatividade cruzada com infecções anteriores de coronavírus. (07/07/2020) Fonte: Nature Reviews Immunology
09/07/2020
Celebrados como chave para monitorar e responder à pandemia, incluindo o reinício das atividades econômicas, testes sorológicos para detectar anticorpos contra o SARS-CoV-2 ainda precisam de avaliação. Esse entusiasmo reflete a esperança de que os anticorpos contra o SARS-CoV-2 forneçam imunidade protetora e duradoura e permitam aos indivíduos recuperados retomarem suas vidas diárias. Infelizmente, ainda não se sabe o que a presença de anticorpos detectáveis significa, para um indivíduo ou para uma população, quão durável será ou qual a variação sorológica esperada entre diferentes grupos, como aqueles que tiveram uma infecção assintomática. Testes de anticorpos de alta qualidade têm o potencial de fornecer informações importantes sobre infecções anteriores, e a prevalência de anticorpos em uma população pode nos ajudar a entender a extensão da epidemia e o papel da transmissão de indivíduos assintomáticos. Entretanto, mais pesquisas são necessárias para abordar questões fundamentais sobre a presença de anticorpos e o grau e durabilidade da proteção. (03/07/2020). Fonte: BMJ.
Quantificação de anticorpos contra SARS-CoV-2 com 08 imunoensaios comercialmente disponíveis. A comparação entre estes dados é necessária como base para análise plasma convalescente e potenciais interpretações (08/2020). Fonte Journal of Clinical Virology.
Artigo apresenta análise da sensibilidade dos testes comerciais de anticorpos para a nucleoproteína e para a glicoproteína do SARS-CoV-2 em um estudo diagnóstico prospectivo. Os testes foram avaliados com 73 soros de indivíduos RNA positivos para SARS CoV-2 apresentando sintomas leve a moderados ou infecção assintomática. A sensibilidade geral dos testes variou de 64,4 a 93,2%. Os ensaios mais sensíveis reconheceram 95,8-100% dos soros obtidos após 4 semanas ou mais. Ensaios com anticorpos para as nucleoproteínas e glicoproteínas apresentaram sensibilidade semelhante indicando que os testes com ambos os antígenos são adequados para diagnósticos sorológicos. No entanto, os resultados demostraram que apesar a sensibilidade comparável, os testes reagiram com diferentes conjuntos de soro. A observação indica que uma combinação de testes à base de nucleoproteína e glicoproteína aumentaria o percentual de resultados positivos.(06/07/2020) Fonte: Journal of Clinical Virology
Estudo busca determinar a dose de radiação gama necessária para inativar o SARS-CoV-2 e seu efeito nos testes de PCR. A radiação gama é frequentemente a escolha preferida para a inativação viral porque costuma preservar a integridade da morfologia viral e suas estruturas proteicas. Uma dose de radiação de 1 Mrad foi capaz de inativar completamente 106,5 TCID50/ml de SARS-CoV-2. A influência da radiação gama na sensibilidade do PCR foi inversamente proporcional e dose dependente até 0,5 Mrad sem maior redução posteriormente, sugerindo que a radiação gama pode ser usada como um método confiável para inativar SARS-CoV-2 com efeito mínimo no ensaio PCR subsequente. (30/06/2020) Fonte: Applied Biosafety
08/07/2020
Nesse artigo os autores da USP fazem uma reflexão sobre a participação das universidades no desenvolvimento e na realização de testes diagnósticos moleculares para identificação do coronavírus. Apontam que apesar de não estarmos prontos para atender essa demanda massiva de testes moleculares em curtíssimo intervalo de tempo, havia diversos atores com formação e capacitação técnica para a entrega dos resultados necessários. Bem como a existência de um número maior de equipamentos do que aqueles disponíveis na estrutura pública de vigilância em saúde (26/06/2020). Cadernos de Saúde Pública
07/07/2020
O artigo pre-proof revela que o Kit de Detecção (nCoV-DK) reduz pela metade o tempo de detecção do SARS-CoV-2, eliminando as etapas de extração de RNA e purificação. Avaliaram que a concordância entre o nCoV-DK e a PCR direta o vírus foi detectado em 53/71 (74,6%) e 55/71 (77,5%) pela PCR direta e nCoV-DK, respectivamente, com taxa de concordância geral de 94,4% para 95,2% no swab nasofaríngeo, 95,5% na saliva e 85,7% no escarro. O nCoV-DK detecta efetivamente o SARS-CoV-2 em todos os tipos de amostras, incluindo saliva, reduzindo o tempo necessário para detecção, trabalho e risco de erro humano (23/06/2020). Fonte: International Journal of Infectious Diseases
Lista com biomarcadores disponíveis e sua comparação da faixa de secreção de pacientes normais com pacientes COVID-19 através de análises clínicas demonstra a possibilidade do desenvolvimento de um biomarcador não invasivo para o diagnóstico da detecção de COVID-19 (01/07/2020). Fonte: Sensing and Bio-Sensing Research
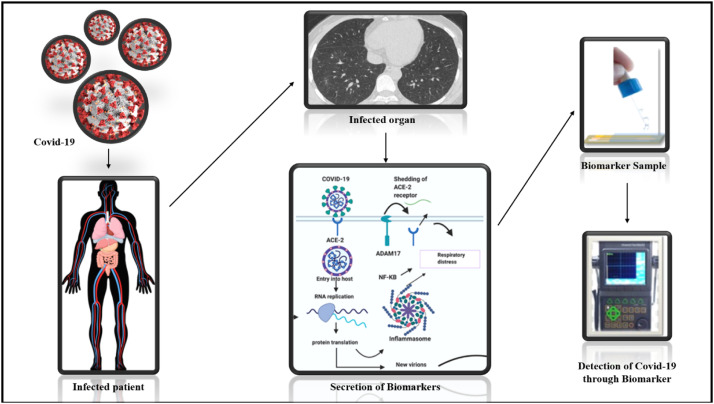
Revisão resume e compara o desenvolvimento de diagnósticos no ponto de atendimento e aqueles atualmente em desenvolvimento, incluindo PCR de transcrição reversa quantitativa (RT-qPCR), imunoensaios sorológicos (SIAs) e método de microarray de proteínas (PMM) projetado para diagnóstico padrão e rápido de COVID-19 (26/06/2020). Fonte: Diagnostics (Basel)
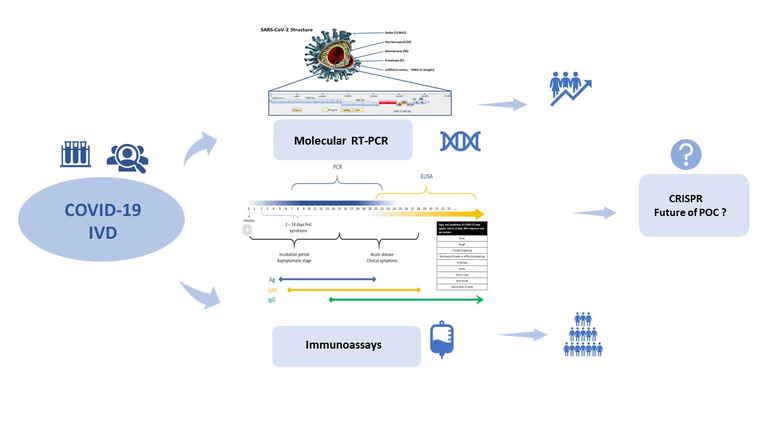
06/07/2020
Pesquisadores fazem uma revisão dos métodos de teste de laboratório existentes para SARS-CoV-2, incluindo testes de ácidos nucleicos, testes de anticorpos e sequenciamento genômico. Comparam as vantagens e desvantagens entre os diferentes métodos de teste de laboratório para o COVID-19 e fornecem uma perspectiva de aprimoramento e desenvolvimento da tecnologia de detecção. A especificidade e a sensibilidade da detecção de anticorpos da subclasse Ig também foram comparadas (02/07/2020) Pre-proof. Fonte: Clinica Chimica Acta
03/07/2020
Foram analisados os perfis de níveis de IgG/IgM/IgA em relação às proteínas S e N no soro de pacientes COVID-19. Todos os soros convalescentes dos pacientes COVID-19 continham anticorpos IgG específicos contra a proteína N do SARS-CoV-2, mas nem todos os pacientes hospitalizados tinham anticorpos IgG específicos para o fragmento RBD da proteína S devido ao estágio de infecção precoce, demonstrando que a proteína N tem um bom potencial para desenvolvimento de diagnóstico. Por outro lado, ensaios para detectar anticorpos neutralizantes indicam que os anticorpos RDB-específicos parecem estar mais relacionados com a proteção antiviral, sugerindo que a manipulação da resposta imune induzida por RDB seriam mais indicadas para desenvolvimento de vacinas efetivas. Para identificar os melhores epítopos foram sintetizados 42 peptídeos da proteína S e identificaram que os domínios responsáveis pela maior imunogenicidade e relacionados com ambas respostas de célula B e T (01/06/2020). Fonte: Cell Research
Revisão sobre a aplicação de nanopartículas magneto-plasmônicas em biossensores, incluindo sensores virais. Esses nanomateriais híbridos são o resultado do progresso feito na síntese e caracterização desses materiais. A possibilidade de aplicar diversas abordagens de química superficial para fornecer grupos funcionais e ligantes superficiais nesses híbridos torna essas nanoestruturas diretamente aplicáveis à detecção viral. (29/07/2020). Fonte: Nanomaterials
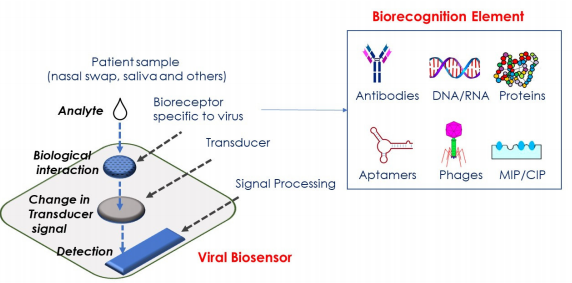
02/07/2020
O ensaio LIAISON® SARS-CoV-2 S1 / S2 IgG foi projetado para medir anticorpos contra as proteínas S1 / S2 nativas de SARS-CoV-2 em um ensaio quimioluminescente automatizado padronizado, os primeiros resultados estão disponíveis em 35 minutos, com um rendimento de 170 testes/hora. O desempenho clínico e analítico do teste foi validado em um estudo observacional utilizando amostras residuais (> 1500) com diagnóstico positivo ou negativo de COVID-19. A sensibilidade diagnóstica do teste foi de 91,3% e 95,7% (> 5 ou ≥15 dias). A especificidade do ensaio variou entre 97% e 98,5%. A imprecisão média do ensaio foi <5% do coeficiente de variação (24/06/2020). Fonte: Journal of Clinical Microbiology
Pesquisa que avaliou 40 estudos preliminares sobre diagnósticos do novo coronavírus apontou "grandes fragilidades" nos estudos que recomendam a realização de testes rápidos para o diagnóstico da COVID-19 e afirmaram não haver evidências para a aplicação de testes sorológicos em pontos de atendimento à saúde. Dentre os estudos apenas quatro contaram com uma análise mais completa no perfil dos pacientes. Além disso, os pesquisadores apontaram para uma diferença na sensibilidade de testes clínicos e comerciais. Os ensaios de imunoabsorção enzimática (ELISA) se mostraram mais eficazes que os imunoensaios de fluxo lateral (LFIA) (02/07/2020). Fonte: BMJ

01/07/2020
Pesquisadores da Suécia mostram que muitas pessoas com COVID-19 leve ou assintomático demonstram a chamada imunidade mediada por células T ao novo coronavírus, mesmo que não tenham testado positivamente para anticorpos. Segundo os pesquisadores, isso significa que a imunidade da população é provavelmente maior do que sugerem os testes de anticorpos. O estudo apresenta as análises imunológicas de amostras de mais de 200 pessoas, muitas das quais apresentaram sintomas leves ou inexistentes de COVID-19. Os resultados indicam que aproximadamente duas vezes mais pessoas desenvolveram imunidade de células T em comparação com aquelas onde se detecta anticorpos. Adicionalmente os resultados indicam que o SARS-CoV-2 provoca respostas robustas das células T de memória semelhantes às observadas em vacinas bem-sucedidas, sugerindo que a exposição ou infecção natural pode impedir episódios recorrentes de COVID-19 grave também em indivíduos soronegativos (29/06/2020). Fonte: BioRxiv
29/06/2020
O uso de testes sorológicos, em conjunto com reação em cadeia da polimerase com transcrição reversa foi demonstrado que aumenta significativamente a sensibilidade de detecção de pacientes infectados com SARSCoV-2. Havia evidências conflitantes sobre se títulos de anticorpos estariam correlacionados com a gravidade clínica. Contudo, investigações preliminares indicaram alguns imunoensaios pode ser um substituto para a previsão de neutralização títulos de anticorpos e seleção de pacientes recuperados para doação de soro convalescente (25/06/2020). Fonte: American Journal of Clinical Pathology.
Estudo demonstra que o GeneXpert®️ forneceu detecção sensível e precisa do SARS-CoV-2 em uma variedade de amostras do trato respiratório superior e inferior sendo um teste altamente sensível e específico. A tecnologia é adequada para o teste de vários tipos de amostras e fornece resultados em tempo real (até 45 minutos). Muitos hospitais em todo o mundo já possuem sistemas GeneXpert que podem executar de 1 a 80 testes por vez, portanto a implementação dessa tecnologia tem o potencial de um impacto global significativo. Como os testes podem ser realizados em laboratórios hospitalares locais onde o tempos de resposta estendidos associados aos testes de laboratório de referência podem ser evitados (04/05/2020). Fonte: American Siciety for Microbiology
26/06/2020
Artigo com explicação sobre as principais questões sobre os testes utilizados para diagnosticar a COVID-19 (24/06/2020). Fonte:BMJ
Autores comparam os testes de triagem de saliva com os testes de swab nasofaríngeas convencionais. Os resultados sugerem que a saliva pode ser uma amostra confiável para a detecção de SARS-CoV-2 (23/06/2020). Fonte: Journal of Oral Science
25/06/2020
Estudo revela que os soros inativados pelo aquecimento a 56 ℃ por 30 minutos podem minimizar o risco de contaminação por vírus e não prejudicar a taxa de detecção positiva usando o kit de detecção de anticorpos SARS-CoV-2 (imunoensaio ELISA) e representando uma contribuição valiosa para um diagnóstico sorológico mais seguro do COVID-19. No entanto, como as pequenas amostras o estudo, são necessárias mais experiências e amostras em outros laboratórios para validar os resultados (20/06/2020). Fonte: Clinica Chimica Acta
19/06/2020
Além da UFMG, as universidade as federais Fluminense (UFF), da Paraíba (UFPB), de Pernambuco (UFPE), de Goiás (UFG), de São Paulo (Unifesp), de Santa Maria (UFSM/RS), do Mato Grosso do Sul (UFMS), do Rio de Janeiro (UFRJ), do Amazonas (Ufam), do Paraná (UFPR), do Oeste da Bahia (Ufob) e a Universidade Estadual de Santa Cruz (UESC/BA) compõem rede de laboratórios dedicada a ampliar a capacidade de realização de testes diagnósticos da COVID-19, por meio da detecção de marcadores moleculares do vírus Sars-CoV-2. (19/06/2020). Fonte: UFMG
Pesquisadores estudam a amplificação isotérmica mediada por loop de transcrição reversa em tempo real (RT-LAMP) para detecção rápida de SARS-CoV-2. Este ensaio detectou uma cópia / reação do RNA SARS-CoV-2 em 30 min. Tanto a sensibilidade clínica como a especificidade deste ensaio foram de 100%. O RT-LAMP mostrou desempenho comparável ao RT-qPCR. Combinando simplicidade e relação custo-benefício, este ensaio é, portanto, recomendado para uso em configurações de recursos limitados (03/06/2020). Fonte: PeerJ
Estudo compara o desempenho de 13 testes de RT-PCRs comerciais para detecção do SARS-CoV-2 e identifica que a sensibilidade analítica variou entre 3,3 cópias de RNA e 330 cópias de RNA. Todos os kits de RT-PCR incluídos neste estudo exibiram eficiências de > 90%, exceto um (que apresentou 80%) e apenas um ensaio apresentou reação cruzada com outro coronavírus (MERS) (17/06/2020). Fonte: Journal of Clinical Virology
Estudo avalia o desempenho do teste do swab orofaríngeo em comparação com o teste do swab nasofaríngeo para diagnóstico de COVID-19. Foram analisados 146 pares de swab nasofaríngeo (NP) e orofaríngeo (OP) coletados ≤7 dias desde o início da doença. Os resultados diagnósticos do RT-PCR SARS-CoV-2 foram 95,2% concordantes. No entanto, os valores de Ct do swab NP foram mais baixos (indicando mais vírus) em 66,7% dos pares positivos-concordantes, sugerindo que os swabs NP podem detectar com mais precisão a quantidade de SARS-CoV-2 (16/06/2020). Fonte : Clinical Infectious Diseases
17/06/2020
Foram analisados os dados de detecção dos anticorpos IgM e IgG em 169 pacientes com a COVID-19 para avaliar diferenças no desempenho clínico do método de ouro coloidal e o do método de quimioluminescência. Embora o método de ouro coloidal seja geralmente menos sensível do que o método de quimioluminescência, ele demonstra vantagens por ter tempo de retorno mais curto, procedimento mais simples e nenhum equipamento especial necessário. As duas metodologias podem ser escolhidas de acordo com diferentes condições laboratoriais (16/06/2020). Fonte:Journal of medical virology
A PCR quantitativa para transcrição reversa (qRT-PCR) é o padrão para detecção de SARS-CoV-2; no entanto, a amplificação isotérmica mediada por alça de transcrição reversa (RT-LAMP) pode permitir testes baseados em campo mais rápidos e baratos no ponto de risco. Neste estudo, pesquisadores desenvolveram um teste rápido de diagnóstico para rastreamento que possa ser concluído em 30 a 45 minutos. Amostras de pacientes simuladas foram geradas por soro, urina, saliva, zaragatoas orofaríngeas e zaragatoas nasofaríngeas com uma porção da sequência nucleica de SARS-CoV-2. O RNA isolado de swabs nasofaríngeos coletados de pacientes reais com COVID-19 também foi testado. Segundo os autores, esse estudo pode ser usado para monitorar indivíduos expostos ou auxiliar nos esforços de triagem no campo e nos possíveis portos de entrada do vírus (12/06/2020). Fonte: PLOS ONE
16/06/2020
O objetivo deste estudo foi investigar a viabilidade de testes sorológicos de anticorpos totais combinados com o RT-PCR para detecção de SARS-CoV-2. Realizou-se um estudo retrospectivo no qual 375 pacientes foram testados. Os pacientes foram divididos em um grupo COVID-19 (n = 141) e um grupo controle (n = 234). Amostras de soro e cotonetes de garganta foram coletados de 375 pacientes para testes totais de anticorpos contra análise SARS-CoV-2 e RT-PCR, respectivamente. Os resultados de sensibilidade e especificidade mostraram a vantagem do método combinado de detecção do SARS-CoV-2, como ferramenta útil para diagnóstico preciso e tratamento oportuno de pacientes suspeitos, investigação epidemiológica, bem como monitoramento de surtos contínuos de infecções com SARS-CoV-2 (15/06/2020). Journal of Virological Methods
Pesquisadores propõem uma tecnologia baseada em impressão molecular em polímeros (MIP) para testes rápidos para COVID-19. Este artigo discute a metodologia detalhada e as características analíticas resultantes dos sensores desenvolvidos até agora e também descreve a adequação da técnica MIP para a fabricação de kits de teste para detecção rápida de COVID-19 (13/06/2020). Fonte: Transactions of the Indian National Academy of Engineering
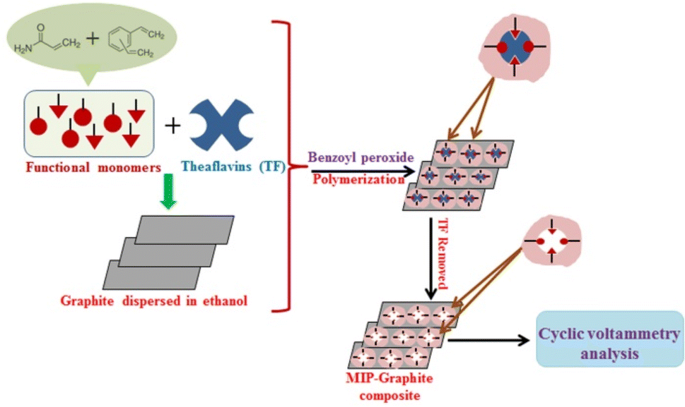
Estudo realizado com 381 pacientes propõe a utilização de escatergrama de glóbulos brancos de pacientes COVID‐19 para fazer um screening rápido dos pacientes com COVID-19, buscando aumentar a sensitividade do testagem inicial. Foi identificado um aspecto específico de "ampulheta" no fluxograma refletindo a presença de linfócitos plasmócitos circulantes. Os pacientes foram dicotomizados como COVID‐19 positivos ou negativos com base nos resultados de RT‐PCR e tomografia computadorizada. Sensibilidade e especificidade do aspecto "ampulheta" foram de 85,9% e 83,5%, respectivamente. O valor preditivo positivo foi de 94,3%. Os achados fornecem uma ferramenta não invasiva e simples para categorizar rapidamente pacientes sintomáticos como ou COVID‐19, especialmente quando RT‐PCR e/ou TC torácica não estão disponíveis rapidamente (15/06/2020). Fonte: British Journal of Haematology
15/06/2020
Pesquisadores apresentam uma tecnologia que compreende um dispositivo microfluídico de separação de plasma sanguíneo que é capaz de separar efetivamente o plasma do sangue humano total, para fins de teste de diagnóstico. Aproximadamente 10 ml de plasma podem ser removidos usando 1 ml de sangue humano, em aproximadamente 3 min. O dispositivo visa a detecção de anticorpos COVID-19 usando uma plataforma ELISA no chip (10/06/2020). Fonte: Transactions of the Indian National Academy of Engineering
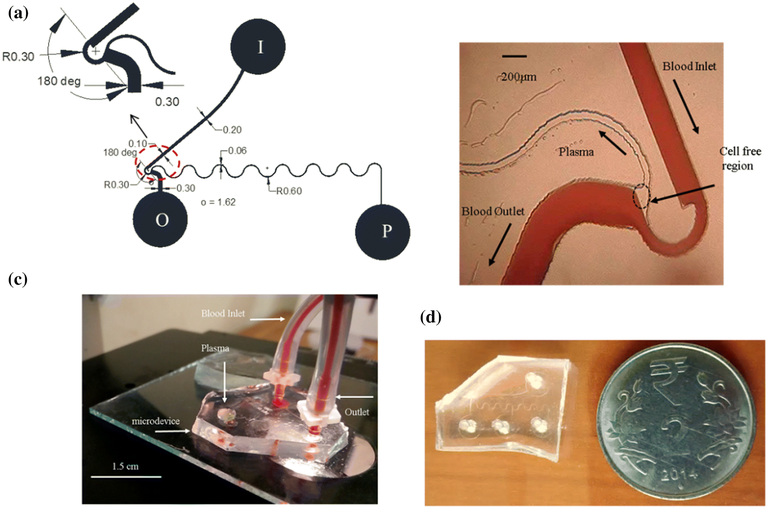
(a) Projeto de microdispositivo de plasma sanguíneo e visão ampliada na junção. Símbolos: I - entrada de sangue, O - saída de sangue, P - saída de plasma. (b) Fotografia experimental mostrando a separação do plasma no microdispositivo usando sangue total a uma taxa de fluxo de 0,5 ml/min. (c) Visão externa da separação do plasma sanguíneo que ocorre no microdispositivo PDMS. (d) Comparação do tamanho do dispositivo com uma moeda.
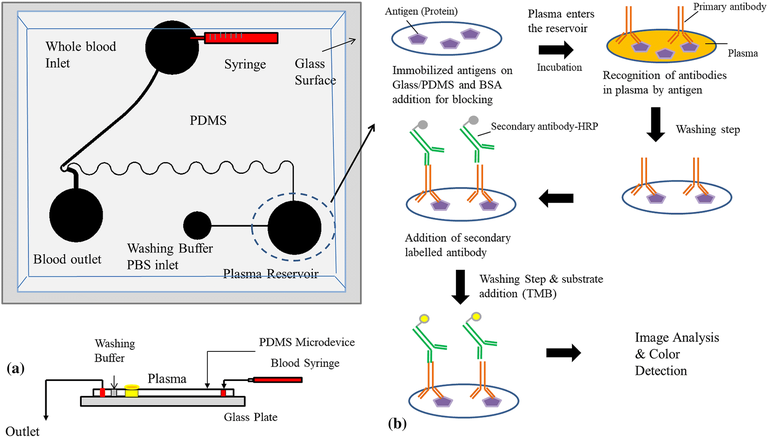
(a) Parte superior: máscara do projeto original do microdispositivo de separação de plasma sanguíneo com entrada adicional para realizar as etapas de lavagem e injeção de anticorpos. Parte inferior: vista lateral do microssistema. (b) ELISA experimental em sanduíche: mostrando etapas para identificar a presença de anticorpos SARS-CoV-2 (COVID-19) presentes no plasma sanguíneo.
Revisão da precisão diagnóstica dos testes sorológicos SARS-CoV-2 produziram uma sensibilidade sumária de 82% para IgM, e 85% para IgG e anticorpos totais. Para especificidade, a estimativa de agrupamento foi de 98% para IgM e 99% para IgG e anticorpos totais. Em populações com ≤ 5% dos indivíduos soro convertidos, a menos que os ensaios tenham 100% especificidade, o valor preditivo positivo seria ≤ 88%. Os testes sorológicos devem ser utilizados para levantamentos de prevalência apenas em áreas atingidas (11/06/2020). Fonte: Eurosurveillance
Artigo de revisão em que se fornece a descrição da tecnologia de amplificação isotermal, seu potencial e as lacunas que precisam ser consideradas para ser utilizados como teste rápido na detecção de SARS-CoV-2 (11/06/2020). Fonte: Diagnostics
Neste artigo, os autores fornecem uma visão geral sobre as características moleculares do vírus SARS-CoV-2 e resumem os esforços para desenvolver um teste de diagnóstico confirmatório rápido para COVID-19. Os desempenhos diagnósticos dos testes disponíveis são analisados com base nas informações da pesquisa inicial (13/06/2020). Fonte: Journal of Molecular Medicine
Revisão discute os métodos de diagnóstico aplicados à COVID-19 e suas limitações, reforçando a necessidade de se desenvolver testes acurados e rápidos para o controle epidemiológico da pandemia, principalmente nos países de baixa e média renda. Os autores discutem ainda a escolha do tipo espécime clínico a ser testado, que deve estar relacionado com as condições do paciente e o estágio do curso da doença. (14/06/2020) Fonte: New Microbes and New Infections
12/06/2020
O estudo teve como objetivo a determinação do volume de testes necessários, para vigilância epidemiológica. Esses volumes foram estimados utilizando-se métodos estatísticos baseados no desempenho analítico do teste, prevalência da doença, precisão desejada e tamanho populacional. Com os números estimados os autores levantam preocupações quanto à disponibilidade de teste suficiente para atender à demanda. Além disso, levantam a questão de que o uso dos testes para vigilância exigem um design cuidadoso e randomização para fornecer insights significativos (10/06/2020). Fonte: American Journal of Clinical Pathology.
10/06/2020
Estudo avalia os imunoensaios de alto rendimento, disponíveis comercialmente, usando diferentes antígenos recombinantes de SARS-CoV-2, funcionam com amostras clínicas. Com foco em anticorpos IgG e totais, demonstramos o desempenho de quatro imunoensaios automatizados em comparação com ensaios ELISA. Ao calcular a sensibilidade geral, em um período de 49 dias após a primeira positividade para PCR. A sensibilidade geral no grupo de ensaios à base de proteína N variou de 66,7 a 77,8% e nos ensaios à base de proteína S de 71,1 a 75,6% (31/05/2020). Fonte: Journal of Clinical Virology
O estudo avaliou imunoensaios para a detecção de anticorpos contra SARS-CoV-2. Especificamente, avaliou-se a produção de IgM e IgG e seu valor diagnóstico. Duzentos e quatorze pacientes confirmados de COVID-19 foram recrutados para fazer testes ELISA baseados na proteína N(rN) e na proteína S (rS) do SARS-CoV-2 para detectar anticorpos IgM e IgG. As taxas positivas dos testes ELISA baseados em rN e rS para detecção de anticorpos (IgM e/ou IgG) foram de 80,4% e 82,2%, respectivamente. ELISA tem alta sensibilidade, especialmente para a detecção de amostras de soro de pacientes com 10 dias do início da doença, por isso pode ser um importante método suplementar para o diagnóstico COVID-19 (26/05/2020). Fonte: Journal of clinical microbiology
Pesquisadores, usando ensaios ELISA para COVID-19, mediram anticorpos SARS-CoV-2 IgM e IgG em 64 pacientes com COVID-19 confirmados por RT-PCR para SARS-CoV-2 com amostras seriais de sangue (n = 104) coletados em diferentes momentos do início dos sintomas. Também foram utilizadas amostras de sangue de 200 doadores de sangue saudáveis e 256 pacientes de unidade de terapia intensiva (UTI) coletados antes do surto de COVID-19. Este estudo mostra altas taxas de positividade "verdadeira" vs. baixas taxas "falsa" para os testes ELISA SARS-CoV-2 IgM e IgG (08/06/2020) Pre proof. Fonte: Clinica Chimica Acta
09/06/2020
Pesquisadores da USP estão desenvolvendo uma plataforma digital que utiliza dados de pacientes para criar indicadores e auxiliar na tomada de decisão dos médicos no combate ao novo coronavírus. Apenas com dados de hemograma, o sistema utiliza inteligência artificial para ajudar os hospitais a agilizar o processo de diagnóstico e otimizar recursos (09/06/2020). Fonte: USP
Pesquisadores fazem uma revisão com as informações atualizadas sobre a seleção de amostras e disponibilidade de vários métodos de diagnóstico e sua utilidade com os resultados atuais para o diagnóstico laboratorial da infecção por SARS-CoV-2 (07/06/2020) In Press. Fonte: Journal of Infection and Public Health
Avaliação do teste rápido de antígenos para detecção do vírus SARS-CoV-2. Este estudo demonstrou que o teste RAD serve apenas como complemento do teste de RT-PCR devido ao potencial de resultados falso-negativos (08/06/2020) In Press. Fonte: Journal of Clinical Virology
08/06/2020
Autores descrevem que o gen nsp1, localizado na extremidade 5 'do genoma SARS-CoV ‐ 2, é altamente expresso nas amostras nasofaríngeas ou salivares de pacientes com COVID ‐ 19. Com base nessa descoberta, foi desenvolvido um novo ensaio de RT-PCR nsp1 em tempo real. Os primers e sondas são altamente específicos para SARS ‐ CoV ‐ 2. A validação com 101 amostras clínicas mostrou que o ensaio nsp1 RT ‐ PCR tem uma sensibilidade de 93,1%, semelhante aos dos ensaios RT ‐ PCR dos genes N e E. A especificidade diagnóstica foi de 100%. A adição de nsp1 para a detecção de SARS ‐ CoV ‐ 2 em vários alvos pode evitar resultados falso-negativos devido a mutações nos locais de ligação dos primers / sondas dos ensaios de RT-PCR atualmente disponíveis (05/06/2020). Fonte: Journal of Medical Virology.
05/06/2020
Estudo prospectivo avaliou a prevalência de soropositividade em profissionais de saúde assintomáticos através de testes rápidos a fim de que possa ser usado para dentificar possiveis individuos infectados. Foi considerando um total de 246 trabalhadores a estimativa de infectados por SARS-CoV-2 foi de 35 pacientes positivados e destes 23 assintomáticos e 12 sintomáticos (06/2020). Fonte: HemaSphere
04/06/2020
Estudo, avalia o desempenho de seis testes de “point of care” (POC) com CE-marcação e três ensaios ELISA para o diagnóstico de COVID-19, explorando soroconversões em pacientes hospitalizados que testaram positivo para RNA SARS-CoV-2. Os resultados demonstraram que os testes ELISA e POC foram capazes de detectar anticorpos SARS-CoV-2 em pelo menos metade das amostras coletadas sete dias ou mais após o início dos sintomas. Após 15 dias, a taxa de detecção aumentou para mais de 80%, mas sem atingir 100%, independentemente do teste utilizado (28/05/2020). Fonte: Journal of Infection
Em uma avaliação do desempenho diagnóstico de ensaios de imunocromatografia de fluxo lateral rápido (LFAs) em comparação com os ensaio de imunoabsorção enzimática (ELISA) e testes de ácidos nucleicos (NAT) em pacientes com suspeita de COVID-19, observou-se que os testes LFAs podem contribuir para rapidamente confirmar a COVID-19 em função da sua grande especificidade, no entanto resultados negativos não excluem a COVID-19 em função da sensibilidade reduzida destes tipos de testes (02/06/2020). Clinical Microbiology and Infection
Estudo comparativo analisa as diferentes ferramentas de diagnóstico para a COVID-19 que tem sido utilizadas no Brasil. Os autores sugerem que as três metodologias analisadas têm suas vantagens e desvantagens e podem e devem ser combinadas para identificar rapidamente os pacientes infectados, a fim de impedir a transmissão do vírus e garantir o tratamento oportuno dos pacientes, a fim de conter esse surto. (in press) Fonte: JRBA Assisted Reproduction
03/06/2020
A Empresa Brasileira de Pesquisa e Inovação Industrial (EMBRAPII), o Instituto de Pesquisa Tecnológica (IPT – Unidade EMBRAPII) e a startup de biotecnologia Aptah se uniram para desenvolver um teste rápido, com espera máxima de uma hora para o resultado e sem necessidade de deslocamento ou exposição ao ambiente hospitalar. O exame identifica a presença do RNA do novo coronavírus permitindo o diagnóstico em estágios iniciais de infecção (06/05/2020). Fonte: EMBRAPII
Em artigo da Nature pesquisadores citam que como a maioria dos testes de anticorpos foi validada usando amostras de sangue de pessoas hospitalizadas com doença grave, ou seja, com altos níveis mais de anticorpos circulando em seu corpo, podem ser ineficazes para pessoas com sintomas leves ou inexistentes. Os pesquisadores dizem que são necessários estudos mais detalhados para avaliar até que ponto os testes de anticorpos detectam infecções anteriores em pessoas com doenças leves (03/06/2020). Fonte: Nature
Avaliação de teste rápido de detecção de antígeno rápido e de fácil manuseio apresentou alta sensibilidade e especificidade de diagnóstico em amostras respiratórias obtidas de pacientes na primeira semana de sintomas da COVID-19. O teste de imunofluorescência baseado em antígenos pode ser benéfico para diagnóstico precoce e em locais de acesso limitado a testes moleculares (01/06/2020). Fonte: International Journal of Infectious Diseases.
Estudo apresenta o desempenho clínico do teste de diagnóstico molecular Painel Estendido Luminex NxTAG CoV para detecção de SARS-CoV-2 em amostras nasofaríngeas de pacientes com COVID-19 em Hong Kong. O teste, que é simples de usar, demonstrou alta sensibilidade (97,8%) e alta especificidade (100%) ao SARS-CoV-2 em amostras nasofaríngeas, alem disso, foi observada alta concordância com o protocolo de rotina COVID-19 RT-PCR. Os pesquisadores recomendam esse sistema de diagnóstico para a triagem de COVID-19 de alta produtividade na comunidade (01/06/2020). Fonte: Journal of Clinical Microbiology
02/06/2020
Além de testes de RNA para diagnóstico da COVID-19, é necessária a avaliação de testes rápidos de diagnóstico. Estudo realizado com 87 pacientes discute a importância de testes sorológicos para detecção de anticorpos IgA e a conversão sorológica, inclusive em pacientes assintomáticos. (28/05/2020). Cellular & Molecular Immunology
01/06/2020
O CT Vacinas, núcleo formado por pesquisadores da UFMG e da Fundação Oswaldo Cruz (Fiocruz), desenvolveu um teste para detecção da COVID-19 baseado no método conhecido como Elisa. o Elisa é um teste sorológico mais sensível do que os exames rápidos, ou seja, menos passível de fornecer resultados “falsos negativos”. Diferentemente dos exames rápidos, o Elisa só é realizado dentro do laboratório (01/06/2020). Fonte: UFMG
Estudo em 774 pacientes, nos quais 714 amostras negativas foram enviadas para confirmação e destas 159 foram positivadas pelo qRT-PCR. A concordância percentual positiva mediana foi de 23,9% para o ensaio antigênico COVID-19 Ag Respi-Strip. Estudo conclui que a utilização deste ensaio imunocromatográfico como teste de triagem não reduziu significativamente o número de amostras para confirmação de COVID-19 por qRT-PCR (30/05/2020). Fonte: Journal of Clinical Virology
28/05/2020
Em carta pesquisador cita que os testes de PCR para SARS-CoV-2 estão longe de serem qualitativamente confiáveis e nunca indicam como a doença pode progredir em um indivíduo. À medida que o COVID-19 se torna endêmico, há uma necessidade de testes sorológicos precisos para detectar anticorpos contra antígenos SARS-CoV-2 e marcadores prognósticos para direcionar as opções de tratamento (27/05/2020). Fonte: The lancet
27/05/2020
Laboratório brasileiro anunciou um novo teste para identificar casos de COVID-19. Trata-se de uma análise feita a partir de proteínas de amostras extraídas do nariz e da garganta de pacientes. O exame tem sensibilidade próxima ao RT-PCR. O novo teste permite que as amostras sejam processadas de forma automatizada, sem necessidade de manipulação, e sem necessidade de refrigeração. Adicionalmente, o teste não utiliza os mesmos insumos necessários para a análise molecular, portanto, seria uma alternativa à atual falta de estoque por conta da demanda mundial de testes. Os testes já estão disponíveis para hospitais e clínicas e o prazo para resultados é de três dias úteis. (27/05/2020) Fonte: Veja
Pesquisadores apresentam revisão sobre detecção eletroquímica de vírus e anticorpos. Segundo estudo, os sensores eletroquímicos de alta sensibilidade para DNA viral permitem a detecção precoce da doença e o teste de anticorpos permite avaliar a extensão da doença e o status de imunidade dos indivíduos recuperados. Os desafios permanecem em termos de seletividade, prazo de validade, capacidade de fabricação e uso de materiais sustentáveis (26/05/2020). Fonte: Electrochemistry Communications

Pesquisadores desenvolvem teste CRISPR-FDS para COVID-19 que utiliza uma abordagem simplificada que não requer nenhum equipamento especial além do encontrado na maioria dos laboratórios clínicos e de pesquisa (diferente do RT-qPCR padrão). O CRISPR-FDS emprega três etapas intimamente ligadas: extração de RNA, amplificação de alvo e detecção de sinal fluorescente. Essa abordagem permitiu a detecção sensível e robusta de amostras positivas para SARS-CoV-2, com um tempo de resposta da amostra de ∼50min e um limite de detecção de 2 cópias por amostra. Os resultados do diagnóstico do ensaio CRISPR obtiveram amostras de swab nasal de indivíduos com suspeita de casos de COVID-19 foram comparáveis aos resultados pareados de um ensaio de qPCR aprovado pelo CDC (23/05/2020). Fonte: Biosensors and Bioeletronics
25/05/2020
Estudo apresenta um método de detecção viral mais sensível que o RT-PCR. Apesar de apresentar a mesma especificidade que o RT-PCT, o “droplet digital PCR” (ddPCR) se mostrou mais sensível na detecção de ácido nucleico do vírus em swabs quando as concentrações do vírus eram menores, apresentando assim menos resultados falso-negativos que o RT-PCR (22/05/2020). Fonte: Emerging Microbes & Infections
20/05/2020
Artigo faz uma análise de artigos científicos para determinar a taxa de falsos negativos de testes para SARS-CoV-2 que utilizam RT-PCR de acordos com o tempo de exposição. O estudo conclui que a taxa de falsos negativos é alta, tanto no período de 5 dias após a exposição (até 67%) quanto após o oitavo dia de exposição (21%). Portanto, indica que casos de COVID-19 não podem ser descartados pelo RT-PCR sozinho (18/05/2020). American College of Cardiology
19/05/2020
Relato de caso indica RT-PCR positivo na urina de um paciente assintomático com infecção por COVID-19. Autores sugerem o exame da urina caso, na triagem o RT-PCR da garganta for negativo (18/05/2020). Fonte: Infection Diseases
Estudo faz uma meta-análise através da revisão de quatro trabalhos que sugerem as troponinas como um marcador preditivo de severidade da COVID-19. Autores propões que a troponina elevada seja considerada como fator de risco, relacionado com aumento da mortalidade em pacientes internados. (13/05/2020) Fonte: Journal of Infection
18/05/2020
Estudo demonstra que o nível de PCR plasmática está diretamente relacionado com a gravidade da pneumonia por COVID-19. Os pesquisadores sugerem que o nível de PCR pode ser usado como um indicador de pacientes com pneumonia moderada a grave e assim dividir os pacientes para UTIs (15/05/2020). Fonte: Annals of Clinical Microbiology and Antimicrobials
14/05/2020
Artigo de revisão que analisa os avanços em relação uso de sistemas CRISPR-Cas, especialmente CRISPR-Cas9, CRISPR-Cas12 e CRISPR-Cas13, no desenvolvimento de testes de diagnóstico rápidos, precisos e portáteis. O artigo destaca o potencial do CRISPR-Cas13 para diagnóstico da COVID- 19 (13/05/2020). Fonte: Journal of Drug Targeting
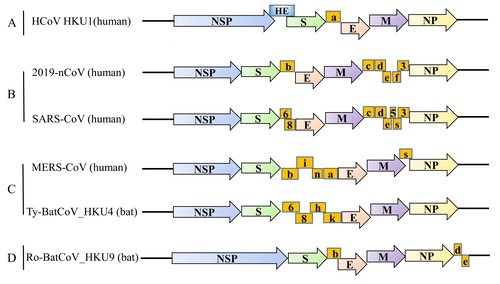
A imunoglobulina intravenosa atualmente disponível contém anticorpos que reagem contra antígenos do SARS-CoV-2. Os produtos foram testados usando técnicas de ELISA para detecção de anticorpos contra vários antígenos de betacoronaviruses humanos. Para SARS-CoV-2, foi observada reatividade positiva em concentrações de IVIG variando de 100 μg / ml com Gamunex-C a 1 mg / ml com Flebogamma 5% DIF (12/05/2020). Fonte: Immunotherapy
Artigo revela um método para rastrear um grande número de pacientes que envolve a combinação de várias amostras de pacientes em uma única amostra de teste e, caso positivado fazer os testes individualmente (13/05/2020). Fonte: Journal of Medical Virology
13/05/2020
Pesquisadores descrevem um ELISA para a triagem e identificação de soroconversão em humanos para o SARS-CoV-2. Este ensaio não requer o manuseio de vírus infeccioso, pode ser ajustado para detectar diferentes tipos de anticorpos no soro e no plasma e é passível de expansão. Os ensaios sorológicos são de importância crítica para ajudar a definir a exposição anterior de populações ao SARS-CoV-2, identificar doadores humanos reativos para terapia com plasma convalescente e investigar correlatos de proteção (12/05/2020). Fonte: Nature MedicineArtigo de revisão que explica os diferentes tipos de testes para COVID-19 e identifica as incertezas nos resultados dos mesmos (12/05/2020). Fonte: BMJ
Apesar de vários testes de sorologia para SARS-CoV-2 estarem em uso, a busca por técnicas com maior sensibilidade e especificidade é essencial para detecção de infecções prévias na população. Empregando o sistema de imunoprecipitação Luciferase (LIPS), foram avaliados os perfis de anticorpos contra SARS-CoV-2 para 15 antígenos do vírus. Foram identificados novos alvos imunogênicos, mesmo no início da doença (02/05/2020). Fonte: MedRxiv.
12/05/2020
Pesquisadores da Força-tarefa de modelagem da COVID-19, sediada na UFMG, desenvolveram uma estratégia de aplicação da técnica de testagem em grupo (group testing) para o vírus Sars-CoV-2 que possibilita promover uma grande expansão da atual capacidade de exames das infraestruturas laboratoriais existentes no país (12/05/2020). Fonte: UFMGMetodologia desenvolvida pela Hemominas pode aumentar em 40 vezes o número de diagnósticos de testes de COVID-19. A metodologia consiste em unir várias amostras em uma só, agilizando o processo. Caso a presença do coronavírus seja detectada, o método que identifica qual o paciente, dentre todos aqueles analisados ao mesmo tempo, está infectado. (12/05/2020) Fonte: G1
Avaliação da performance de novo RT-PCR em tempo real (Simplexa™ COVID-19 Direct assay), que não requer extração separada. O teste com alta sensibilidade e especificidade promete diagnóstico laboratorial mais rápido que outros ensaios que requerem extração e tecnologias de amplificação (04/05/2020). Fonte: Journal of Clinical Virology.
Estudo mostra o desenvolvimento de um kit de teste rápido para SARS-CoV-2. Foi escolhido um teste de antígeno baseado em RT-LAMP com leitura colorimétrica. O uso direto de amostra de swab sem extração de RNA foi explorado. Após extenso estudo experimental, um kit de teste rápido foi fabricado para atender a todos os critérios de projeto (11/05/2020). Fonte: Bio-Design and Manufacturing.
Pesquisadores realizam comparação da detecção de SARS ‐ CoV ‐ 2 a partir de amostras de swab nasofaríngeo pelo teste Roche cobas® 6800 SARS ‐ CoV ‐ 2 e um teste de RT ‐ PCR em tempo real desenvolvido em laboratório. Segundo estudo, uma taxa geral de discordância de 4,2% entre os dois sistemas pode refletir diferenças nas seqüências de iniciadores, limite de detecção de teste ou outros fatores, destacando a importância de comparar o desempenho de diferentes plataformas de teste (08/05/2020). Fonte: Journal of Medical Virology
11/05/2020
Por meio da avaliação de 45 paciente, os autores propõem o uso das concentrações séricas de IL-6 como biomarcador de progressão da doença.(08/05/2020) Fonte: GENETICS IN MEDICINEOs autores apresentam a técnica de detecção de IgG e IgM por ensaio imunológico quimioluminescente magnético (CMIA) e propõe seu uso combinado com outros métodos. (08/05/2020) Fonte: J Infect Dis.
O FDA concedeu sua primeira aprovação de uso emergencial para um novo teste de coronavírus que utiliza a tecnologia de edição de genes CRISPR (08/05/2020). Fonte: Nature
08/05/2020
Estudo indica que células T CD3+, CD4+, CD8+ e células Natural Killer (NK) diminuem drasticamente em pacientes com COVID-19 e, portanto, os autores propõe a contagem de subsets de células T no sangue periférico como biomarcadores de prognóstico relacionado à severidade da COVID-19. (07/05/2020) Fonte: J Infect Dis
07/05/2020
Grupo de pesquisadores do MIT e Harvard desenvolveram um teste para o SARS-CoV-2 mais rápido e mais simples que o procedimento atual, que exige equipamentos de laboratório caros e reagentes escassos. O protocolo CRISPR da equipe pode ser executado por um leigo e por um equipamento de cozinha normalmente barato e disponível. O teste disponibiliza resultados em tiras de papel semelhantes às usadas nos testes de gravidez (07/05/2020) Pre print. Fonte: NatureEstudo reporta um novo teste diagnóstico rápido que utiliza nano partículas de citrato de ouro revestida com o lisado do vírus. A amostra do plasma do sangue ou soro é testada, em caso positivo as nano partículas agregam, e a formação é detectada usando uma técnica espalhamento de luz dinâmico. O processo é rápido e já foi testado em diversos tipos de vírus como Zica, dengue e chicungunha e pode ser adaptado para uma gama de doenças infecciosas virais como COVID-19(Pre-print 06/05/2020). Fonte: Sensors International
06/05/2020
Estudo usando 483 amostras investigou características analíticas de desempenho do teste Xpress SARS-CoV-2 (teste molecular rápido e automatizado), avaliando a sensibilidade e a especificidade ao SARS-CoV-2 frente a outras espécies. Os resultados demonstraram 99,5% de concordância positiva e 95,8 % de negativa, demonstrando uma detecção precisa e sensível do SARS-CoV-2 com resultado em aproximadamente 45 minutos (04/05/2020). Fonte: Journal Clinical MicrobiolArtigo faz um estudo da performance de dois testes rápidos IgG/IgM, IgG/IgA e teste de fluxo lateral. Os dois primeiros mostraram especificidade semelhantes de IgG e os resultados dos ensaios de fluxo lateral foram facilmente interpretáveis com bandas de leitura coloridas (05/05/2020). Fonte: Journal of Clinical Virology
05/05/2020
Reações de hibridização em cadeia (HCR, em inglês) para genes relacionados às fosfoproteínas nucleocapsídicas do SARS – CoV-2 e a RNase P humana são propostas para fornecer uma ferramenta para melhorar o rastreamento e prevenção de novas epidemias. (01/05/2020). Fonte: International Journal of Molecular Science.
04/05/2020
Avaliando os dados laboratoriais de 140 pacientes, os autores propõem o uso das concentrações séricas de IL-6, Proteína C Reativa e Procalcitonina como indicadores efetivos da gravidade da COVID-19 (04/05/2020_ In press). Fonte: Journal of Clinical VirologyArtigo apresenta uma revisão dos recentes avanços em relação teste baseados em ácido nucleico, incluindo artigos revisados por pares e “pre-print”, com isso o artigo tem como objetivo consolidar e disseminar a informação para ajudar os pesquisadores a desenhar e otimizar protocolos de testes e aumentar a disponibilidade acurácia e velocidade dos testes para COVID-19 (01/05/2020). Fonte: RNA
29/04/2020
A UFMG prevê o desenvolvimento de um software baseado em inteligência artificial e aprendizado de máquina para auxiliar na detecção automática de síndromes respiratórias agudas, como a Covid-19 e a H1N1 (28/04/2020). Fonte: UFMGCentro de Estudos de Venenos e Animais Peçonhentos da Unesp (Cevap), localizado no campus de Botucatu, uniu-se ao Instituto Biológico de São Paulo, à Organização Pan-Americana da Saúde (OPAS), ao Instituto Vital Brazil, à Fundação Ezequiel Dias e a empresas farmacêuticas brasileiras e americanas para desenvolver tratamento inovador baseado em nanocorpos para o combate à Covid-19 em pacientes infectados (28/04/2020). Fonte:Unesp
Os testes genéticos em larga escala são dificultados, em parte, pela escassez de soluções usadas para armazenar amostras e extrair RNA viral delas. Para superar essa dificuldade, uma equipe da Universidade de Washington em Seattle, desenvolveu um procedimento diferentes para detectar RNA viral nos swabs (29/04/2020). Fonte: Biorexiv
28/04/2020
A ANVISA aprovou a proposta de realização de testes rápidos (ensaios imunocromatográficos) de anticorpos para o novo coronavírus (Sars-CoV-2) em farmácias e drogarias. A medida tem caráter temporário e excepcional e visa ampliar a oferta e a rede de testagem, bem como reduzir a alta demanda em serviços públicos de saúde durante a pandemia. No entanto, é importante ressaltar que os testes não têm finalidade confirmatória, servindo apenas para auxiliar no diagnóstico da Covid-19 (28/07/2020). Fonte: ANVISA
27/04/2020
Solução desenvolvida pelo Pasteur-TheraVectys detecta anticorpos e mede, acima de tudo, sua capacidade de inibir a entrada do vírus nas células. Permite classificar a resposta imunológica em três categorias: forte neutralizante [do vírus], fraco ou não neutralizante (27/04/2020). Fonte.: RFIAtualização das diretrizes do CDC americano para avaliação e teste de pacientes para COVID-19 (27/04/2020). Fonte CDC.
Pesquisadores da Universidade de Yale de modo a melhorar o processo de teste de COVID-19 demonstraram em um preprint que a saliva é mais sensivel que o uso de swab nasofaríngeo para detecção de SARS-Cov-2 (22/04/2020). Fonte: MedRxiv.
23/04/2020
A ANVISA lançou a plataforma Business Intelligence (BI), que proporciona transparência à situação dos pedidos de produtos de diagnóstico in vitro protocolados na Agência (23/04/2020). Fonte: ANVISA
22/04/2020
Artigo da Nature questiona se o uso de testes rápidos baseados na resposta imune do indivíduo podem ser utilizados para ajudar a acabar o isolamento visto que pode podem apresentar resultados falsos. A OMS e o FDA afirmam que apenas testes PCR-para o vírus deveriam ser utilizados para confirmar os casos (21/04/2020). Fonte: NatureArtigo do Lancet faz uma revisão da importância e uso de testes sorológicos (baseados na resposta imune do indivíduo) para identificação rápida de casos e seu uso em políticas de controle. O artigo aponta que como testes PCR não identificam infecções passadas, os testes e dados sorológicos serão cada vez mais importantes para entender o passado das pandemias e prever seu futuro (21/04/2020). Fonte: The Lancet Infectious Diseases
Anvisa publica artigo explicando sobre o teste rápido de anticorpos (baseados na resposta imune do indivíduo) para o novo coronavírus (SARS-CoV-2). O teste pode ser usado como apoio para a avaliação do estado imunológico de pacientes que apresentem sintomas da COVID-19. (21/04/2020). Fonte: Anvisa
21/04/2020
Artigo demonstra um novo ensaio de teste RT-LAMP rápido através de amplificação isotérmica mediada por loop de transcrição reversa (RT-LAMP) para a detecção específica de SARS-CoV-2. O ensaio exibiu um intervalo de detecção rápida de 30 min, combinado com a visualização colorimétrica. Este teste pode detectar RNAs virais específicos do SARS-CoV-2 sem reatividade cruzada a coronavírus relacionados, como HCoV-229E, HCoV-NL63, HCoV-OC43 e MERS-CoV, além de vírus da influenza humana infecciosa (tipo B, H1N1pdm, H3N2, H5N1, H5N6, H5N8 e H7N9) e outros vírus causadores de doenças respiratórias (RSVA, RSVB, ADV, PIV, MPV e HRV). O artigo demonstra uma alta sensibilidade e especificidade, essa amplificação isotérmica conjugada com um método de detecção colorimétrica de tubo único pode contribuir para as respostas de saúde pública e controle de doenças, especialmente nas áreas com capacidades laboratoriais limitadas (20/04/2020). Fonte: Emerging Microbes & Infections
20/04/2020
Nos próximos dias, a produção semanal de testes da Fiocruz vai decuplicar, passando de 20 000 para 200 000 kits. A Fiocruz é o maior produtor nacional, responsável por abastecer toda a rede pública de saúde. (20/04/2020) Fonte: Jornal da Manhã
18/04/2020
ANVISA publica perguntas e respostas sobre os testes disgnósticos realizado no Brasil, as respostas se referem ao testes para detecção de doenças como a COVID-19, os tipos de amostras usadas e sobre como sedá o registro dos mesmos. Fonte: ANVISAO Banco do Brasil e o Bradesco vão doar R$ 20 milhões à Fundação Oswaldo Cruz (Fiocruz) para ajudar no combate ao novo coronavírus. O dinheiro será usado na produção de kits de diagnósticos rápidos para o COVID-19, que serão destinados ao Ministério da Saúde. todos os kits já contam com tecnologia brasileira desenvolvida pela Fiocruz. (18/04/2020) Fonte: Globo.com
UFMG amplia capacidade de realização de testes para detectar o coronavírus. Laboratório da Faculdade de Medicina deverá processar 1 mil exames por dia até o fim do mês (17/04/2020). Fonte: UFMG
17/04/2020
Características e comparação entre testes de diagnoóstico para COVID-19 “drive-through” e “walk-through” empregados na Coréia do Sul (16/04/20). Fonte: Clincal end Experimental Emergency Medicine.Unicamp usa reagentes nacionais e desenvolve teste de coronavírus mais barato. Foram realizadas parcerias com empresas de biotecnologia e startups para desenvolver exame sem dependência de insumos internacionais, em falta no mercado. (08/04/2020) Fonte: G1
A Anvisa mantém em seu portal relação de produtos para diagnóstico in vitro para detecção do COVID-19 regularizados. Esta lista é atualizada diariamente na página da agencia. Os registros concedidos nas condições (emergenciais) do Art. 12 da RDC 348/2020 terão validade de 1 (um) ano. Já os produtos registrados com base no Art. 11 da mesma Resolução e aqueles que atendem a totalidade dos requisitos da RDC 36/2015 terão a validade de registro padrão de 10 (dez) anos. (Atualização diária) Fonte: ANVISA
14/04/2020
Bio-Manguinhos obteve junto à Anvisa registro para seus dois kits de diagnóstico para o novo coronavírus: o Kit TR DPP Covid-19,detectar simultaneamente anticorpos das classes IgM (infecção recente, a partir do 5º dia após o início dos sintomas) e IgG (memória) de forma independente e diferencial, e o Kit Molecular SARS-CoV2, capaz de detectar a infecção viral desde o primeiro dia do aparecimento dos sintomas mesmo quando a carga viral no paciente é baixa. (14/04/2020) Fonte: Bio-Manguinhos/Fiocuz
13/04/2020
Para aumentar o número de diagnósticos da covid-19 no Brasil, pesquisadores do Instituto de Ciências Biomédicas (ICB) da USP desenvolveram diferentes métodos, em três frentes. Um deles permite fazer testes para identificar o vírus em equipamentos disponíveis na maioria dos laboratórios do País (13/04/2020). Fonte: Jornal da USP
O INCQS/ Fiocruz realiza análises prévias nos kits de diagnóstico, que são compostos por conjuntos e reagentes, calibradores e controles, de classe 3 (no caso de surtos) e de classe 4, para compor o processo de registro junto à Agência Nacional de Vigilância Sanitária (Anvisa). (13/04/2020) Fonte: INCQS/Fiocruz12/04/2020
Cientistas brasileiros, em corrida contra o tempo, avaliam a eficácia de testes para diagnóstico no novo coronavírus (12/04/2020). Fonte: G1.
10/04/2020
A Agência Biomédica Federal da Rússia (FMBA) lançou dois novos sistemas de teste, baseados em chips de detecção de coronavírus. Um deles permite reduzir o tempo de teste de 90 para 15-20 minutos (10/04/2020). Fonte: The General Digital-Partner
09/04/2020
Pesquisadores avaliam a precisão dos parâmetros laboratoriais na detecção de pacientes COVID-19 com RT-PCR positivo. Os achados sugerem que os níveis de desidrogenase de lactato (LDH), proteína C reativa (PCR), alanina aminotransferase (ALT) e neutrófilo (NEU) podem ser usados para prever o resultado do teste COVID-19 (04/04/2020). Fonte: Arch Acad Emerg MedEditorial discute os desafios de se desenvolver um teste de diagnóstico para um novo patógeno no curso de uma pandemia, ressaltando a importância da comunicação entre os profissionais do laboratório envolvidos e a administração do hospital.
08/04/2020
ANVISA publica atualização periódica dos produtos autorizados para diagnóstico de COVID-19. Fonte: ANVISAPesquisadores chineses desenvolvem teste rápido, simples, sensível e para detecção do novo Coronavirus SARS-CoV-2. O teste de RT-LAMP (reverse transcription loop-mediated isothermal amplification) foi comparado ao RT-PCR (08/04/2020) Fonte: Clinical Microbiology and Infection
07/04/20202
O estudo retrata a atual evolução celular, epidemiologia e diagnóstico em resposta ao surto de COVID-19. Além disso, mostra que os estudos explorando o genoma e a estrutura das proteínas virais são essenciais para definir prevenção (07/04/2020). Fonte: Chemotherapy
06/04/2020
Os diagnósticos etiológicos da COVID-19, são baseados essencialmente nos aspectos virológicos (como por exemplo testes moleculares RT-PCR), o artigo aponta para necessidade da identificação de biomarcadores (novos ou conhecidos), para guiar os médicos e profissionais de laboratório (06/04/2020). Fonte: Clinical Chemistry and Laboratory Medicine (CCLM)
04/04/2020
ANBIOTEC informa que a startup iBench está oferecendo produtos de diversos fornecedores nacionais, inclusive a matéria-prima para os testes do COVID-19, reagentes e insumos para os testes de diagnóstico como Taq e Master Mix produzidos por biotecnologia nacional. A empresa Enzytec Biotecnologia, que trabalha no desenvolvimento de kits diagnóstico e registro de produtos junto à Anvisa, está apoiando gratuitamente as indústrias nacionais nos primeiros registros de produtos para detecção do coronavírus no Brasil. Já a startup Pickcells desenvolveu um algoritmo para identificar pneumonia em exames de imagens (04/04/2020). Fonte: ANBIOTEC
Conheça as vantagens e desvantagens dos diferentes tipos de teste para diagnosticar coronavírus: RT-PCR, testes rápidos e testes sorológicos estão chegando ao Brasil e têm características variadas (04/04/2020). Fonte: O Globo03/04/2020
UFPB prepara dois laboratórios para teste de COVID-19 e parceria da UFPB com o Lacen/PB viabiliza 40 testes de COVID-19 por dia (03/04/2020). Fonte: UFPB, UFPB
02/04/2020
Laboratório de Virologia Molecular da UFRJ faz 280 testes por dia e lança campanha TESTAR-TESTAR-TESTAR, para obter recursos para atender 10 mil pessoas (02/04/2020). Fonte: G1
31/03/2020
Estudo retrospectivo mostra que ~15% dos pacientes COVID-19 que se tornam swab-negativo para o vírus permanecem com o mesmo detectável no escarro ou nas fezes (31/03/2020). Fonte: Annals of Internal Medicine
29/03/2020
Pesquisadores das Universidades de Campinas (Unicamp) e de São Paulo (USP) uniram esforços para desenvolver um teste rápido e de baixo custo para diagnosticar os casos de COVID-19 e, além disso, identificar os pacientes com risco de evoluir para quadros de insuficiência respiratória (29/03/2020). Fonte: FAPESP
27/03/2020
FDA aprova teste diagnóstico da Abbott que dá resultado em 15 minutos (Abbott) (27/03/2020). Fonte: UOL
26/03/2020
Reino Unido encomenda 3.5 milhões de testes para verificar se a pessoa já teve contato com o COVID-19 da empresa holandesa Sensitest, que promete vender na AMAZON (26/03/2020). Fonte: NATURE
25/03/2020
Startup paranaense Hi Technologies desenvolve teste rápido para COVID-19. (25/03/2020) Fonte: FINEP
23/03/2020
Coppe e UFRJ desenvolvem novo teste para detecção do SARS-CoV2 mais simples e a um custo quatro vezes mais baixo (23/03/2020). Fonte: UFRJ