Notícias
Ministério da Saúde discute redução de preços para viabilizar tratamento no SUS de pacientes no estágio 2 da Polineuropatia Amiloidotica Familiar (PAF)

Com uma audiência pública marcada para a próxima quarta-feira (14), o Ministério da Saúde (MS) busca viabilizar uma alternativa no SUS para o tratamento de pacientes com amiloidose hereditária relacionada à transtirretina com polineuropatia (PAF) em estágio 2 ou que apresentem resposta inadequada ao medicamento tafamidis (incorporado em 2018). A doença é grave e ultrarrara, e nesse estágio ainda sem opção medicamentosa na rede pública de saúde. Dois medicamentos, inotersena e patisirana sódica, já foram avaliados pela Conitec para esse grupo, e ambos receberam recomendação desfavorável à incorporação em razão do elevado impacto orçamentário para o Sistema Único de Saúde, ainda que comprovados benefícios clínicos para os pacientes que vivem com a doença.
Para mais informações, clique aqui .
Além da área técnica responsável pela Política Nacional de Atenção Integral às Pessoas com Doenças Raras no MS, representantes dos dois fabricantes das tecnologias foram convidados para falar sobre o assunto.
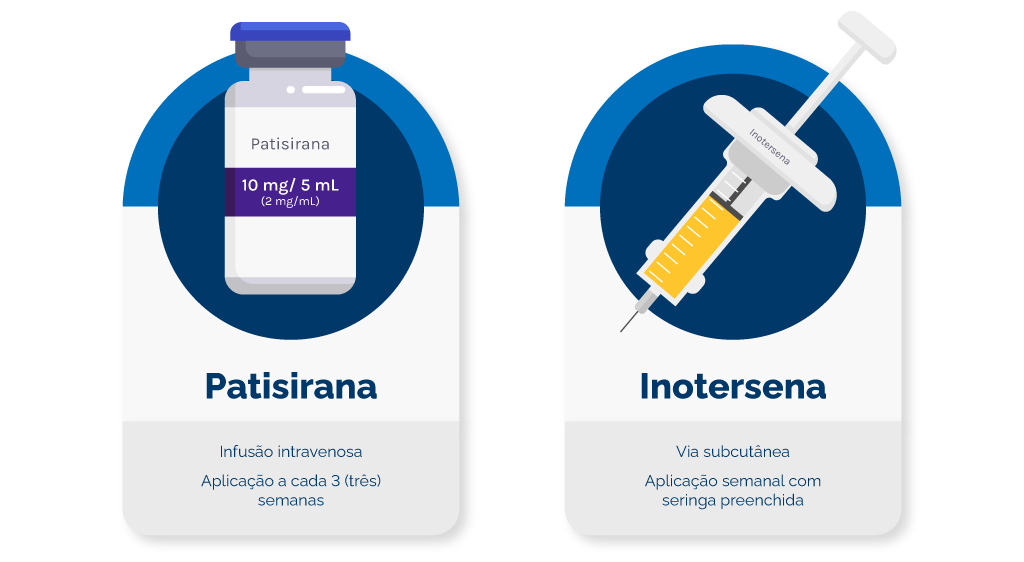
Os pedidos para avaliação do inotersena e patisirana foram enviados por seus fabricantes em momentos distintos: em fevereiro e agosto de 2022, respectivamente, ocasionando a avaliação pela Conitec também em períodos diferentes. No geral, observou-que as duas tecnologias demonstraram eficácia e segurança em retardar a progressão da doença, porém com alta razão de custo-efetividade e um alto impacto orçamentário para o SUS. Por esse motivo, a Secretaria-Executiva da Comissão providenciou um relatório de comparação indireta de ambas as tecnologias a fim de auxiliar na tomada de decisão. O conteúdo foi apresentado ao colegiado em março de 2023. Para consultar, acesse https://www.gov.br/conitec/pt-br/midias/relatorios/2023/20230511_relatorio_799_inotersena_pafttr.pdf .
A audiência será online e haverá transmissão ao vivo a partir das 16h no pelo canal da Conitec no YouTube . Posteriormente, a gravação será disponibilizada no site oficial da Comissão.As contribuições compartilhadas ao longo da audiência serão utilizadas para subsidiar a tomada de decisão da Secretaria de Ciência, Tecnologia, Inovação e Complexo da Saúde (SECTICS/MS) do Ministério da Saúde.
Avaliação econômica das tecnologias
Estima-se que haja 219 pessoas com PAF relacionada à transtirretina em estágio 1 não respondedoras ao Tafamidis e em estágio 2 da doença que seriam candidatas ao tratamento. O custo anual por paciente seria de R$ 1.194.556,00 com patisirana e R$ 1.337.807,00 com inotersena, considerando-se os últimos preços oferecidos ao SUS.